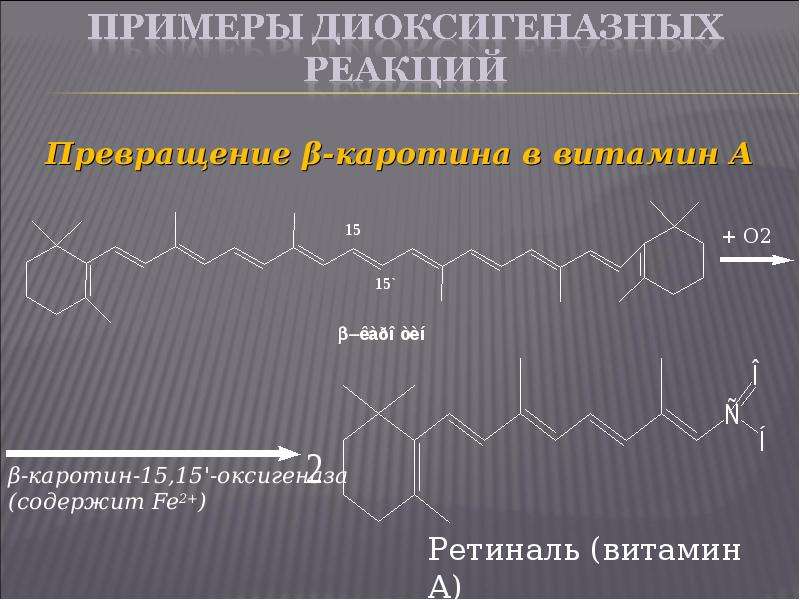
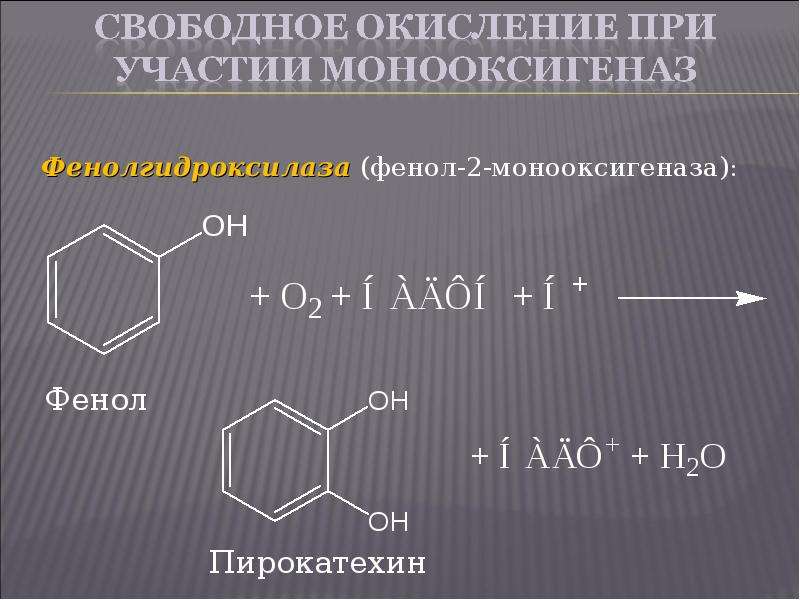
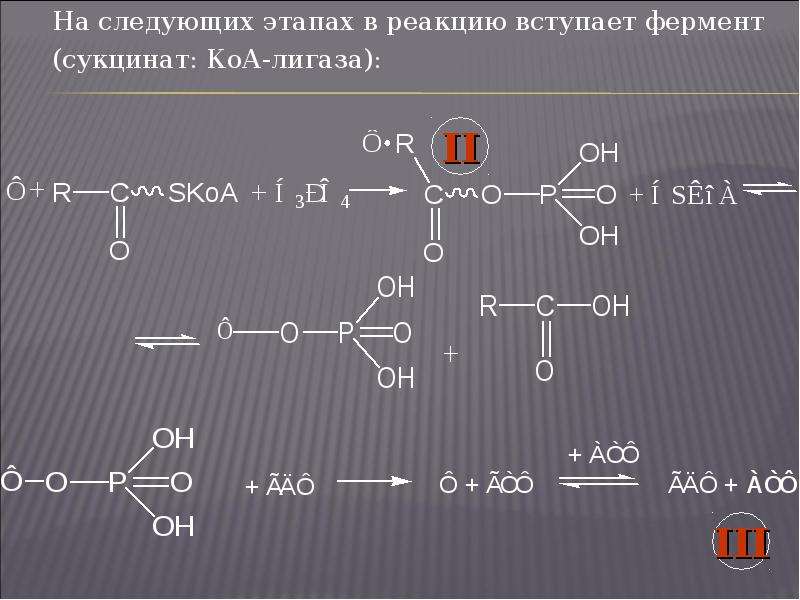
Презентация На тему "Биологическое окисление" - скачать бесплатно презентации по Биологии онлайн
На нашем сайте вы можете скачать и просмотреть онлайн доклад-презентацию на тему На тему "Биологическое окисление" - скачать бесплатно презентации по Биологии абсолютно бесплатно. Урок-презентация на эту тему содержит всего 38 слайдов. Все материалы созданы в программе PowerPoint и имеют формат ppt или же pptx. Материалы и темы для презентаций взяты из открытых источников и загружены их авторами, за качество и достоверность информации в них администрация сайта не отвечает, все права принадлежат их создателям. Если вы нашли то, что искали, отблагодарите авторов - поделитесь ссылкой в социальных сетях, а наш сайт добавьте в закладки.
Презентации » Биология » На тему "Биологическое окисление" - скачать бесплатно презентации по Биологии
Оцените!
Оцените презентацию от 1 до 5 баллов!
- Тип файла:ppt / pptx (powerpoint)
- Всего слайдов:38 слайдов
- Для класса:1,2,3,4,5,6,7,8,9,10,11
- Размер файла:6.80 MB
- Просмотров:60
- Скачиваний:0
- Автор:неизвестен
Слайды и текст к этой презентации:
№3 слайд


Содержание слайда: Энергетическое обеспечение:
Энергетическое обеспечение:
а) поддержания температуры тела;
б) биолюминесценции (свечения);
в) химических синтезов;
г) осмотических явлений;
д) электрических процессов;
е) механической работы.
Синтез важнейших (ключевых) метаболитов.
Регуляция обмена веществ.
Устранение вредных для клетки продуктов обмена (шлаков).
Детоксикация проникших в организм чуждых соединений – ксенобиотиков (пестицидов, препаратов бытовой химии, лекарственных средств, промышленных загрязнений и т.п.).
№4 слайд
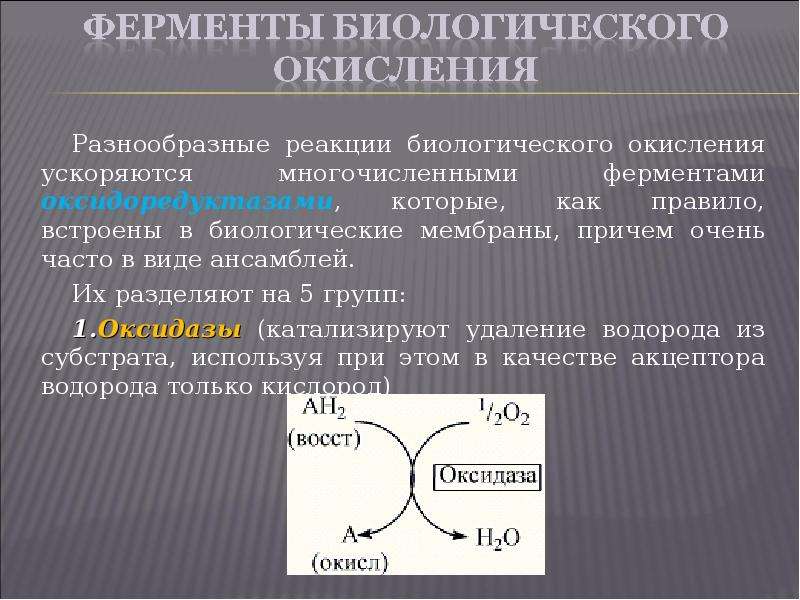

Содержание слайда: Разнообразные реакции биологического окисления ускоряются многочисленными ферментами оксидоредуктазами, которые, как правило, встроены в биологические мембраны, причем очень часто в виде ансамблей.
Разнообразные реакции биологического окисления ускоряются многочисленными ферментами оксидоредуктазами, которые, как правило, встроены в биологические мембраны, причем очень часто в виде ансамблей.
Их разделяют на 5 групп:
Оксидазы (катализируют удаление водорода из субстрата, используя при этом в качестве акцептора водорода только кислород)
№5 слайд
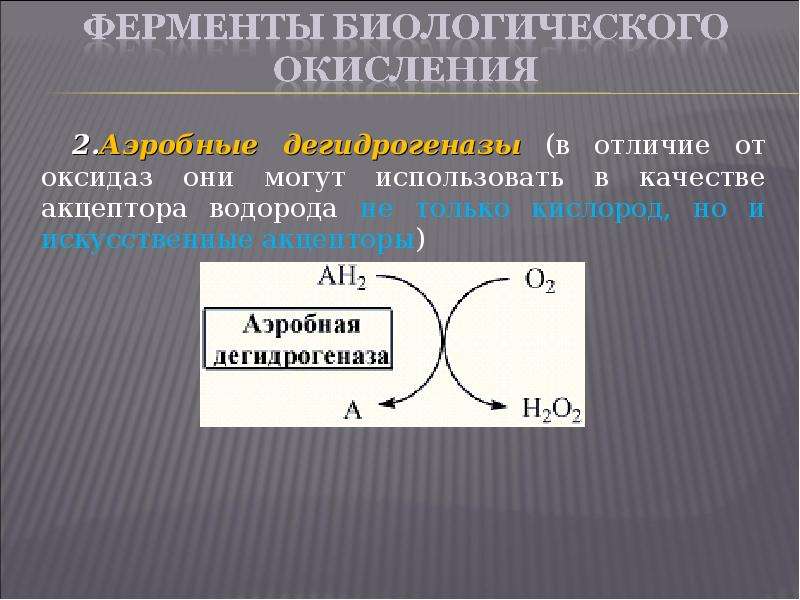

Содержание слайда: Аэробные дегидрогеназы (в отличие от оксидаз они могут использовать в качестве акцептора водорода не только кислород, но и искусственные акцепторы)
Аэробные дегидрогеназы (в отличие от оксидаз они могут использовать в качестве акцептора водорода не только кислород, но и искусственные акцепторы)
№6 слайд
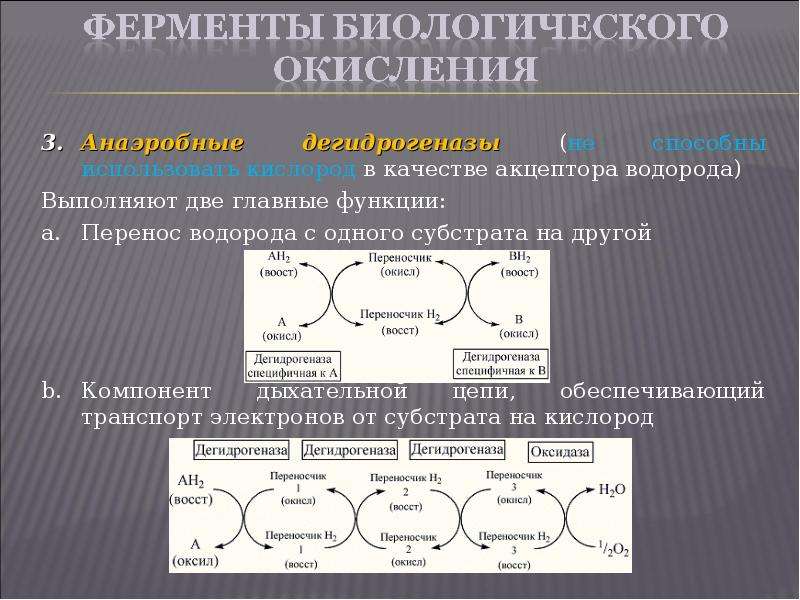

Содержание слайда: Анаэробные дегидрогеназы (не способны использовать кислород в качестве акцептора водорода)
Анаэробные дегидрогеназы (не способны использовать кислород в качестве акцептора водорода)
Выполняют две главные функции:
Перенос водорода с одного субстрата на другой
Компонент дыхательной цепи, обеспечивающий транспорт электронов от субстрата на кислород
№8 слайд


Содержание слайда: Существуют 2 типа биологического окисления:
Существуют 2 типа биологического окисления:
Свободное окисление
Окисление, не сопряженное с фосфорилированием АДФ и не сопровождающееся трансформацией энергии, выделяющейся при окислении, в энергию макроэргических связей.
При свободном окислении высвобождающаяся энергия переходит в тепловую и рассеивается.
Окисление, сопряженное с фосфорилированием АДФ
Этот тип биологического окисления осуществляется двумя путями:
субстратное фосфорилирование
окислительное фосфорилирование
№10 слайд


Содержание слайда: Реакции свободного окисления органических соединений в живой природе и ускоряющие их ферментные системы многообразны. Этим путем непосредственно окисляются не только многочисленные природные и неприродные субстраты, но и восстановленные коферменты (НАДН, НАДФН, ФАД·Н2 и др.), образовавшиеся при действии первичных и вторичных дегидрогеназ.
Реакции свободного окисления органических соединений в живой природе и ускоряющие их ферментные системы многообразны. Этим путем непосредственно окисляются не только многочисленные природные и неприродные субстраты, но и восстановленные коферменты (НАДН, НАДФН, ФАД·Н2 и др.), образовавшиеся при действии первичных и вторичных дегидрогеназ.
Реакции свободного окисления протекают в цитозоле, на мембранах различных субклеточных структур, в ядерном аппарате клетки. Основным средоточием их являются мембраны эндоплазматической сети (ЭПС).
Так как мембраны ЭПС при гомогенизации клеток и фракционировании субклеточных частиц гомогената дают фракцию микросом, то реакции окисления на мембранах ЭПС называются микросомальным окислением.
№11 слайд


Содержание слайда: 1) Несмотря на наличие ферментов цепи переноса электронов, ни в одном пункте этой цепи не происходит сопряжения с фосфорилированием АДФ.
1) Несмотря на наличие ферментов цепи переноса электронов, ни в одном пункте этой цепи не происходит сопряжения с фосфорилированием АДФ.
2) Своеобразие структуры и функциональной активности цитохромов b5 и Р–450, входящих в ее состав.
3) Высокое сродство терминальной оксидазы микросомальных цепей к кислороду, позволяющее ей конкурировать за кислород с митохондриальной цитохромоксидазой.
№13 слайд


Содержание слайда: Пирокатехаза (катехол: кислород-1,2-оксидоредуктаза дециклизующая)
Пирокатехаза (катехол: кислород-1,2-оксидоредуктаза дециклизующая)
Она содержит в активном центре два прочно связанных атома Fе, которые, согласно О. Хайаиши, соединяются с молекулярным кислородом в комплекс, где кислород далее активируется:
Fe2+ + О2 → Fе2+О2 → Fе3+О2–
№20 слайд


Содержание слайда: Субстратное фосфорилирование – такой вид биологического окисления, при котором:
Субстратное фосфорилирование – такой вид биологического окисления, при котором:
макроэргическая связь возникает в момент непосредственного окисления субстрата,
затем тем или иным путем передается на фосфатный остаток,
который, в свою очередь, используется для фосфорилирования АДФ, т.е. синтеза АТФ.
Окисление, сопряженное с фосфорилированием АДФ на уровне субстрата.
№21 слайд


Содержание слайда: При окислении 3-фосфоглицеринового альдегида (3-ФГА) в 2-фосфоглицериновую кислоту (2-ФГК) – гликолиз;
При окислении 3-фосфоглицеринового альдегида (3-ФГА) в 2-фосфоглицериновую кислоту (2-ФГК) – гликолиз;
При превращении фосфоенолпировиноградной кислоты (ФЕП) в пировиноградную (пируват, ПВК) – гликолиз;
При превращении -кетоглутаровой кислоты в янтарную (реакция цикла Кребса).
№27 слайд


Содержание слайда: Это сопряжение окисления с синтезом АТФ, когда атомы водорода с коферментов дегидрогеназ, принимающих участие в окислении субстратов, передаются в оксидоредуктазную цепь, где сопряжено с переносом ионов Н+ и электронов на молекулярный кислород происходит активирование неорганического фосфата и при его посредстве – фосфорилирование АДФ с образованием АТФ
Это сопряжение окисления с синтезом АТФ, когда атомы водорода с коферментов дегидрогеназ, принимающих участие в окислении субстратов, передаются в оксидоредуктазную цепь, где сопряжено с переносом ионов Н+ и электронов на молекулярный кислород происходит активирование неорганического фосфата и при его посредстве – фосфорилирование АДФ с образованием АТФ
Окисляемый субстрат в этом случае непосредственного участия в активировании неорганического фосфата не принимает
Сопряжение окисления с фосфорилированием идет главным образом на внутренних мембранах митохондрий
№30 слайд


Содержание слайда: Легкая обратимость.
Легкая обратимость.
Коферменты легко отделяются от белковой части, обладают высокой подвижностью, что позволяет им переносить атомы Н, ионы Н+ и электроны из одной части клетки в другую.
НАД и НАДФ способны принимать атомы Н от большого числа субстратов, окислительно-восстановительные потенциалы которых ниже (-0,32В).
№31 слайд


Содержание слайда: Коферменты – ФМН и ФАД.
Коферменты – ФМН и ФАД.
Флавиновые ферменты являются акцепторами атомов водорода и осуществляют перенос их от НАДН2:
НАДН2 + ФАД ⇄ НАД + ФАДН2.
В некоторых случаях (при окислении янтарной кислоты в цикле Кребса или при окислении жирных кислот) флавиновые ферменты могут играть роль первичных дегидрогеназ.
ФМН и ФАД очень прочно связаны с апоферментом и не отщепляются от него ни на одной стадии каталитического цикла.
Активной частью молекул ФАД и ФМН является изоаллоксазиновое кольцо рибофлавина, к атомам азота которого могут присоединяться 2 атома водорода:
№34 слайд


Содержание слайда: Дальнейший перенос электронов от КоQ на кислород осуществляет система цитохромов, состоящая из ряда гемопротеидов, расположенных в порядке возрастания окислительно-восстановительных потенциалов, что обеспечивает упорядоченную передачу электронов. Цитохромы а и а3 содержат в своем составе еще и атомы меди.
Дальнейший перенос электронов от КоQ на кислород осуществляет система цитохромов, состоящая из ряда гемопротеидов, расположенных в порядке возрастания окислительно-восстановительных потенциалов, что обеспечивает упорядоченную передачу электронов. Цитохромы а и а3 содержат в своем составе еще и атомы меди.
При транспорте электронов в направлении увеличения окислительно-восстановительных потенциалов происходят процессы:
Fe2+ ⇄ Fe3+ (в цит. b, c1, с)
Cu+ ⇄ Cu2+ (в цит. а, а3).
№36 слайд


Содержание слайда: Самой примечательной особенностью дыхательной цепи ферментов является наличие в ней участков, где соседние компоненты резко отличаются значениями окислительно-восстановительных потенциалов.
Самой примечательной особенностью дыхательной цепи ферментов является наличие в ней участков, где соседние компоненты резко отличаются значениями окислительно-восстановительных потенциалов.
Именно здесь происходит сопряжение окисления с фосфорилированием АДФ, т.к. разность энергетических уровней электрона, транспортируемого с огромной скоростью, вполне достаточна для синтеза макроэргической связи и составляет 51 кДж для I, 36 кДж – для II и 80,7 кДж – для III точки сопряжения.
№37 слайд


Содержание слайда: Питер Митчелл, Владимир Петрович Скулачев
Питер Митчелл, Владимир Петрович Скулачев
Реакции, сопровождающиеся расходованием или образованием Н+, протекают на внутренней мембране митохондрий таким образом, что протоны переносятся с внутренней мембраны на внешнюю, т.е. перенос электронов сопровождается возникновением трансмембранного градиента концентрации ионов Н+ – совершением осмотической работы.
Этот градиент, создающий разность химических () и электрических () потенциалов, является источником энергии для протекания эндэргонического процесса образования АТФ.
АТФаза является ферментом, способным использовать градиент концентрации ионов Н+ для обращения процесса гидролиза АТФ.
Скачать все slide презентации На тему "Биологическое окисление" - скачать бесплатно презентации по Биологии одним архивом:
Похожие презентации
-
 На тему "Информационные технологии в биологических исследованиях" - скачать бесплатно презентации по Биологии
На тему "Информационные технологии в биологических исследованиях" - скачать бесплатно презентации по Биологии -
 На тему "Биологические особенности моллюсков" - скачать презентации по Биологии
На тему "Биологические особенности моллюсков" - скачать презентации по Биологии -
 На тему "Биологический бой" - скачать презентации по Биологии
На тему "Биологический бой" - скачать презентации по Биологии -
 На тему "Биологический аукцион «Простейшие»" - скачать презентации по Биологии
На тему "Биологический аукцион «Простейшие»" - скачать презентации по Биологии -
 На тему "Биологические ритмы организма человека" - скачать презентации по Биологии
На тему "Биологические ритмы организма человека" - скачать презентации по Биологии -
 На тему "Обеспечение клеток энергией вследствие окисления органических веществ" - скачать презентации по Биолог
На тему "Обеспечение клеток энергией вследствие окисления органических веществ" - скачать презентации по Биолог -
 На тему "БИОЛОГИЧЕСКИЙ МОНИТОРИНГ" - скачать презентации по Биологии
На тему "БИОЛОГИЧЕСКИЙ МОНИТОРИНГ" - скачать презентации по Биологии -
 На тему "Свойства воды" - скачать бесплатно презентации по Биологии
На тему "Свойства воды" - скачать бесплатно презентации по Биологии -
 На тему "Мы и наш мир" по теме "Человек и природные сообщества" - скачать бесплатно презентации по Биологии
На тему "Мы и наш мир" по теме "Человек и природные сообщества" - скачать бесплатно презентации по Биологии -
 На тему "Планета рыб" - скачать бесплатно презентации по Биологии
На тему "Планета рыб" - скачать бесплатно презентации по Биологии