Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
15 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
74.63 kB
Просмотров:
60
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Лекция №11 по химии
Галогены
№2 слайд
Содержание слайда: План лекции
Строение атома
Возможные степени окисления
Способы получения галогенов
Водородные соединения галогенов
Хлорная вода
Хлорная известь
Кислородсодержащие кислоты галогенов и их соли
№3 слайд
Содержание слайда: Строение атома
ns2np5- внешний эл. слой
F 1s22s22p5
Cl 1s22s22p63s23p5
Br 1s22s22p63s23p63d104s24p5
I 1s22s22p63s23p63d104s24p64d105s25p5
Радиус атома увеличивается.
Max. валентность F = I
Max. валентность Cl, Br, I =VII
№4 слайд
Содержание слайда: Степень окисления
F : -1, 0
F2 - окислитель ( ядовит, не имеет цвета и запаха)
HF – плавиковая кислота => плавит стекло
NaF – фторид натрия
CaF2 – фторид кальция ( на зубной эмали)
№5 слайд
№6 слайд
Содержание слайда: Получение галогенов
Получение F2 - электролиз р-ра HF
2HF эл-з (KF) H2 + F2
№7 слайд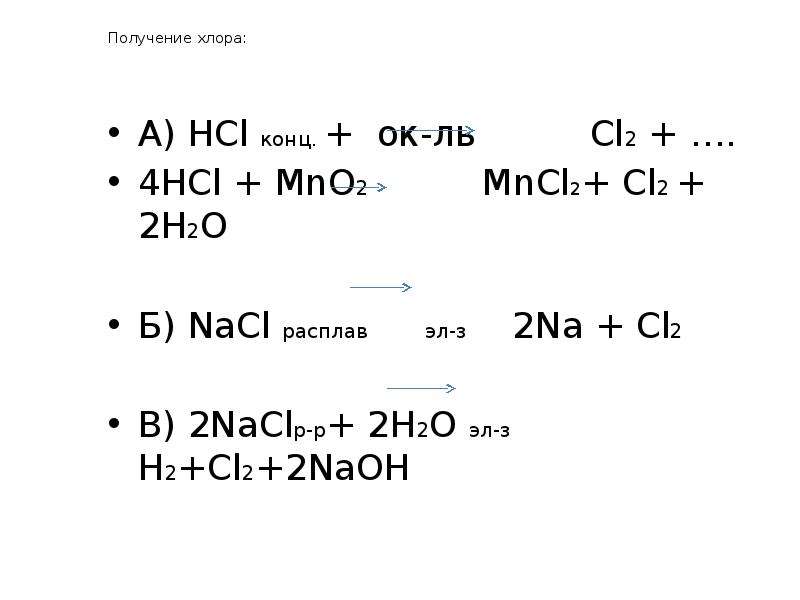
Содержание слайда: Получение хлора:
А) HCl конц. + ок-ль Cl2 + ….
4HCl + MnO2 MnCl2+ Cl2 + 2H2O
Б) NaCl расплав эл-з 2Na + Cl2
В) 2NaClр-р+ 2H2O эл-з H2+Cl2+2NaOH
№8 слайд
Содержание слайда: Получение брома и йода:
Br2 и I2 (из растворов солей)
2NaBr + Cl2 2NaCl + Br2
2NaI + Cl2 2NaCl + I2
№9 слайд
Содержание слайда: Галогеноводороды
Сравнение силы кислот
H F
H Cl сила кислот увелич.
H Br
H I
№10 слайд
Содержание слайда: Сравнение восстановительной силы галогенид -ионов
F +9))8e
Cl +17)))8e восст. способность увеличивается
Br +35 ))))8e
I +53))))) 8e
№11 слайд
Содержание слайда: Сравнение окислительной способности атомов галогенов
F +9))7e
Cl +17)))7e окислительная способность увеличивается
Br +35 ))))7e
I +53))))) 7e
№12 слайд
Содержание слайда: Хлорная вода
Получение:
Cl2 + H2O холод НCl + HСlO
Свойства :
HСlO свет НCl + [O ]
Атомарный кислород отбеливает и дезинфицирует.
№13 слайд
Содержание слайда: Хлорная известь
Получение:
Cl2 + Са(ОН)2тв. холод СаCl 2 + Са(СlO)2 +
Свойства :
Са(СlO)2 + С О2 + H2O СаСO3 + 2HСlO
HСlO свет НCl + [O ]
Атомарный кислород отбеливает и дезинфицирует.
№14 слайд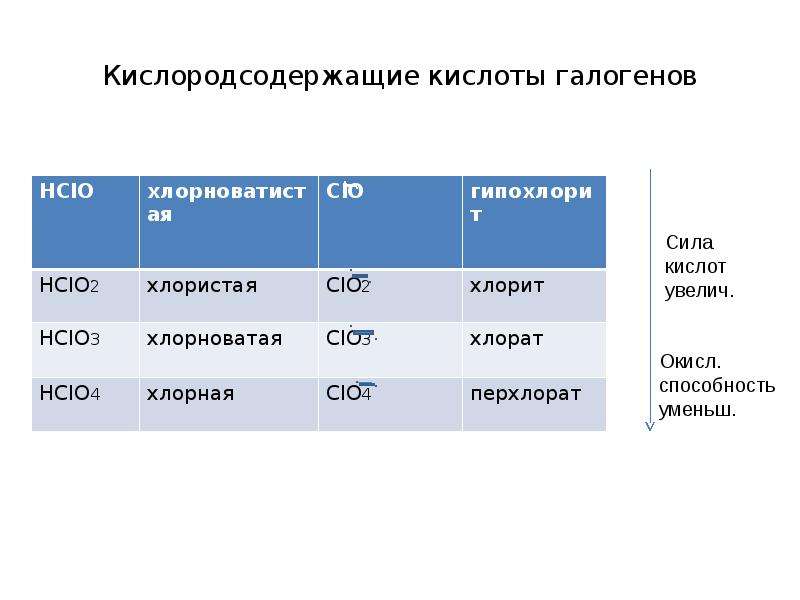
Содержание слайда: Кислородсодержащие кислоты галогенов
№15 слайд
Содержание слайда: Применение галогенов
NaF- сод. в зубных пастах
NaCl – пищевая пром., физ. раствор( 0,9%)
CaCl2 - средство от аллергии
KBr – успокоительное средство
I2 ( спирт. р-р) – дезинфицирующее средство
I2+ KI – (иодинол) - для полоскания горла
























