Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
8 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
128.00 kB
Просмотров:
82
Скачиваний:
2
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Горение и медленное окисление.
Тепловой эффект химической реакции.
№2 слайд
Содержание слайда: Проверь свои знания:
Кислород нельзя получить в результате реакции разложения:
1) воды; 2) бертолетовой соли;
3) перманганата калия ; 4)карбида кальция
2. Получение кислорода из воздуха основано:
1) на разнице температур кипения жидких азота и кислорода;
2) на способности кислорода поддерживать горение;
3) на разнице относительных молекулярных масс азота и кислорода;
4) на малой растворимости кислорода в воде.
3. Катализаторы – это вещества, которые
1) замедляют химическую реакцию;
2) участвуют в химической реакции с образованием сложных веществ ;
3) ускоряют химическую реакцию, но при этом не расходуются;
4) образуются в результате химической реакции
№3 слайд
Содержание слайда: 4.Кислород при обычных условиях:
1) твердое вещество, голубоватого цвета, без вкуса, без запаха;
2) кислород при обычных условиях взаимодействует с азотом;
3) бесцветный газ, без вкуса, без запаха;
4) твердые бесцветные кристаллы, сладковатого вкуса,
без запаха
5. Процесс горения – это
1)физическое явление; 2) химическая реакция, идущая с поглощением теплоты; 3) химическая реакция, идущая с выделением теплоты; 4) химическая реакция окисления, идущая с выделением тепла и света.
6. Вещество, являющееся оксидом, имеет химическую формулу:
1) CuS ; 2) Cu(OH)2 ; 3) CuO ; 4) CuCO3
7. В результате горения угля в кислороде образуется вещество, формула которого:
1) SO2 ; 2) CuO ; 3) CaCO3 ; 4) CO2
№4 слайд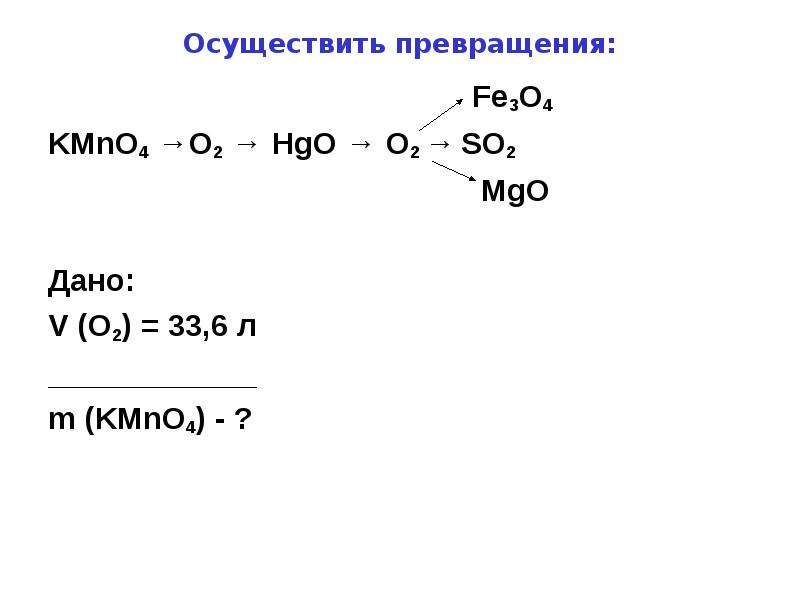
Содержание слайда: Осуществить превращения:
Fe3O4
KMnO4 →O2 → HgO → O2 → SO2
MgO
Дано:
V (O2) = 33,6 л
____________
m (KMnO4) - ?
№5 слайд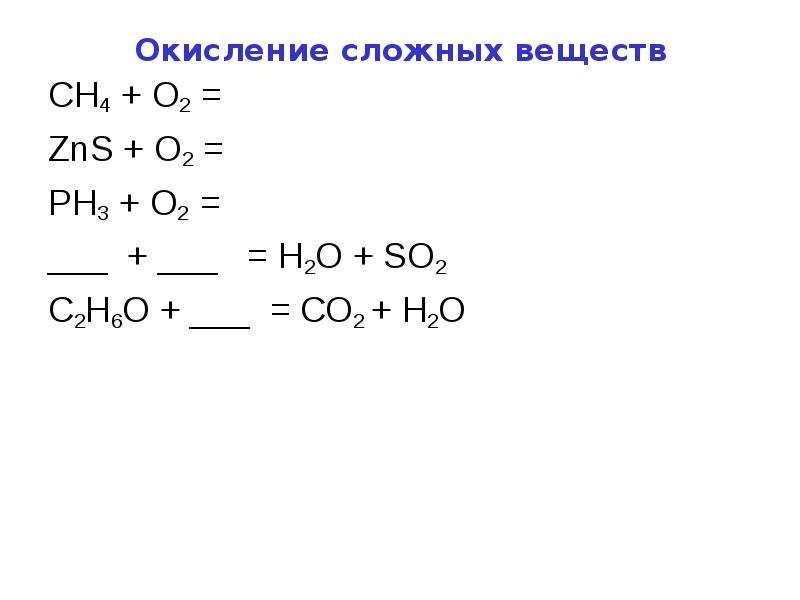
Содержание слайда: Окисление сложных веществ
СН4 + О2 =
ZnS + O2 =
PH3 + O2 =
___ + ___ = H2O + SO2
С2Н6О + ___ = СО2 + Н2О
№6 слайд
Содержание слайда: Реакции
Экзотермические Эндотермические
Реакции, протекающие с Реакции, протекающие с выделением энергии поглощением энергии
С + О2 = СО2 +402 кДж 2HgO = 2Hg + O2 -180 кДж
Q – количество теплоты, которое выделяется или поглощается при химической реакции –
тепловой эффект
№7 слайд
Содержание слайда: Приведите пример эндотермической реакции получения кислорода и вычислите сколько грамм этого вещества потребуется для получения 5,6л кислорода.
№8 слайд
Содержание слайда: На дом: §22,23, зад. 101 в раб тетради
Осуществить превращения:
KC lO3 → O2 → H2O → O2 + NH3 → ?