Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
65 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
6.94 MB
Просмотров:
76
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Общая характеристика элементов VIA-группы (халькогены).
Сера. Кислород
№2 слайд
Содержание слайда: Элементы VI группы главной подгруппы.
O Халькогены, т.е
S « рождающие руды».
Se
Te
Po
№3 слайд
Содержание слайда: Se и Te -минералов не образуют
Ро - очень редкий радиоактивный элемент
№4 слайд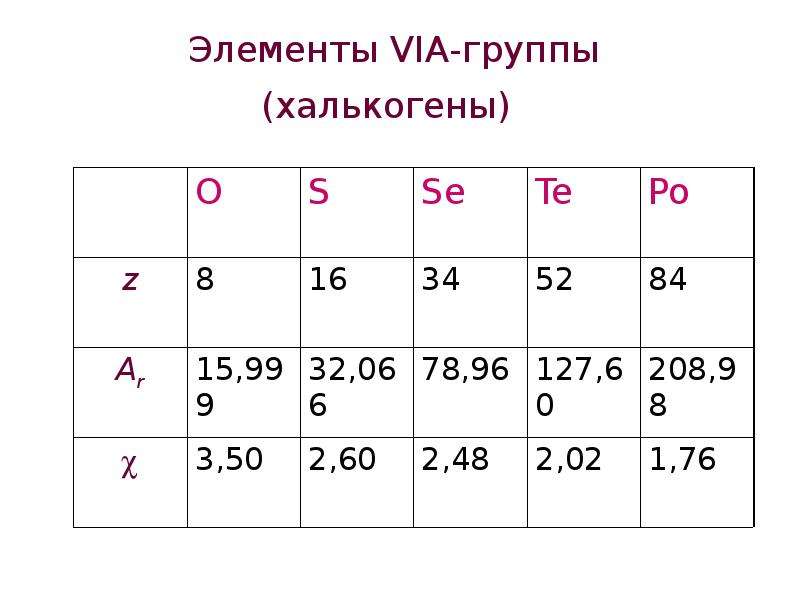
Содержание слайда: Элементы VIА-группы (халькогены)
№5 слайд
Содержание слайда: Кислород
№6 слайд
Содержание слайда: Кислород
Кислород – самый распространенный элемент на Земле (49,5% масс.).
Кислород существует в самородном виде (воздух) и входит в состав воды, горных пород и живых организмов.
В атмосфере содержание кислорода – 23,13% масс..
№7 слайд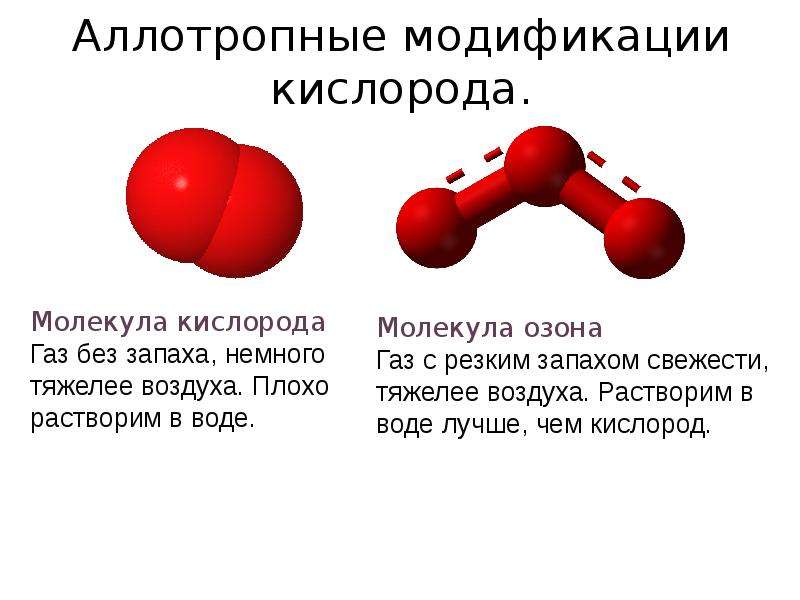
Содержание слайда: Аллотропные модификации кислорода.
№8 слайд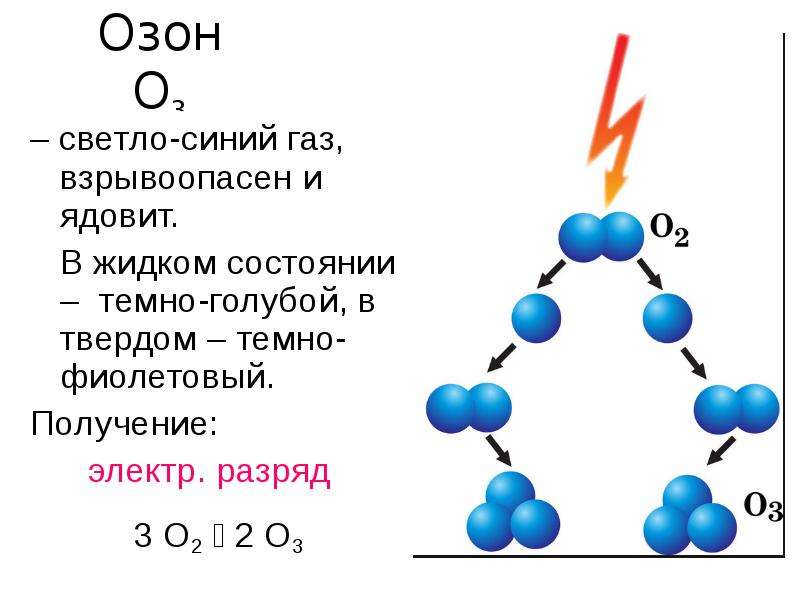
Содержание слайда: Озон O3
– светло-синий газ, взрывоопасен и ядовит.
В жидком состоянии – темно-голубой, в твердом – темно-фиолетовый.
Получение:
электр. разряд
3 O2 2 O3
№9 слайд
№10 слайд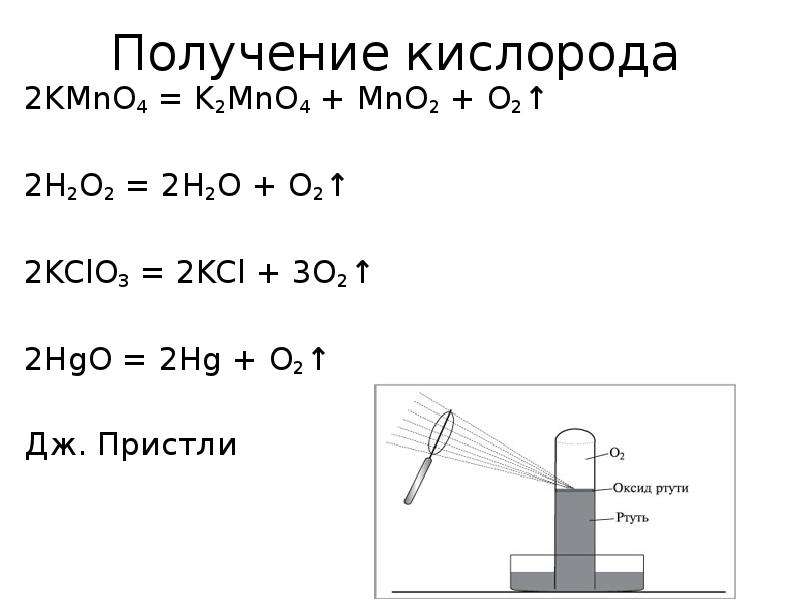
Содержание слайда: Получение кислорода
2KMnO4 = K2MnO4 + MnO2 + O2↑
2H2O2 = 2H2O + O2↑
2KClO3 = 2KCl + 3O2↑
2HgO = 2Hg + O2↑
Дж. Пристли
№11 слайд
Содержание слайда: Кислород активно взаимодействует со щелочными металлами даже без нагревания. Металлы средней и низкой активности реагируют с кислородом при нагревании.
Кислород активно взаимодействует со щелочными металлами даже без нагревания. Металлы средней и низкой активности реагируют с кислородом при нагревании.
4Li + O2 = 2Li2O
3Fe + 2O2 = Fe3O4
2Mg + O2 = 2MgO
№12 слайд
Содержание слайда: Реакция горения
При взаимодействии металлов и неметаллов с кислородом зачастую происходит выделение большого количества тепла и даже воспламенение.
S + O2 = SO2
4P + 5O2 = 2P2O5
№13 слайд
№14 слайд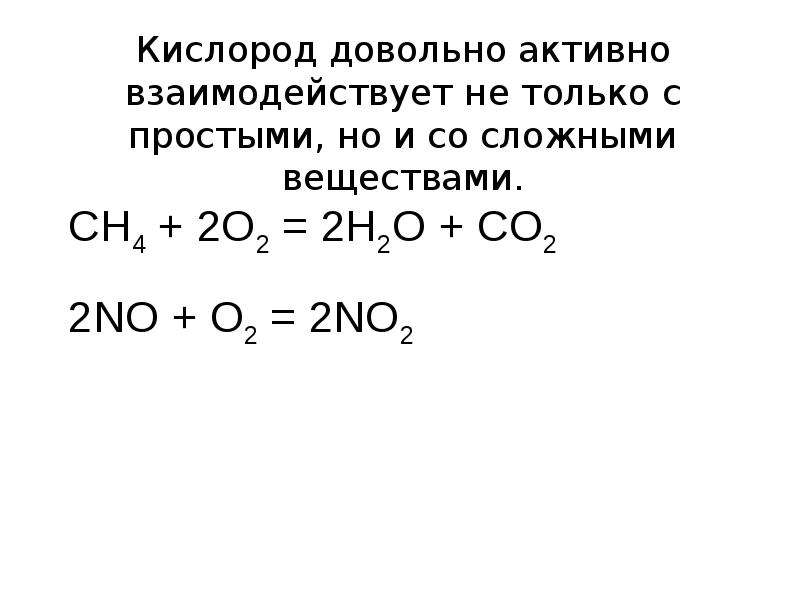
№15 слайд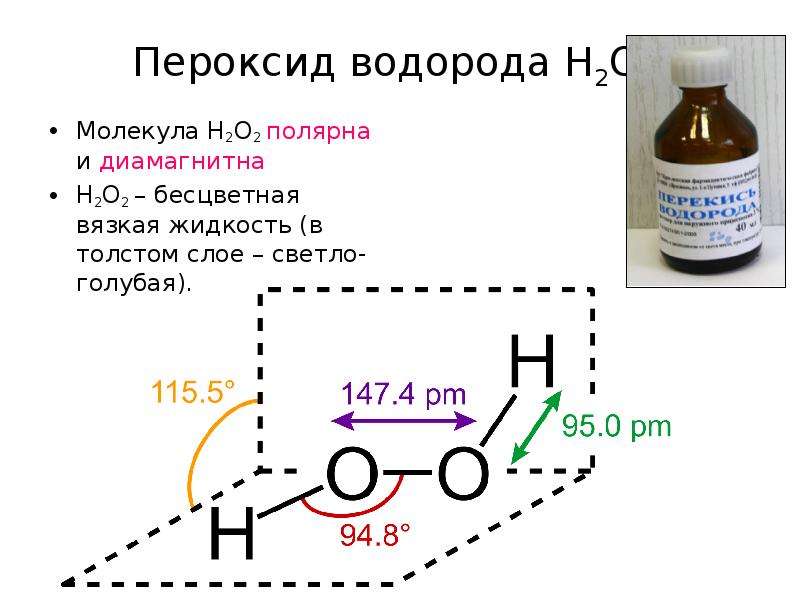
Содержание слайда: Пероксид водорода H2O2
Молекула H2O2 полярна и диамагнитна
H2O2 – бесцветная вязкая жидкость (в толстом слое – светло-голубая).
№16 слайд
Содержание слайда: Пероксид водорода H2O2
В разбавленных растворах пероксид водорода неустойчив и самопроизвольно диспропорционирует:
2H2O2–I = 2H2O–II + O20
№17 слайд
№18 слайд
№19 слайд
Содержание слайда: Сера- химический элемент
Сера - химический элемент ΙΙΙ( малого) периода,3 ряда, VΙ(А) группы
Атомный номер 16
Заряд ядра
Атомная масса 32,066
№20 слайд
Содержание слайда: Шкала степеней окисления серы
№21 слайд
№22 слайд
№23 слайд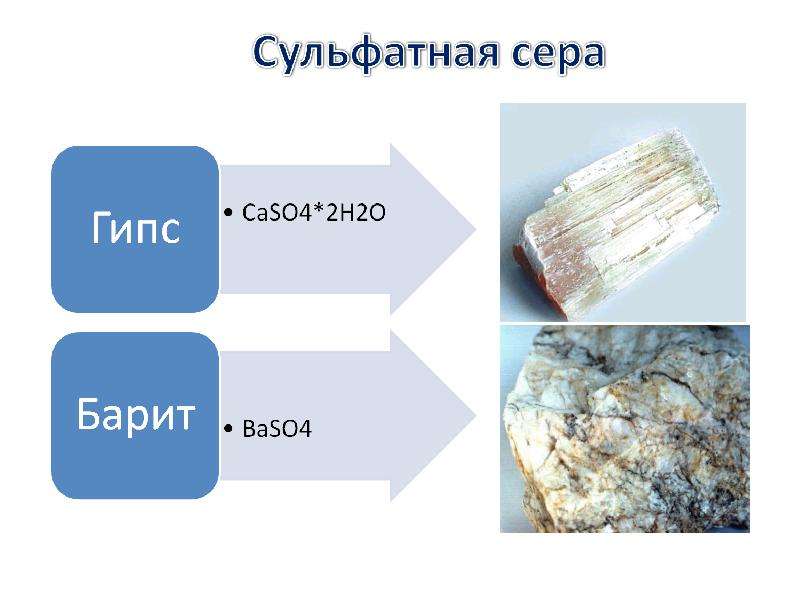
№24 слайд
№25 слайд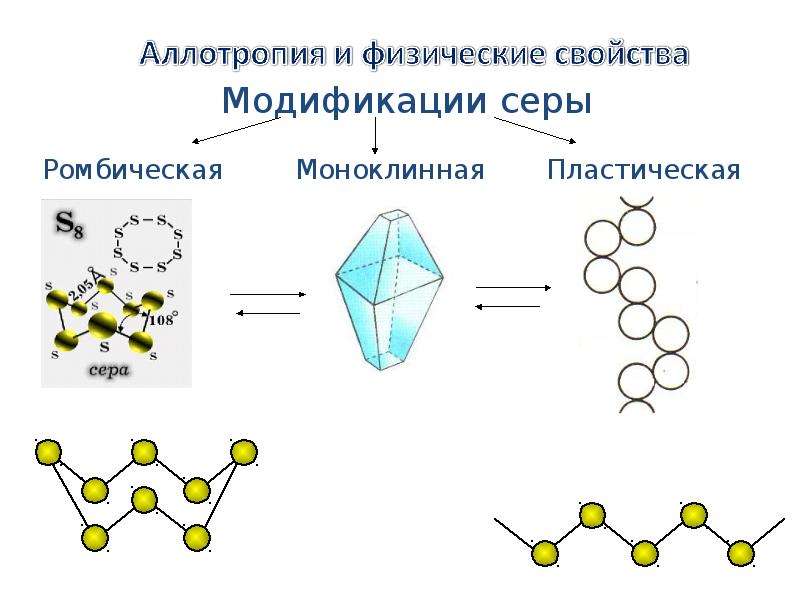
№26 слайд
№27 слайд
№28 слайд
№29 слайд
№30 слайд
№31 слайд
№32 слайд
№33 слайд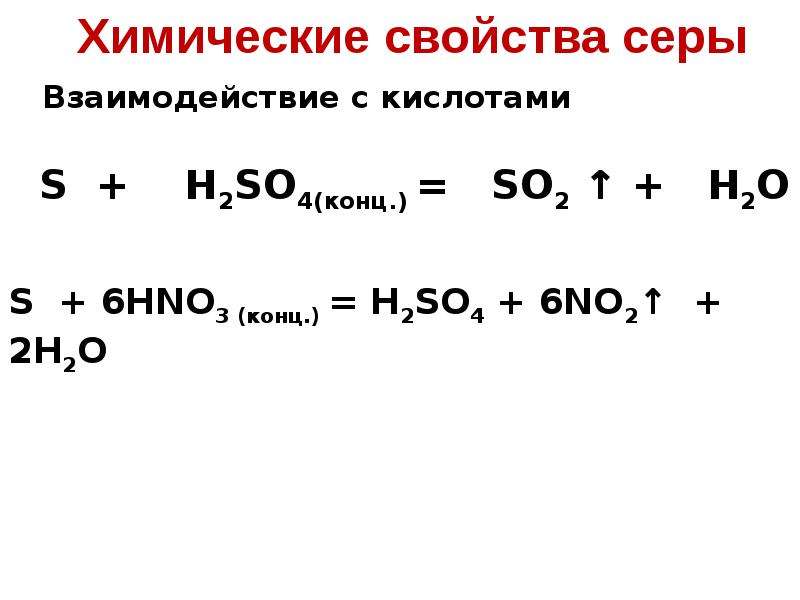
№34 слайд
№35 слайд
Содержание слайда: СЕРА
в организме человека
Сера входит в состав белков(волосы)
Сера- составная часть активных веществ:
витаминов и гормонов
При недостатке серы в организме наблюдаются хрупкость и ломкость костей, выпадение волос.
№36 слайд
Содержание слайда: Применение серы
№37 слайд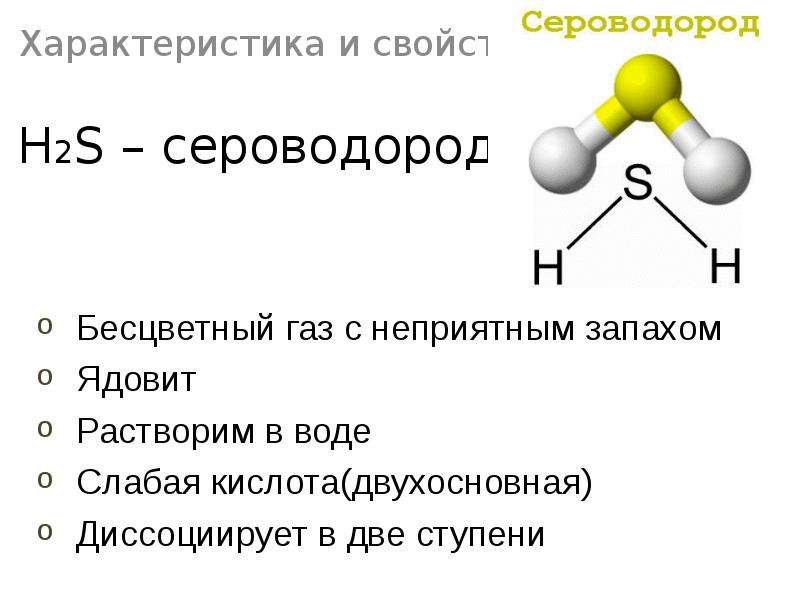
Содержание слайда: H2S – сероводород
Характеристика и свойства
№38 слайд
№39 слайд
Содержание слайда: Получение.
№40 слайд
Содержание слайда: Диссоциация.
№41 слайд
Содержание слайда: Химические свойства
№42 слайд
Содержание слайда: SO2 – сернистый газ
Характеристика и свойства
№43 слайд
Содержание слайда: Получение.
№44 слайд
Содержание слайда: Химические свойства
№45 слайд
Содержание слайда: SO3 – серный ангидрид
Характеристика и свойства
№46 слайд
Содержание слайда: Получение.
№47 слайд
Содержание слайда: Химические свойства
№48 слайд
Содержание слайда: Серная кислота в природе
Кислотное озеро на глубине вулкана Малый Семячик
№49 слайд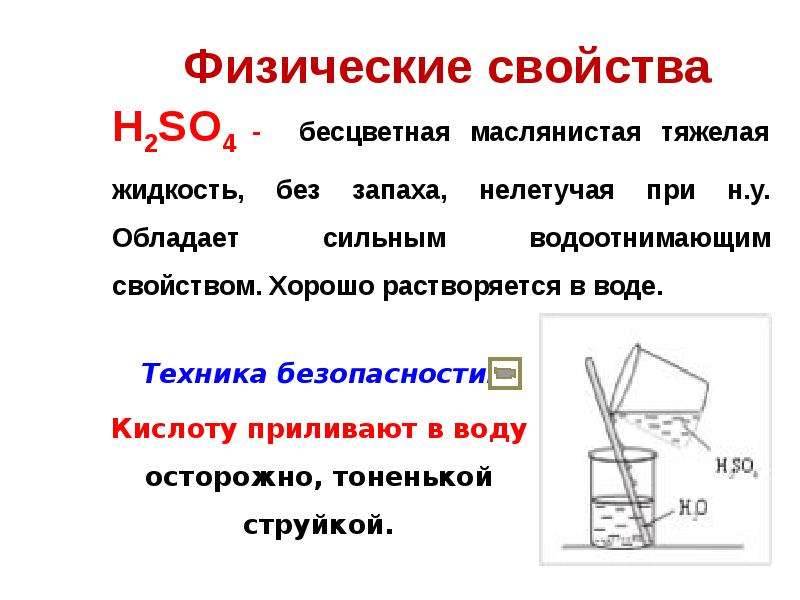
Содержание слайда: Физические свойства
H2SO4 - бесцветная маслянистая тяжелая жидкость, без запаха, нелетучая при н.у. Обладает сильным водоотнимающим свойством. Хорошо растворяется в воде.
№50 слайд
Содержание слайда: Разбавление серной кислоты
№51 слайд
Содержание слайда: Химические свойства
№52 слайд
Содержание слайда: Химические свойства разбавленной H2SO4
№53 слайд
Содержание слайда: Химические свойства разбавленной H2SO4
2. Взаимодействие с основными и амфотерными оксидами
H2SO4 + CuO = CuSO4 + H2O
№54 слайд
Содержание слайда: Химические свойства разбавленной H2SO4
3. Взаимодействие с основаниями:
а) щелочами
H2SO4 + 2NaOH = Na2SO4 + 2H2O
б) нерастворимыми основаниями
H2SO4 + Cu(OH)2 = CuSO4 + 2H2O
№55 слайд
Содержание слайда: Химические свойства разбавленной H2SO4
4. Взаимодействие с солями
H2SO4 + BaCl2 = BaSO4↓+ 2HCl
Качественная реакция – выпадение белого осадка
№56 слайд
Содержание слайда: Химические свойства концентрированной H2SO4
Концентрированная H2SO4 - сильный окислитель за счет S(+6)
1. Взаимодействие с металлами
№57 слайд
Содержание слайда: СВОЙСТВА СЕРНОЙ КИСЛОТЫ
https://www.youtube.com/watch?v=NbG1fq5MkAg
№58 слайд
Содержание слайда: Соли серной кислоты
№59 слайд
Содержание слайда: СПАСИБО ЗА ВНИМАНИЕ!
№60 слайд
Содержание слайда: Задание.
Определите степени окисления серы в соединениях :
SO2, H2S, SO3, CaS, Na2SO4, NaHS,
KHSO4, MgSO4, H2SO4, K2SO3.
№61 слайд
Содержание слайда: Тест
1. Концентрированная серная кислота при комнатной температуре не действует на каждое из двух веществ:
А) Mg, Cu; Б) Na, Zn; В) Ca, Li; Г) Fe, Al.
2. Разбавленная серная кислота реагирует с каждым из веществ:
А) Cu и KO H; Б) Na2CO3 и Al(OH)3
В) AlCl3 и Ag; Г) FeSO4 и H2SO4
3. При разбавлении серной кислоты всегда приливают кислоту к воде. Чем опасно разбавление концентрированной серной кислоты приливанием к ней воды?:
А) Может возникнуть пожар;
Б) Может произойти разложение воды;
В) Может выделиться ядовитое вещество;
Г) Может произойти разбрызгивание раствора вследствие выделения теплоты.
4. Водный раствор серной кислоты реагирует с каждым из веществ:
А) С цинком и оксидом натрия;
Б) С железом и оксидом углерода (II);
В) С алюминием и хлоридом натрия;
Г) С медью и гидроксидом калия.
№62 слайд
Содержание слайда: Тест
(ответы)
1 – Г
2 – Б
3 – Г
4 – А
№63 слайд
№64 слайд
№65 слайд










































































