Презентация ОЧКАСОВ ЕВГЕНИЙ МИХАЙЛОВИЧ ПРЕПОДАВАТЕЛЬ ХИМИИ И БИОЛОГИИ ГОСУДАРСТВЕННОГО АВТОНОМНОГО ОБРАЗОВАТЕЛЬНОГО УЧРЕЖДЕНИЯ СРЕДНЕГО онлайн
На нашем сайте вы можете скачать и просмотреть онлайн доклад-презентацию на тему ОЧКАСОВ ЕВГЕНИЙ МИХАЙЛОВИЧ ПРЕПОДАВАТЕЛЬ ХИМИИ И БИОЛОГИИ ГОСУДАРСТВЕННОГО АВТОНОМНОГО ОБРАЗОВАТЕЛЬНОГО УЧРЕЖДЕНИЯ СРЕДНЕГО абсолютно бесплатно. Урок-презентация на эту тему содержит всего 38 слайдов. Все материалы созданы в программе PowerPoint и имеют формат ppt или же pptx. Материалы и темы для презентаций взяты из открытых источников и загружены их авторами, за качество и достоверность информации в них администрация сайта не отвечает, все права принадлежат их создателям. Если вы нашли то, что искали, отблагодарите авторов - поделитесь ссылкой в социальных сетях, а наш сайт добавьте в закладки.
Презентации » Химия » ОЧКАСОВ ЕВГЕНИЙ МИХАЙЛОВИЧ ПРЕПОДАВАТЕЛЬ ХИМИИ И БИОЛОГИИ ГОСУДАРСТВЕННОГО АВТОНОМНОГО ОБРАЗОВАТЕЛЬНОГО УЧРЕЖДЕНИЯ СРЕДНЕГО
Оцените!
Оцените презентацию от 1 до 5 баллов!
- Тип файла:ppt / pptx (powerpoint)
- Всего слайдов:38 слайдов
- Для класса:1,2,3,4,5,6,7,8,9,10,11
- Размер файла:4.31 MB
- Просмотров:71
- Скачиваний:1
- Автор:неизвестен
Слайды и текст к этой презентации:
№1 слайд


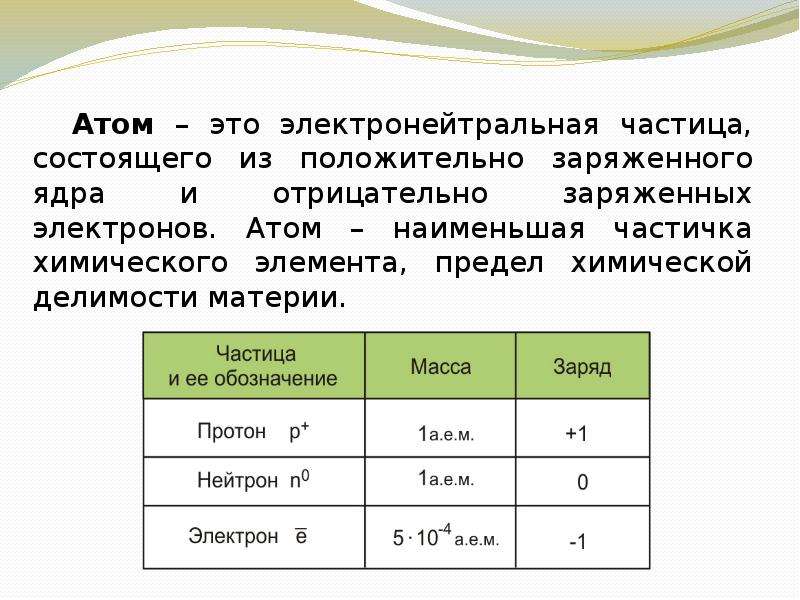
Содержание слайда: ОЧКАСОВ ЕВГЕНИЙ МИХАЙЛОВИЧ
ПРЕПОДАВАТЕЛЬ ХИМИИ И БИОЛОГИИ
ГОСУДАРСТВЕННОГО АВТОНОМНОГО ОБРАЗОВАТЕЛЬНОГО УЧРЕЖДЕНИЯ
СРЕДНЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
ДЕПАРТАМЕНТА ОБРАЗОВАНИЯ ГОРОДА МОСКВЫ
ПОЛИТЕХНИЧЕСКИЙ КОЛЛЕДЖ № 8
ИМЕНИ ДВАЖДЫ ГЕРОЯ СОВЕТСКОГО СОЮЗА И.Ф.ПАВЛОВА
(ГАОУ СПО ПК №8 ИМ. И.Ф.ПАВЛОВА)
№3 слайд


Содержание слайда: Содержание
Основные понятия химии…………………………………. 3
Состав веществ. Изменение веществ………………… 8
Основные законы химии......................................... 24
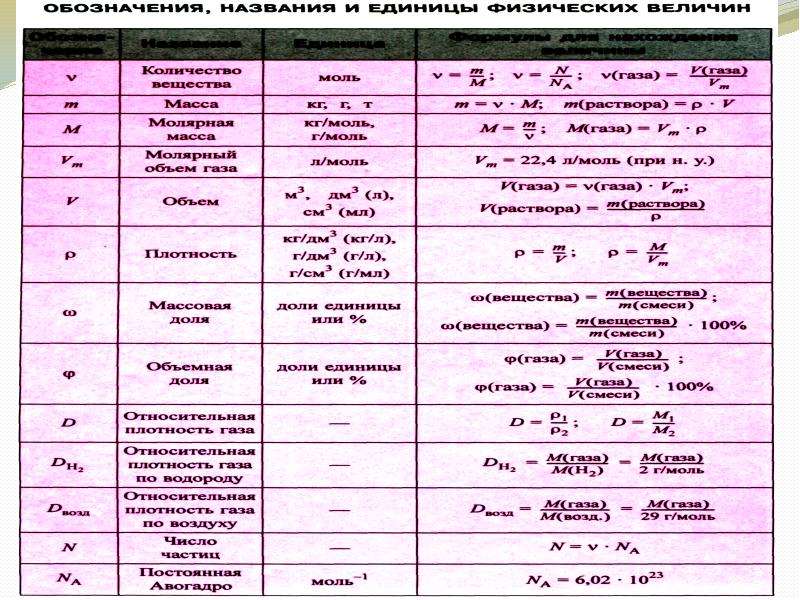
Обозначения, названия и единицы физической величины…………………………………………………………….. 34
Задания...................................................................... 35
№7 слайд


Содержание слайда: Молекула – это отдельная электронейтральная частица, образующаяся при возникновении ковалентных связей между атомами одного или нескольких элементов, которая определяет химические свойства вещества.
Молекула – это отдельная электронейтральная частица, образующаяся при возникновении ковалентных связей между атомами одного или нескольких элементов, которая определяет химические свойства вещества.
№8 слайд


Содержание слайда: Химический элемент – это совокупность атомов с одинаковым зарядом ядра.
Вещества, образованные одним химическим элементом, называют простыми. Один и тот же химический элемент может образовывать несколько простых веществ. Это явление называют аллотропией, а различные простые вещества, образованные одним элементом, - аллотропными видоизменениями, или аллотропными модификациями.
№10 слайд
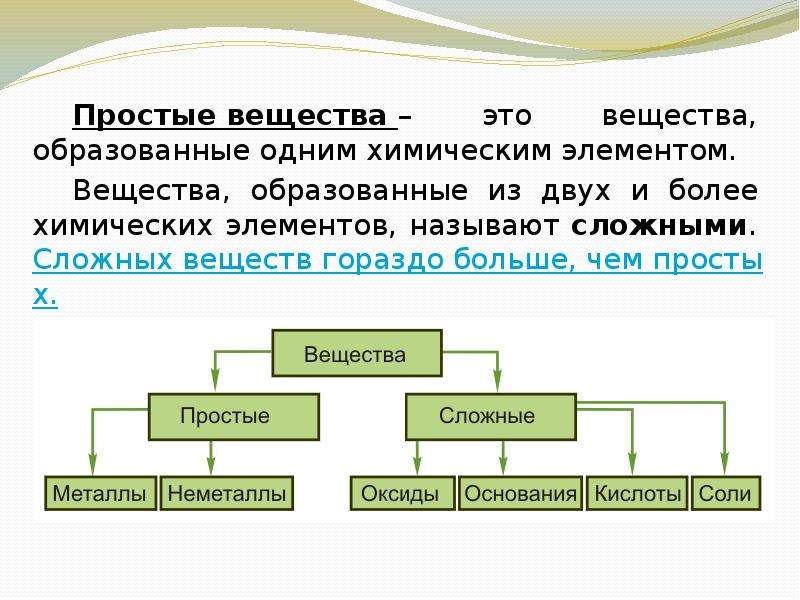

Содержание слайда: Простые вещества – это вещества, образованные одним химическим элементом.
Простые вещества – это вещества, образованные одним химическим элементом.
Вещества, образованные из двух и более химических элементов, называют сложными. Сложных веществ гораздо больше, чем простых.
№11 слайд


Содержание слайда: Различают в качественный и количественный состав веществ.
Качественный состав – это совокупность химических элементов и (или) атомных группировок, составляющих данное химическое вещество.
Количественный состав – это показатели, характеризующие количество или число атомов того или иного химического элемента и (или) атомных группировок, образующих данное химическое вещество.
№13 слайд


Содержание слайда: Химический знак (символ) – несет значительную информацию. Он обозначает название элемента, один его атом, один моль атомов этого элемента. По символу химического элемента можно определить его атомный номер и относительную атомную массу.
Химический знак (символ) – несет значительную информацию. Он обозначает название элемента, один его атом, один моль атомов этого элемента. По символу химического элемента можно определить его атомный номер и относительную атомную массу.
№14 слайд


Содержание слайда: Химическая формула – это способ отображения химического состава вещества. Она обозначает название вещества, одну молекулу его, один моль этого вещества. По химической формуле можно определить качественный состав вещества, число атомов и количество вещества каждого элемента в одном моле вещества, его относительную молекулярную и молярную массу.
Химическая формула – это способ отображения химического состава вещества. Она обозначает название вещества, одну молекулу его, один моль этого вещества. По химической формуле можно определить качественный состав вещества, число атомов и количество вещества каждого элемента в одном моле вещества, его относительную молекулярную и молярную массу.
Посмотреть видеоролик.
№15 слайд


Содержание слайда: Формулы вещества составляют на основании еще одного важнейшего понятия в химии – валентности.
Формулы вещества составляют на основании еще одного важнейшего понятия в химии – валентности.
Валентность – это способность атомов одного химического элемента соединятся со строго определенным числом атомов другого химического элемента.
№16 слайд


Содержание слайда: Широко используются несколько видов химических формул:
Широко используются несколько видов химических формул:
Простейшая (эмпирическая) формула показывает качественный состав и соотношения, в которых находятся частицы, образующие данное вещество.
Молекулярная (истинная) формула показывает качественный состав и число составляющих вещество частиц, но не показывает порядок связей частиц в веществе, т. е. его структуру.
Графическая формула отражает порядок соединения атомов, т. е. связи между ними.
Посмотреть видеоролик получения формулы по названию
№19 слайд
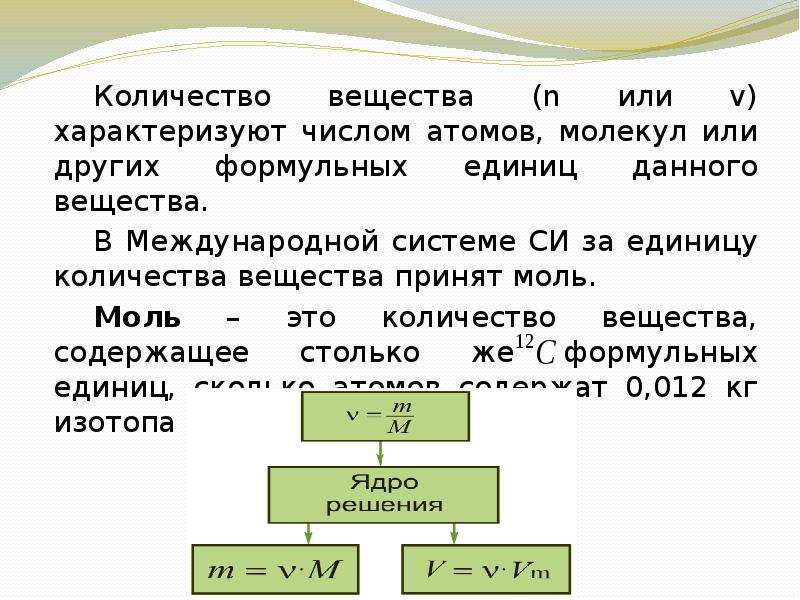

Содержание слайда: Количество вещества (n или v) характеризуют числом атомов, молекул или других формульных единиц данного вещества.
Количество вещества (n или v) характеризуют числом атомов, молекул или других формульных единиц данного вещества.
В Международной системе СИ за единицу количества вещества принят моль.
Моль – это количество вещества, содержащее столько же формульных единиц, сколько атомов содержат 0,012 кг изотопа углерода .
№23 слайд


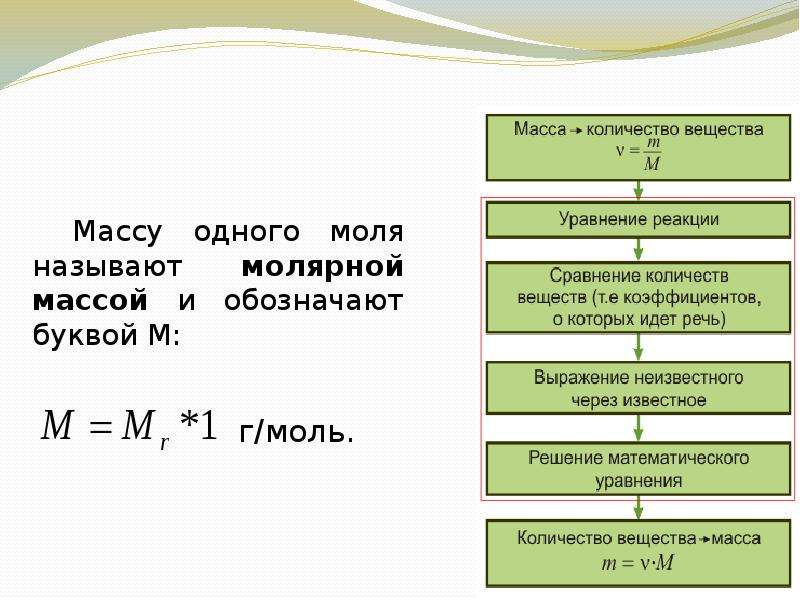
Содержание слайда: Молярная масса может быть выражена через число молекул (или атомов) в одном моле вещества ( ) и массу ( ) отдельной молекулы (или атома):
Молярная масса может быть выражена через число молекул (или атомов) в одном моле вещества ( ) и массу ( ) отдельной молекулы (или атома):
Массу молекулы (атома) в килограммах можно рассчитать по уравнению
следовательно
№24 слайд


Содержание слайда: Из этого выражения можно определить число молекул или атомов, содержащихся в одном месте любого вещества, которое называют постоянной Авогадро.
Из этого выражения можно определить число молекул или атомов, содержащихся в одном месте любого вещества, которое называют постоянной Авогадро.
Постоянная Авогадро ( ) – число атомов или молекул (или других формульных единиц), содержащихся в одном моле вещества; она всегда равна
№26 слайд


Содержание слайда: Закон сохранения массы.
Закон сохранения массы.
Был открыт М. В. Ломоносовым и сформулирован А. Лавуазье:
Масса веществ, вступивших в реакцию, равна массе веществ, образовавшихся в результате реакции.
Этот закон является одним из основных стехиометрических законов химии.
Посмотреть видеоролик.
№28 слайд


Содержание слайда: Закон постоянства состава вещества.
Сформулирован Ж.-Л. Прустом в 1799 г.:
Всякое чистое вещество независимо от способа его получения всегда имеет постоянный качественный и количественный состав.
Однако уже в начале XIX в. К. Бертолле показал, что элементы могут соединятся друг с другом в разных соотношениях в зависимости от массы реагирующих веществ.
№29 слайд


Содержание слайда: Современная формулировка закона постоянства состава вещества таков:
Состав соединений молекулярной структуры является постоянным независимо от способа их получения. Состав соединений немолекулярной структуры (с атомной, ионной или металлической кристаллической решеткой) не является постоянным и зависит от способа их получения.
№32 слайд


Содержание слайда: Из закона Авогадро вытекают 2 следствия:
Из закона Авогадро вытекают 2 следствия:
Один моль любого газа при одинаковых условиях занимает один и тот же объем. Этот объем, называемый молярным ( ), при нормальных условиях (давление = 101325 Па и абсолютной температуре = 273,15 К) равен 22,4 л:
№33 слайд


Содержание слайда: Массы двух разных газов, занимающих одинаковый объем при одинаковых условиях, относятся между собой как их молярные массы
Отношение масс двух газов, занимающих равный объем при одинаковых условиях, называют относительной плотностью одного газа по другому и обозначают буквой D.
№37 слайд


Содержание слайда: Сколько молекул содержится в 32 г сернистого газа
Сколько молекул содержится в 32 г сернистого газа
?
Какова масса молекул аммиака ?
Какова масса 5,6 (н. у.) углекислого газа? Сколько молекул содержится в этом объеме газа?
Каков объем 128 г сернистого газа при нормальных условиях? Сколько молекул содержится в 128 г этого газа?
Найдите массу кислорода, содержащегося в баллоне объемом 50 л при температуре и давлении 790 кПа.
№38 слайд


Содержание слайда: Список использованной литературы
Габриелян О.С. Химия для профессий и специальностей технического профиля. Учебник - М. Академия, 2011.
Габриелян О.С. Химия: учеб. для студ. проф. учеб. заведений / О.С. Габриелян, И.Г. Остроумов. – М., 2009.
Габриелян О.С. Химия. 8-11 класс. Базовый уровень: учеб. для общеобразоват. учреждений. – М., 2006.
1с химия. Мультимедийное пособие
Тестер А.Баженова. http://edu-lider.ru/proverka-znanij-konstruktor-testov/
Скачать все slide презентации ОЧКАСОВ ЕВГЕНИЙ МИХАЙЛОВИЧ ПРЕПОДАВАТЕЛЬ ХИМИИ И БИОЛОГИИ ГОСУДАРСТВЕННОГО АВТОНОМНОГО ОБРАЗОВАТЕЛЬНОГО УЧРЕЖДЕНИЯ СРЕДНЕГО одним архивом:
Похожие презентации
-
 Использование дрожжей в пищевой промышленности Федеральное государственное образовательное учреждение среднего профессионал
Использование дрожжей в пищевой промышленности Федеральное государственное образовательное учреждение среднего профессионал -
 АЗОТ Дегтярева Марина Олеговна учитель химии Автономное общеобразовательное учреждение Лицей научно-инженерного профи
АЗОТ Дегтярева Марина Олеговна учитель химии Автономное общеобразовательное учреждение Лицей научно-инженерного профи -
 Федеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования Томский
Федеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования Томский -
 Муниципальное образовательное учреждение «Лицей 3» Научно-исследовательская работа по химии «Получение ароматических масел»
Муниципальное образовательное учреждение «Лицей 3» Научно-исследовательская работа по химии «Получение ароматических масел» -
 Негосударственное образовательное учреждение частная школа «Радуга» Исследование чипсов Выполнил Ученик 10класса Борзов Ден
Негосударственное образовательное учреждение частная школа «Радуга» Исследование чипсов Выполнил Ученик 10класса Борзов Ден -
 Влияние химической завивки на волосы Муниципальное образовательное учреждение среднеобразовательная школа 1 работа Рожковой
Влияние химической завивки на волосы Муниципальное образовательное учреждение среднеобразовательная школа 1 работа Рожковой -
 Муниципальное общеобразовательное учреждение «Дмитриевская средняя общеобразовательная школа» Урок химии в 9 классе
Муниципальное общеобразовательное учреждение «Дмитриевская средняя общеобразовательная школа» Урок химии в 9 классе -
 Лектор Турло Евгений Михайлович Доцент кафедры химии, кандидат педагогических наук -410
Лектор Турло Евгений Михайлович Доцент кафедры химии, кандидат педагогических наук -410 -
 Калитина Тамара Михайловна учитель экологии, биологии МОУ СОШ 3 и учитель химии МОУ СОШ 2 с. Александров-Гай Саратовской области
Калитина Тамара Михайловна учитель экологии, биологии МОУ СОШ 3 и учитель химии МОУ СОШ 2 с. Александров-Гай Саратовской области -
 МЕТАЛЛЫ Подготовила: преподаватель химии и биологии Уалихановского сельскохозяйственного колледжа Сыздыкова Карлыгаш Казбеков
МЕТАЛЛЫ Подготовила: преподаватель химии и биологии Уалихановского сельскохозяйственного колледжа Сыздыкова Карлыгаш Казбеков