Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
20 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
794.88 kB
Просмотров:
104
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства.
№2 слайд
Содержание слайда: Цель урока:
1. на основе положения металлов в ПСХЭ прийти к пониманию особенностей строения их атомов и кристаллов (металлической химической связи и кристаллической металлической решетки).
2.Обобщить и расширить знания о физических свойствах металлов и их классификаций.
3. Развивать умение анализировать, делать выводы исходя из положения металлов в периодической системе химических элементов.
№3 слайд
№4 слайд
Содержание слайда: ЖЕЛЕЗО
№5 слайд
Содержание слайда: Металлы – это группа веществ с общими свойствами.
№6 слайд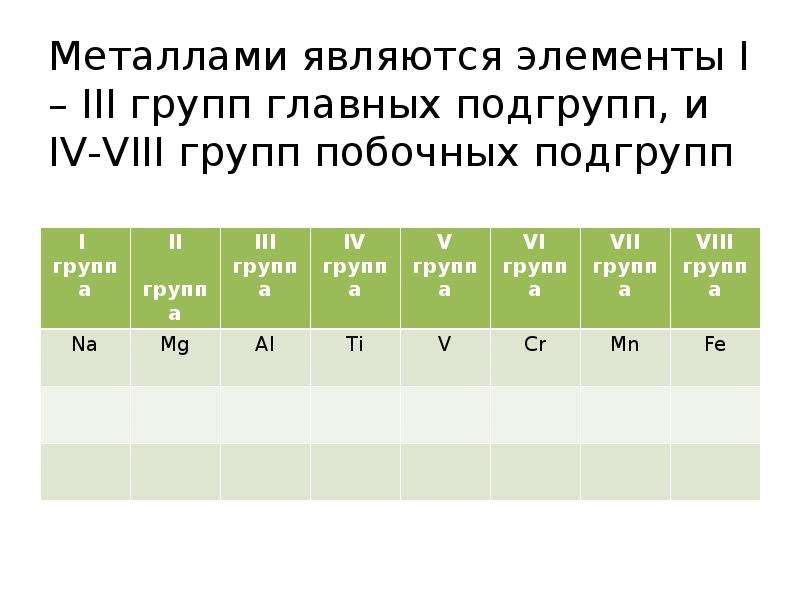
Содержание слайда: Металлами являются элементы I – III групп главных подгрупп, и IV-VIII групп побочных подгрупп
№7 слайд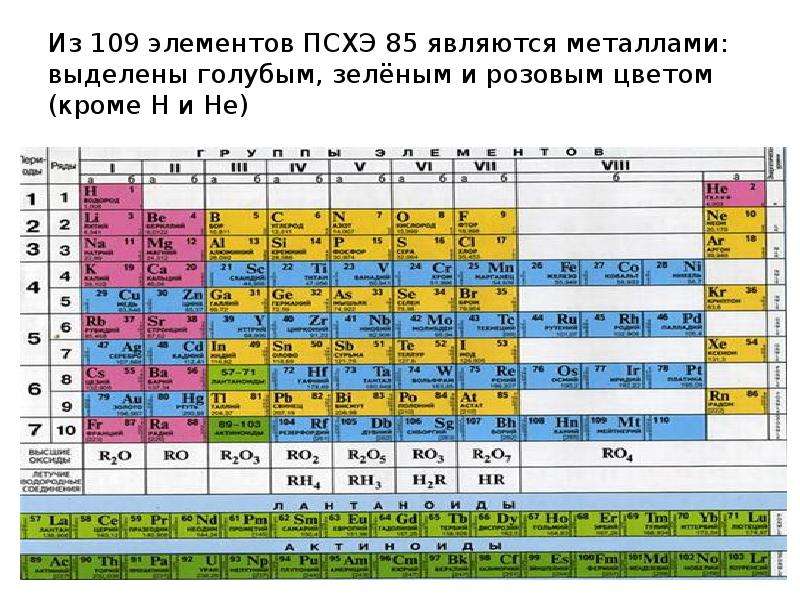
Содержание слайда: Из 109 элементов ПСХЭ 85 являются металлами: выделены голубым, зелёным и розовым цветом (кроме H и He)
№8 слайд
Содержание слайда: Положение элемента в ПС отражает строение его атомов
№9 слайд
Содержание слайда: Модель атома натрия
№10 слайд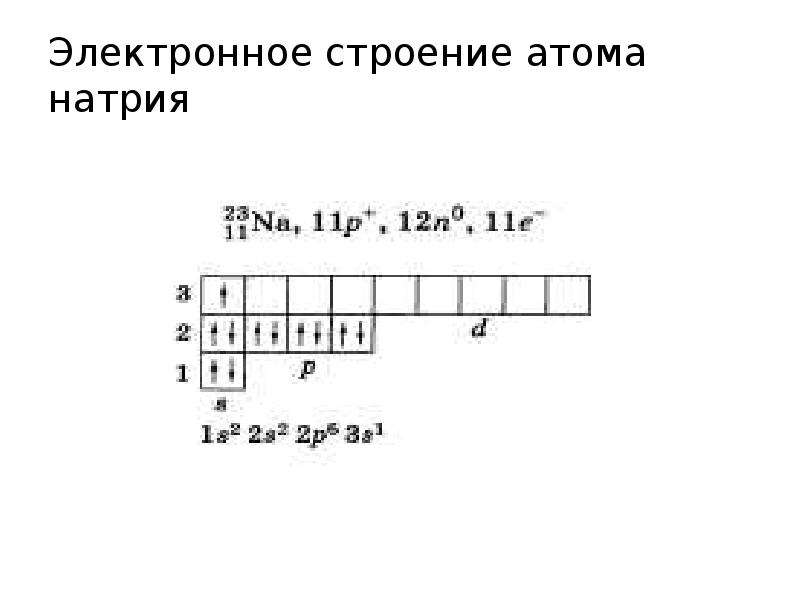
Содержание слайда: Электронное строение атома натрия
№11 слайд
Содержание слайда: Задание 2.
Составьте схему электронного строения атома алюминия и кальция в тетради самостоятельно по примеру с атомом натрия.
№12 слайд
Содержание слайда: Вывод:
1. Металлы– элементы, имеющие на внешнем энергетическом уровне 1-3 электрона, реже 4-6.
2. Металлы – это химические элементы атомы которых отдают электроны внешнего (а иногда предвнешнего) электронного слоя превращаясь в положительные ионы. Металлы – восстановители. Это обусловлено небольшим числом электронов внешнего слоя, большим радиусом атомов, вследствие чего эти электроны слабо удерживаются с ядром.
№13 слайд
Содержание слайда: Металлическая химическая связь характеризуется:
- делокализацией связи, т.к. сравнительно небольшое количество электронов одновременно связывают множество ядер;
- валентные электроны свободно перемещаются по всему куску металла, который в целом электронейтрален;
- металлическая связь не обладает направленностью и насыщенностью.
№14 слайд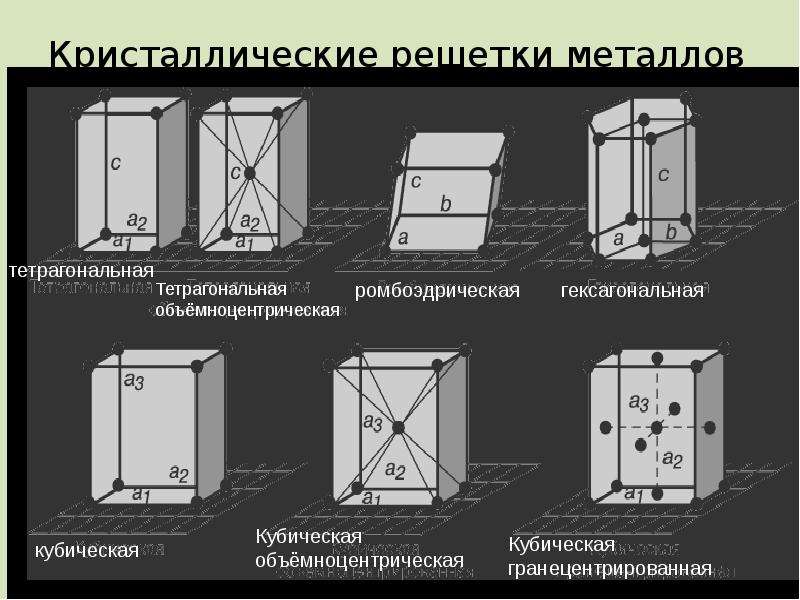
Содержание слайда: Кристаллические решетки металлов
№15 слайд
Содержание слайда: Видеоинформация о кристаллах металлов
№16 слайд
Содержание слайда: Свойства металлов определяются строением их атомов.
№17 слайд
Содержание слайда: Проверьте усвоение знаний на уроке тестированием
№18 слайд
Содержание слайда: Задания теста 2 и 3
№19 слайд
Содержание слайда: Задания теста 4 и 5
№20 слайд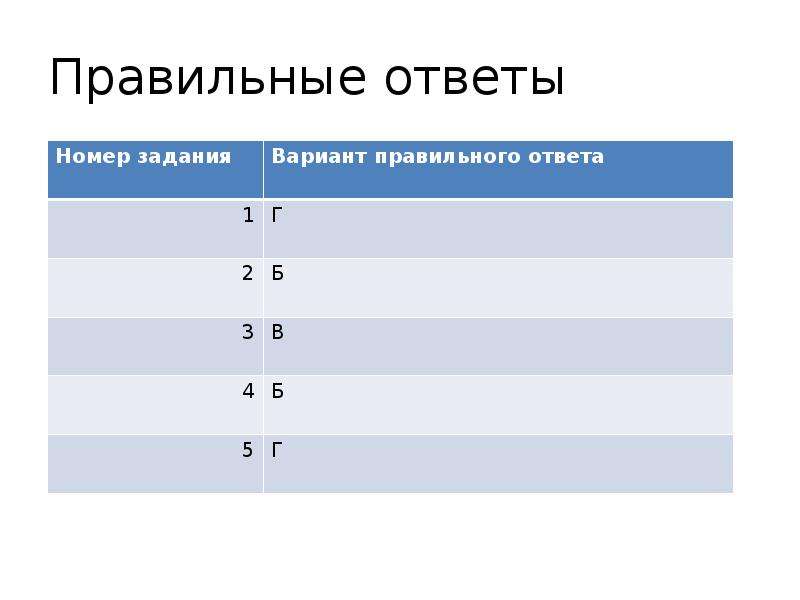
Содержание слайда: Правильные ответы





























