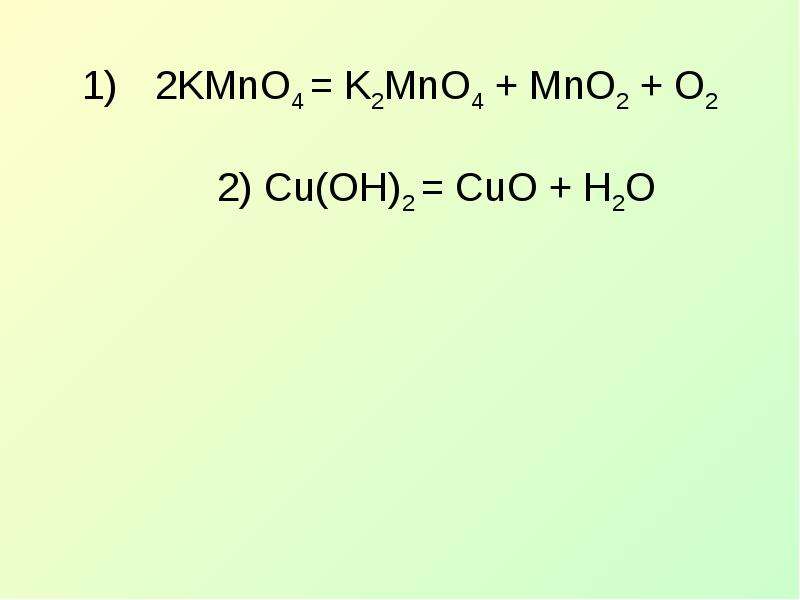Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
22 слайда
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
1.43 MB
Просмотров:
101
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
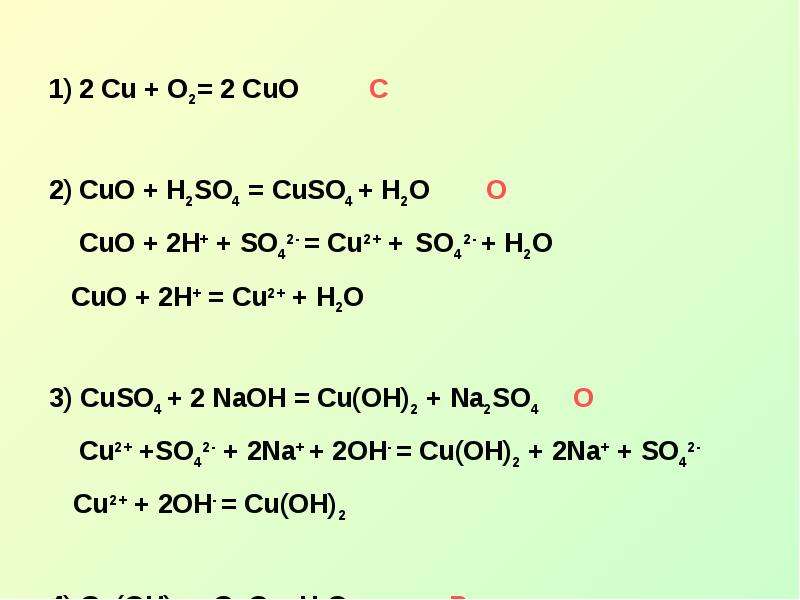
№1 слайд
№2 слайд
№3 слайд
Содержание слайда: Окислительно-восстановительные реакции (ОВР)
или
«Кто-то теряет, кто-то находит»
Задачи урока:
Познакомиться с понятиями: ОВР, окисление, восстановление, окислитель, восстановитель.
Научиться по уравнениям реакций распознавать ОВР, определять окислитель, восстановитель
№4 слайд
Содержание слайда: Входной контроль
1 вариант
1 - Г
2 - А
3 – Г
4 – А
5) А- 1
Б- 3
В- 3
Г- 4
№5 слайд
Содержание слайда: Лабораторная работа
А) Проведите химические реакции
Взаимодействия железа с сульфатом меди
Взаимодействия растворов сульфата меди и раствором щелочи.
Б) Запишите уравнения реакций в молекулярном и ионном виде. Укажите тип реакции
В) Укажите различия данных реакций.
№6 слайд
Содержание слайда: Fe0+Cu+2 SO4 = Fe SO4 + Сu
Fe0+Cu+2 SO4 = Fe SO4 + Сu
№7 слайд
Содержание слайда: Какие два процесса происходят в ОВР?
Fe0 + Cu+2SO4 = Cu0 + Fe+2SO4
№8 слайд
№9 слайд
№10 слайд
Содержание слайда: Уэ-1 Значение ОВР
№11 слайд
Содержание слайда: УЭ-2 Распознавание ОВР по химическим уравнениям
Окислительно-восстановительную реакцию можно определить по изменению степени окисления у отдельных элементов, по наличию простого вещества и по типу химической реакции.
1, 4
1вариант: Б,Г 2 вариант: А,В
№12 слайд
Содержание слайда: УЭ-3 Процессы окисления и восстановления.
1. А) окисление (ок-ие),восстановитель (в-ль)
Б) восстановление (в-ие), окислитель (ок-ль)
В) окисление (ок-ие),восстановитель (в-ль)
Г) восстановление (в-ие), окислитель (ок-ль)
2. 1) увеличивается 3) уменьшается
2) уменьшается 4) увеличивается
3. 1) Fe – 3е = Fe3+ - ок-ие, в-ль
2) C+4 + 2е =C+2 - в-ие, ок-ль
3) S+6 + 8е = S-2 - в-ие, ок-ль
4) P-3 – 3 =P0 - ок-ие, в-ль
№13 слайд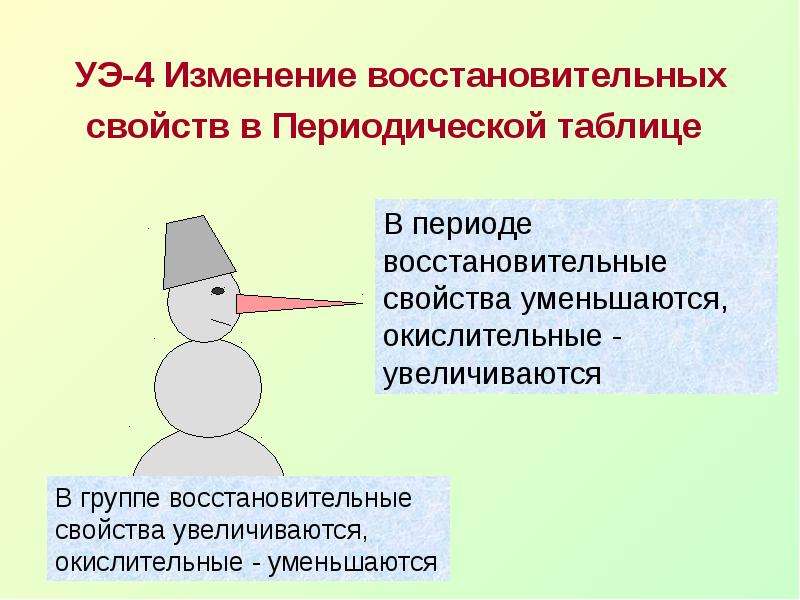
Содержание слайда: УЭ-4 Изменение восстановительных свойств в Периодической таблице
№14 слайд
Содержание слайда: УЭ-4 Изменение восстановительных свойств в Периодической таблице
2. а) Li, Na, K б) S, Si, Na
3) а) С, O, F б) Br, Cl, F
№15 слайд
Содержание слайда: Выходной контроль
1 - Б
2 - Б
3 - В
4 - А
5 - Б
№16 слайд
Содержание слайда: 1 Вариант
1 Вариант
С0 + О20 = С+4О2-2
C0 - 4e = C+4 - ок-ие, в-ль
O0 + 2e = O-2 - в-ие, ок-ль
2Fe2+3O3+3C0 =4Fe0 +3C+4O2
C0 - 4e = C+4- ок-ие, в-ль
Fe+3 +3e = Fe0-в-ие, ок-ль
№17 слайд
Содержание слайда: Домашнее задание
Стр. 229-231, выучить определения.
Стр.235. упр 1( «3»)
упр 1,3 («4»)
упр 1, 3, 5 ( «5»)
№18 слайд
Содержание слайда: Закончите схемы процессов, укажите окислитель и восстановитель:
Na …… = Na+
S-2 …… = S0
S-2 …… = S+6
№19 слайд
№20 слайд
№21 слайд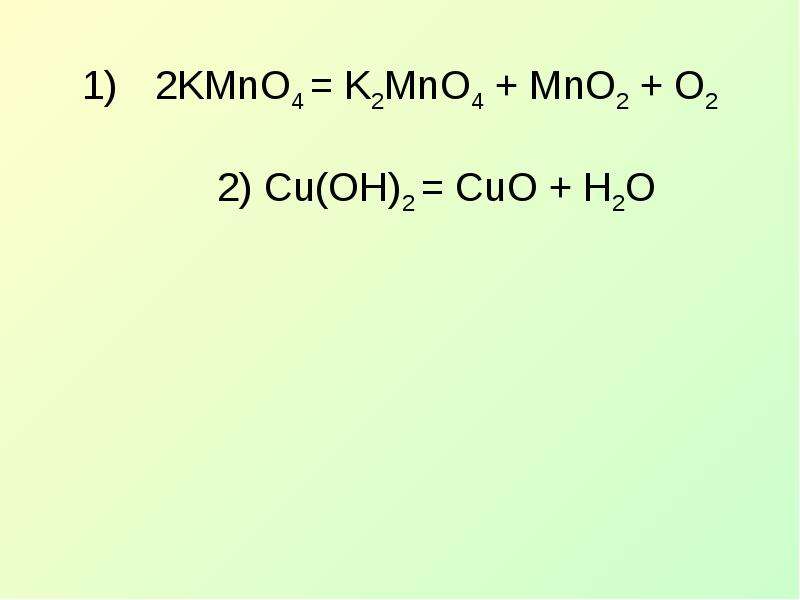
Содержание слайда: 2KMnO4 = K2MnO4 + MnO2 + O2
2) Cu(OH)2 = CuO + H2O
№22 слайд