Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
24 слайда
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
1.53 MB
Просмотров:
52
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Углеводороды
Выполнили
Филаткина Ирина, Филаткина Марина
ученица 11 класса
МОБУ СОШ № 7 ЛГО
№2 слайд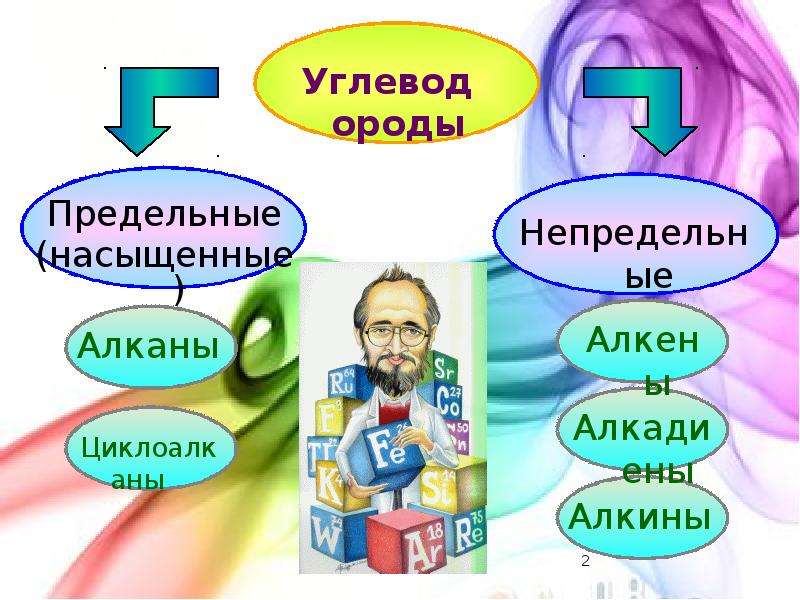
№3 слайд
Содержание слайда: Алканы (парафины)
К алканам (парафинам) относятся соединения с открытой цепью, в которых атомы углерода соединены друг с другом простыми (одинарными) связями, а остальные свободные их валентности насыщены атомами водорода. В обычных условиях алканы мало реакционноспособны, откуда возникло их название "парафины" – от лат. parrum affinis – малоактивный.
№4 слайд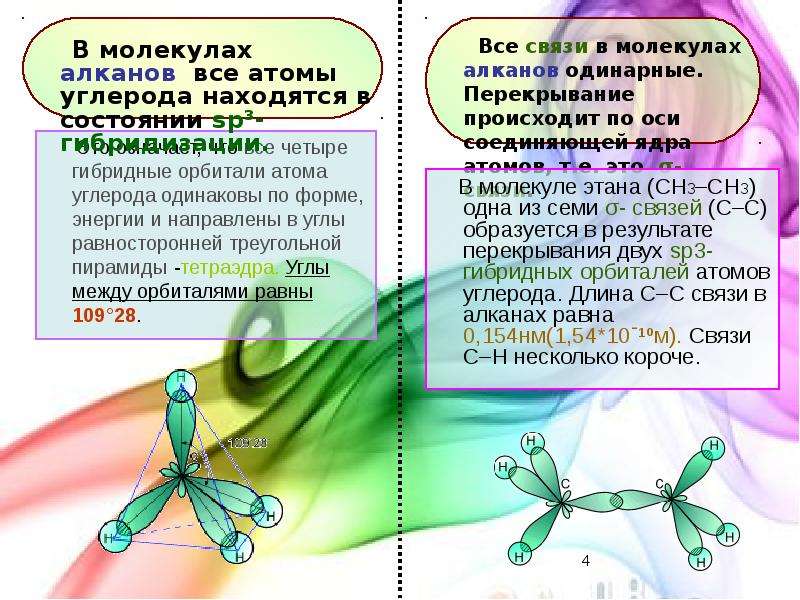
Содержание слайда: В молекуле этана (CH3–СH3) одна из семи σ- связей (С–С) образуется в результате перекрывания двух sp3- гибридных орбиталей атомов углерода. Длина С–С связи в алканах равна 0,154нм(1,54*10ˉ¹ºм). Связи С–Н несколько короче.
В молекуле этана (CH3–СH3) одна из семи σ- связей (С–С) образуется в результате перекрывания двух sp3- гибридных орбиталей атомов углерода. Длина С–С связи в алканах равна 0,154нм(1,54*10ˉ¹ºм). Связи С–Н несколько короче.
№5 слайд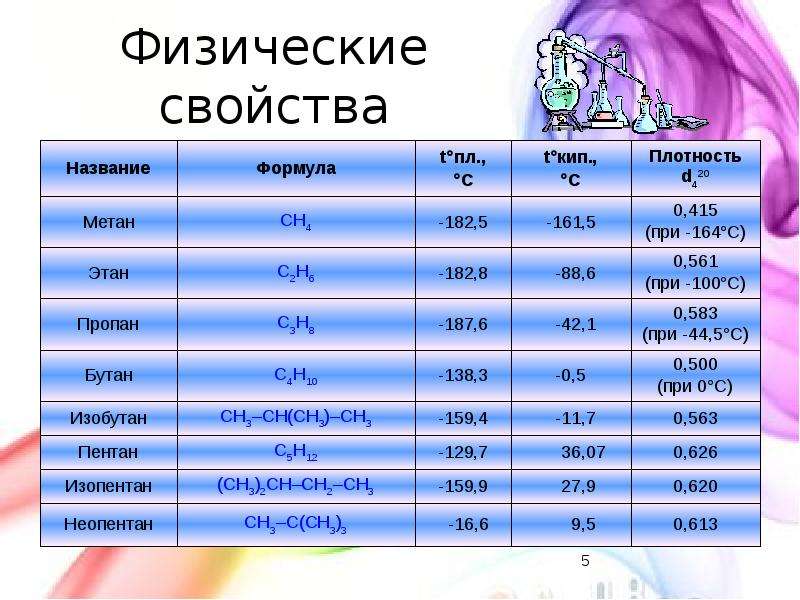
Содержание слайда: Физические свойства
№6 слайд
Содержание слайда: Химические свойства
№7 слайд
Содержание слайда: Применение
№8 слайд
Содержание слайда: Циклоалканы (циклопарафины)
№9 слайд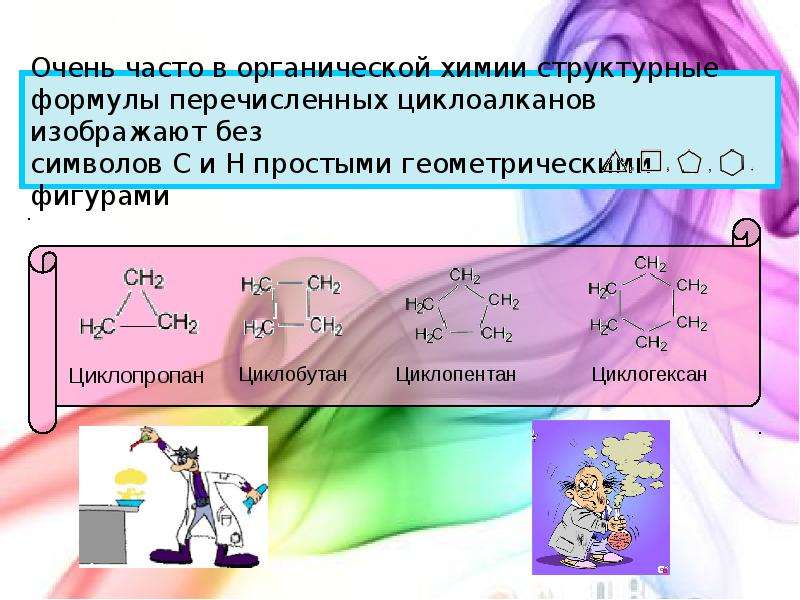
Содержание слайда: Очень часто в органической химии структурные формулы перечисленных циклоалканов изображают без
символов C и H простыми геометрическими фигурами
№10 слайд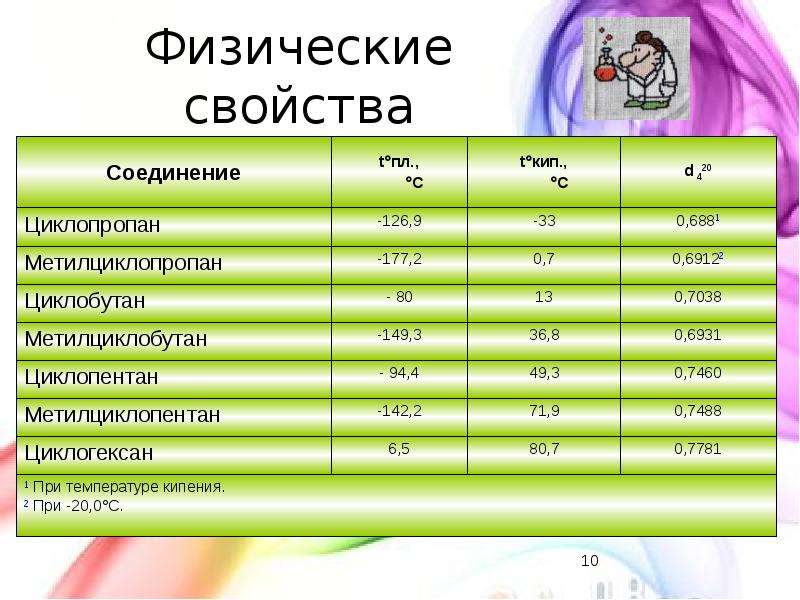
Содержание слайда: Физические свойства
№11 слайд
Содержание слайда: Химические свойства
Гидрирование:
Галогенирование:
Гидрогалогенирование:
Дегидрирование:
№12 слайд
Содержание слайда: Применение
Наибольшее практическое значение имеют циклогексан, этилциклогексан. Циклогексан используется для получения циклогексанола, циклогексанона, адипиновой кислоты, капролактама, а также в качестве растворителя. Циклопропан используется в медицинской практике в качестве ингаляционного анестезирующего средства.
№13 слайд
Содержание слайда: Алкены
Алкенами или олефинами, или этиленовыми углеводородами называются углеводороды, содержащие в молекуле одну двойную связь.
№14 слайд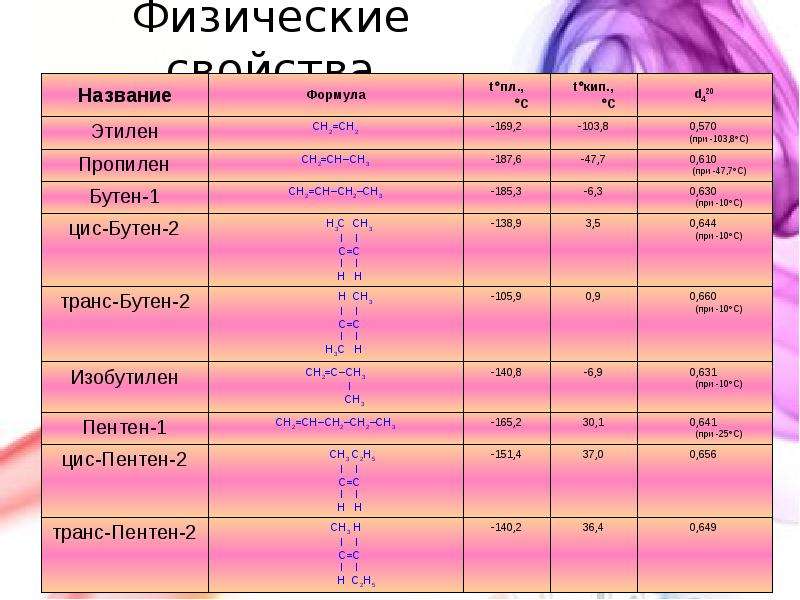
Содержание слайда: Физические свойства
№15 слайд
Содержание слайда: Химические свойства
Галогенирование: H2C=CH2 + Br2 → BrCH2–CH2Br (1,2-дибромэтан)
Гидрирование: CH3–CH=CH2 + H2 ––Ni→ CH3–CH2–CH3 (пропан)
Гидрогалогенирование: H2C=CH2 + HBr → CH3–CH2Br(бромистый этил)
Гидратация: СН2=СН2 + Н2О → СН3-СН2ОН (этанол)
Полимеризация п СН2 = СН2 → ( … - СН2 - СН2- …) п (полиэтилен)
Окисление 1. СН2=СН2 + 3 О2 → 2 СО2 + 2 Н2О
2. СН2 = СН2 + [ О ] + Н2О → СН2ОН – СН2ОН (этиленгликоль)
№16 слайд
Содержание слайда: Применение
Алкены широко используются в промышленности в качестве исходных веществ для получения растворителей (спирты, дихлорэтан, эфиры гликолей и пр.), полимеров (полиэтилен, поливинилхлорид, полиизобутилен и др.), а также многих других важнейших продуктов.
№17 слайд
Содержание слайда: Диеновые углеводороды (Алкадиены)
Диеновые углеводороды или алкадиены – это непредельные углеводороды, содержащие две двойные углерод - углеродные связи.
№18 слайд
Содержание слайда: 1) углеводороды с кумулированными двойными связями, т.е. примыкающими к одному атому углерода. Например, пропадиен или аллен CH2=C=CH2;
1) углеводороды с кумулированными двойными связями, т.е. примыкающими к одному атому углерода. Например, пропадиен или аллен CH2=C=CH2;
2) углеводороды с изолированными двойными связями, т.е разделенными двумя и более простыми связями. Например, пентадиен -1,4 CH2=CH–CH2–CH=CH2;
3) углеводороды с сопряженными двойными связями, т.е. разделенными одной простой связью. Например, бутадиен -1,3 или дивинил CH2=CH–CH=CH2, 2-метилбутадиен -1,3 или изопрен
CH2=С–CH=CH2.
I
CH3
№19 слайд
Содержание слайда: Физические свойства
Бутадиен -1,3 – легко сжижающийся газ с неприятным запахом, t°пл.= -108,9°C, t°кип.= -4,5°C; растворяется в эфире, бензоле, не растворяется в воде.
2- Метилбутадиен -1,3 – летучая жидкость, t°пл.= -146°C, t°кип.= 34,1°C; растворяется в большинстве углеводородных растворителях, эфире, спирте, не растворяется в воде.
№20 слайд
Содержание слайда: Алкины
Ацетиленовыми углеводородами (алкинами) называются непредельные (ненасыщенные) углеводороды, содержащие в молекуле одну тройную связь.
№21 слайд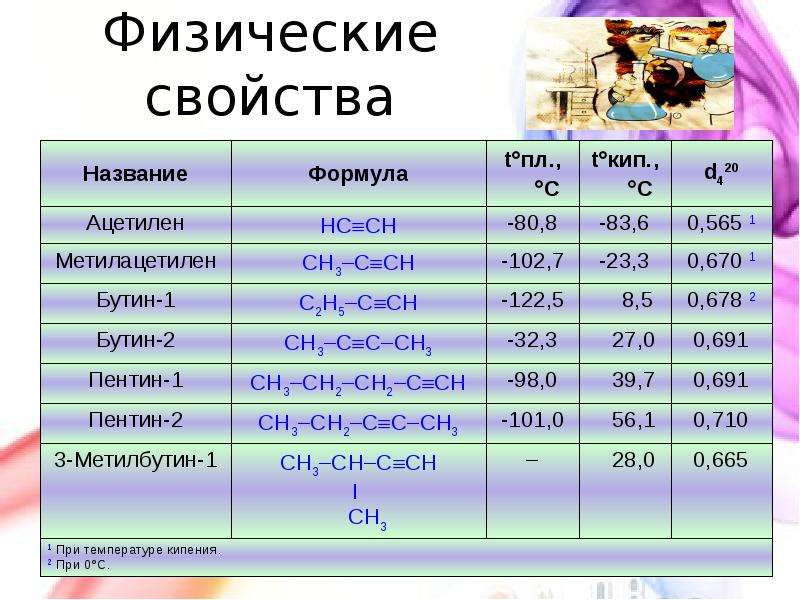
Содержание слайда: Физические свойства
№22 слайд
Содержание слайда: Химические свойства
Реакции присоединения:
Гидрирование:
Галогенирование:
Гидрогалогенирование:
Тримеризация : 3HC≡CH → С6 Н6 (бензол)
№23 слайд
Содержание слайда: Применение
При горении ацетилена в кислороде температура пламени достигает 3150°C, поэтому ацетилен используют для резки и сварки металлов. Кроме того, ацетилен широко используется в органическом синтезе разнообразных веществ - например, уксусной кислоты, 1,1,2,2- тетрахлорэтана и др. Он является одним из исходных веществ при производстве синтетических каучуков, поливинилхлорида и других полимеров.
№24 слайд

































