Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
36 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
1.96 MB
Просмотров:
120
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Соединения железа.
Цель: изучение соединений железа.
Задачи:
исследовать свойства
гидроксидов железа (II) и (III) ;
научиться распознавать ионы
Fe2+ и Fe3+.
№2 слайд
Содержание слайда: Соединения железа.
План урока.
1. Гидроксиды железа (II) и (III): получение и свойства. (Л/О).
2. Качественные реакции на ионы Fe2+ и Fe3+. (Л/О).
3. Значение соединений железа в природе и в жизни человека (сообщение).
4. Исследование продуктов питания на содержание в них железа. ( исследовательская работа).
5. Проверочный тест.
№3 слайд
Содержание слайда: Не в количестве знаний заключается образование, а в полном понимании и искусном применении всего того, что знаешь.
Дистервег.
№4 слайд
Содержание слайда: План урока.
1. Гидроксиды железа (II) и (III): получение и свойства. (Л/О).
№5 слайд
Содержание слайда: Эксперимент – основа познания.
Лабораторный опыт №1. Получение и изучение свойств гидроксидов железа (II) и (III).
Внимание! Соблюдайте правила по технике безопасности:
Во время проведения эксперимента не отвлекайтесь;
Все опыты проводите над лотком;
Берите необходимое количество веществ;
Не нюхайте и не пробуйте вещества на вкус;
С едкими веществами (кислотами и щелочами) работайте предельно осторожно;
Пузырьки с растворами веществ после использования обязательно закрывайте пробками;
По окончании работы приведите свое рабочее место в порядок.
№6 слайд
Содержание слайда: Вывод по лабораторному опыту:
Fe(OH)2 – основные свойства, взаимодействует с кислотами.
Fe(OH)3 - слабовыраженные амфотерные свойства ( с преобладанием основных), т.е. легко реагирует с кислотами, но трудно со щелочами.
Нерастворимое основание можно получить взаимодействием растворимой соли этого металла со щелочью.
№7 слайд
Содержание слайда: План урока.
2. Качественные реакции на ионы Fe2+ и Fe3+. (Л/О).
№8 слайд
Содержание слайда: «Нет искусства столь же трудного, как искусство наблюдения».
Лабораторный опыт №2. Качественные реакции на ионы Fe2+ и Fe3+.
Внимание! Соблюдайте правила по технике безопасности:
Во время проведения эксперимента не отвлекайтесь;
Все опыты проводите над лотком;
Берите необходимое количество веществ;
Не нюхайте и не пробуйте вещества на вкус;
С едкими веществами (кислотами, солями и щелочами) работайте предельно осторожно;
Пузырьки с растворами веществ после использования обязательно закрывайте пробками;
По окончании работы приведите свое рабочее место в порядок.
№9 слайд
Содержание слайда: Лабораторный опыт:
Качественные реакции на ионы Fe2+ и Fe3+.
FeSO4 + K3 [Fe(CN)6 ] KFe +2 [Fe +3(CN)6 ] + K2SO4
красная кровяная соль турнбулева синь
FeCI3 + K4 [Fe(CN)6 ] KFe+3 [Fe +2(CN)6 ] +3KCI
желтая кровяная соль берлинская лазурь
FeCI3 + 3 KCNS Fe(CNS )3 +3KCI
роданид калия кроваво-красный
Объясните опыт, который вы увидели в начале урока.
№10 слайд
№11 слайд
№12 слайд
№13 слайд
№14 слайд
№15 слайд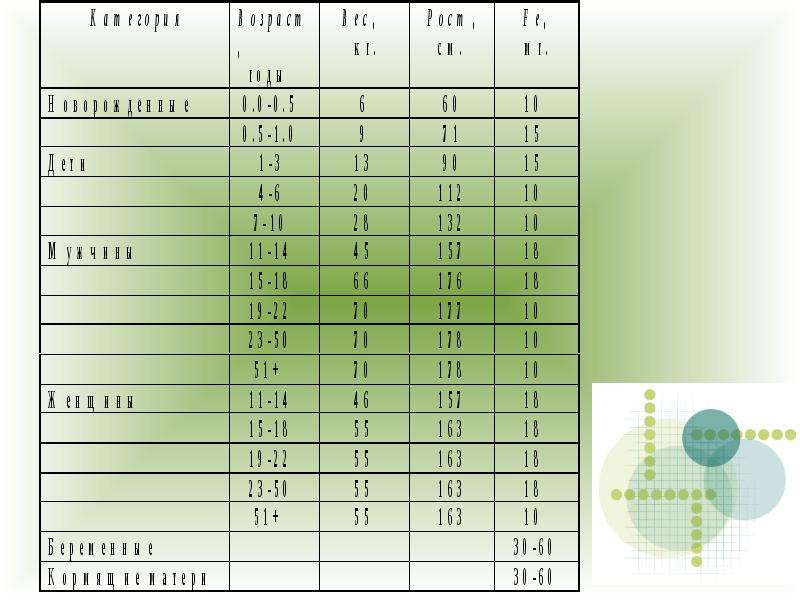
№16 слайд
№17 слайд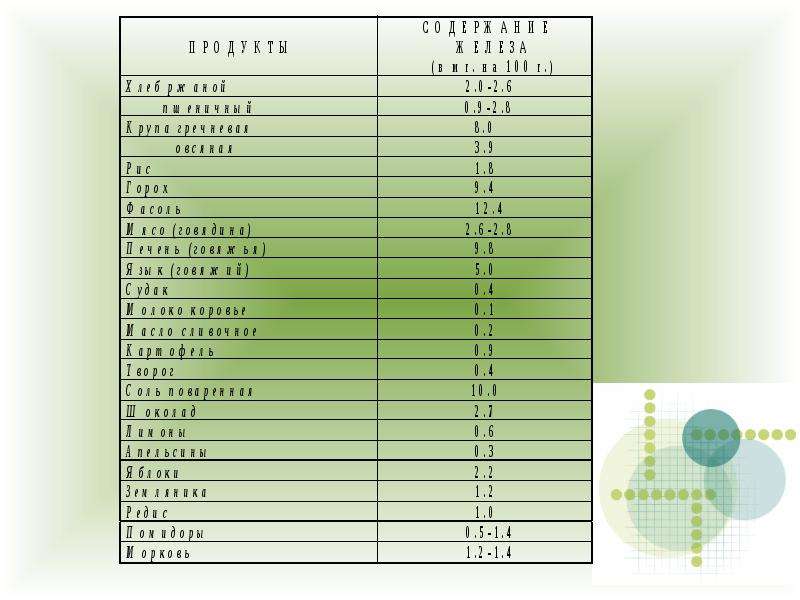
№18 слайд
№19 слайд
№20 слайд
Содержание слайда: План урока.
4. Исследование продуктов питания на содержание в них железа. ( исследовательская работа).
№21 слайд
Содержание слайда: Исследовательская работа.
Определение содержания железа в продуктах питания.
№22 слайд
Содержание слайда: Цель: Обнаружение ионов железа в продуктах питания.
№23 слайд
Содержание слайда: Оборудование: Реактивы:
Штатив
Пробирки
Весы
Горелка
Ступка и пестик
Колба
Воронка
№24 слайд
Содержание слайда: Исследуемые продукты питания:
1) Гречка
2) Пшено
3) Мука пшеничная
4) Ржаной хлеб
№25 слайд
Содержание слайда: Ход работы:
№26 слайд
Содержание слайда: Ход работы:
3. Измельчила золу до порошка.
4. Перенесла золу в пробирку и добавила 10мл HCI.
5 . Перемешав, добавила 5мл дистилированной воды.
№27 слайд
Содержание слайда: Ход работы:
6. собрала прибор для фильтрования.
7. профильтровала содержимое пробирок.
8. 5 мл каждого фильтрата перелила в пробирку.
№28 слайд
Содержание слайда: Ход работы:
9. К фильтратам
добавила раствор
роданида калия - KSCN.
10. Закрыла пробкой
и интенсивно
перемешала
встряхиванием.
№29 слайд
Содержание слайда: Результаты исследования:
Сравнила интенсивность цвета анализируемых растворов.
№30 слайд
Содержание слайда: ВЫВОДЫ:
1. Все исследуемые продукты питания содержат железо.
2. Самое большое содержание железа в ржаном хлебе.
№31 слайд
Содержание слайда: Итог урока.
Изучили соединения железа: оксиды и гидроксиды (II) и (III).
Соединения железа (II) проявляют основные свойства.
Соединения железа (III) проявляют
слабовыраженные амфотерные свойства , с преобладанием основных.
Реактивом на ион Fe2+ является красная кровяная соль при этом выпадает синий осадок – турнбулева синь.
Реактивами на ион Fe3+ являются желтая кровяная соль при этом выпадает синий осадок – берлинская лазурь и роданид калия – при этом образуется кроваво-красный раствор.
№32 слайд
Содержание слайда: План урока.
План урока.
5. Проверочный тест.
№33 слайд
Содержание слайда: То, что не ясно, следует выяснить. То, что трудно творить следует делать с величайшей настойчивостью.
Конфуций.
№34 слайд
Содержание слайда: Домашнее задание:
1. параграф №14, упр. 5.
2. Решите задачи:
а) В состав некоторых сортов природного мела входит оксид железа (III). Предложите опыт для качественного определения содержания железа в образце мела.
б) В куске белого пшеничного хлеба 0,8 мг Fe. Сколько кусков нужно съесть в день для удовлетворения суточной потребности в этом элементе? Суточная потребность для подростков 11-18 лет составляет 18 мг.
№35 слайд
Содержание слайда: Не в количестве знаний заключается образование, а в полном понимании и искусном применении всего того, что знаешь.
Дистервег.
№36 слайд
Содержание слайда: Спасибо за урок.













































