Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
11 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
910.00 kB
Просмотров:
50
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Связи металл – металл в соединениях молибдена и вольфрама
№2 слайд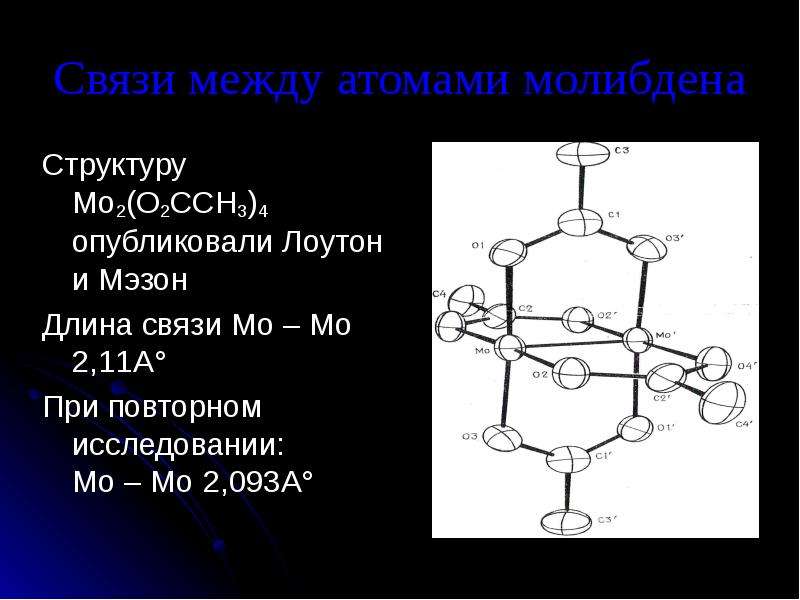
Содержание слайда: Связи между атомами молибдена
Структуру Mo2(O2CCH3)4 опубликовали Лоутон и Мэзон
Длина связи Mo – Mo 2,11А°
При повторном исследовании: Mo – Mo 2,093А°
№3 слайд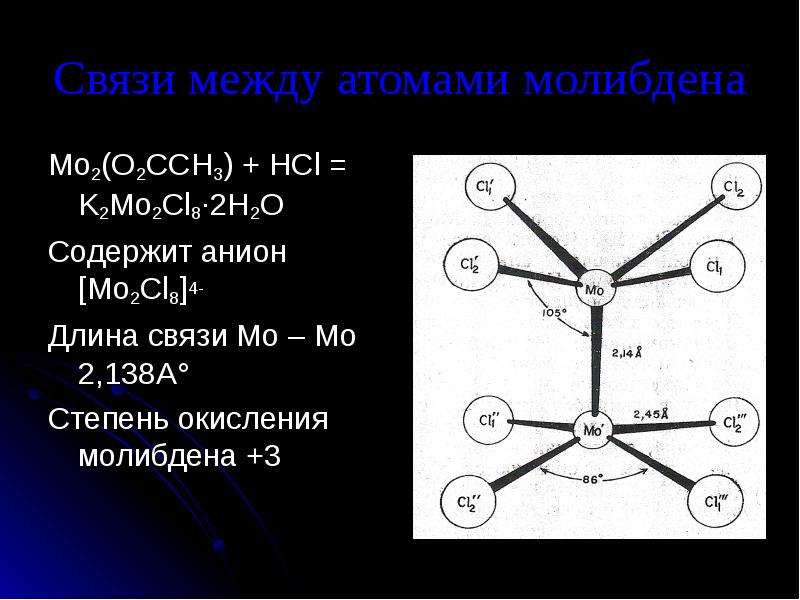
Содержание слайда: Связи между атомами молибдена
Mo2(O2CCH3) + HCl = K2Mo2Cl8∙2H2O
Содержит анион [Mo2Cl8]4-
Длина связи Mo – Mo 2,138А°
Степень окисления молибдена +3
№4 слайд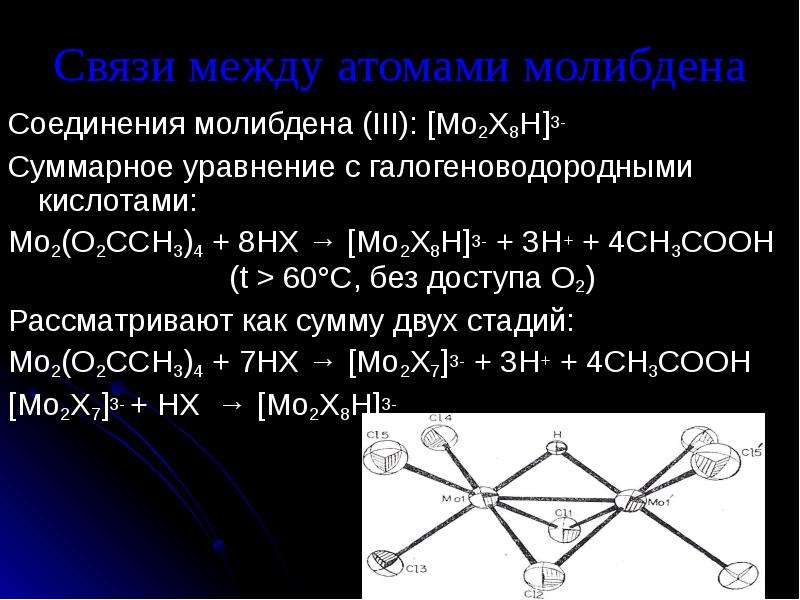
Содержание слайда: Связи между атомами молибдена
Соединения молибдена (III): [Mo2X8H]3-
Суммарное уравнение с галогеноводородными кислотами:
Mo2(O2CCH3)4 + 8HX → [Mo2X8H]3- + 3H+ + 4CH3COOH (t > 60°C, без доступа O2)
Рассматривают как сумму двух стадий:
Mo2(O2CCH3)4 + 7HX → [Mo2X7]3- + 3H+ + 4CH3COOH
[Mo2X7]3- + HX → [Mo2X8H]3-
№5 слайд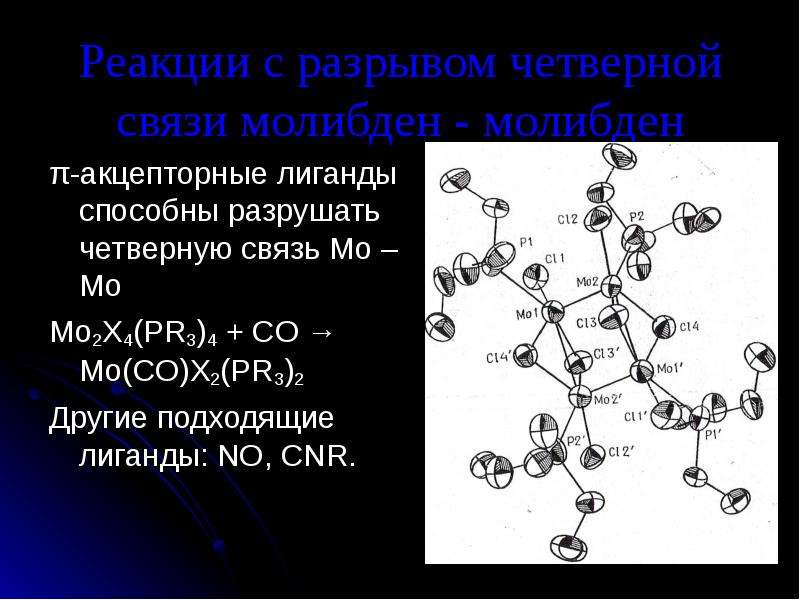
Содержание слайда: Реакции с разрывом четверной связи молибден - молибден
π-акцепторные лиганды способны разрушать четверную связь Mo – Mo
Mo2X4(PR3)4 + CO → Mo(CO)X2(PR3)2
Другие подходящие лиганды: NO, CNR.
№6 слайд
Содержание слайда: Связи между атомами вольфрама
Невозможно получить устойчивый карбоксилат вольфрама (II) W2(O2CR)4
Соединения W24+ очень легко окисляются
Попытки получить карбоксилаты типа W2(O2CR)4 привели к выделению и исследованию W2(O2CCF3)4
№7 слайд
Содержание слайда: Карбоксилаты вольфрама
Получение:
W(CO)6 + CH3COOH + (CH3CO)2O → W2(O2CCH3)4
W2(O2CCH3)4 –коричневого или желтовато – коричневого цвета
Среднее значение степени окисления вольфрама ≈ +3,6
Расстояния W – W равны 2,75А°.
№8 слайд
Содержание слайда: Димеры без мостиковых лигандов
Получение фосфиновых производных W2Cl4(PR3)4:
1 метод
2WCl4 + 4Na/Hg + PR3 → W2Cl4(PR3)4
где PR3 = PMe3, PMe2Ph, PMePh2
2 метод
WCl2(PMe3)4 → 0,5W2Cl4(PMe3)4 + 2PMe3 (Bu2O, кипячение)
WCl3(PMe3)3 → 0,25W2Cl4(PMe3)4 + 0,5WCl4(PMe3)4 + 0,5PMe3
№9 слайд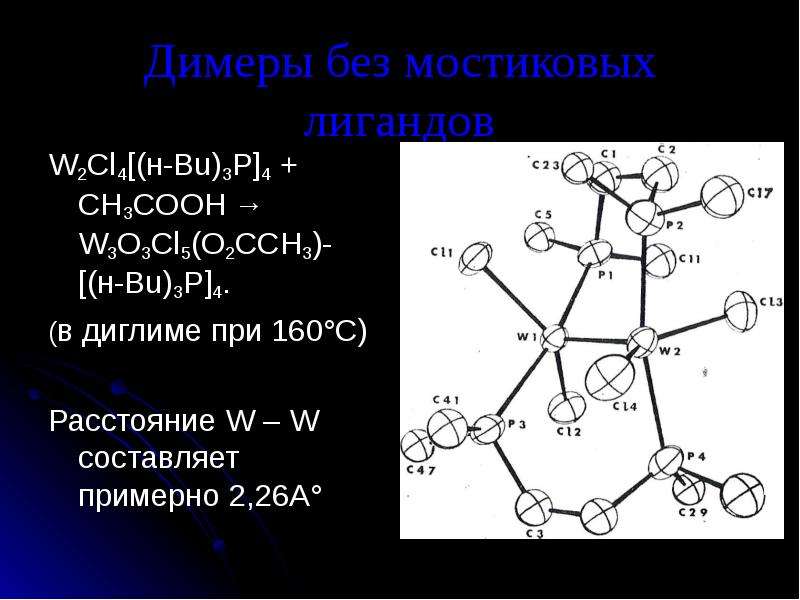
Содержание слайда: Димеры без мостиковых лигандов
W2Cl4[(н-Bu)3P]4 + CH3COOH → W3O3Cl5(O2CCH3)-[(н-Bu)3P]4.
(в диглиме при 160°С)
Расстояние W – W составляет примерно 2,26А°
№10 слайд
Содержание слайда: Димеры с мостиковыми лигандами
WCl4 + K2C8H8 → W2(COT)3 (в ТГФ)
Другие комплексы с четверными связями: W2(mhp)4, W2(chp)4, W2(map)4, W2(dmhp)4, где:
mhp – анион 2-окси-6-метилпиридина
chp – анион 2-окси-6-хлорпиридина
dmhp – анион 2,4-диметил-6-оксипиримидина
map – анион 2-амино-6-метилпиримидина
№11 слайд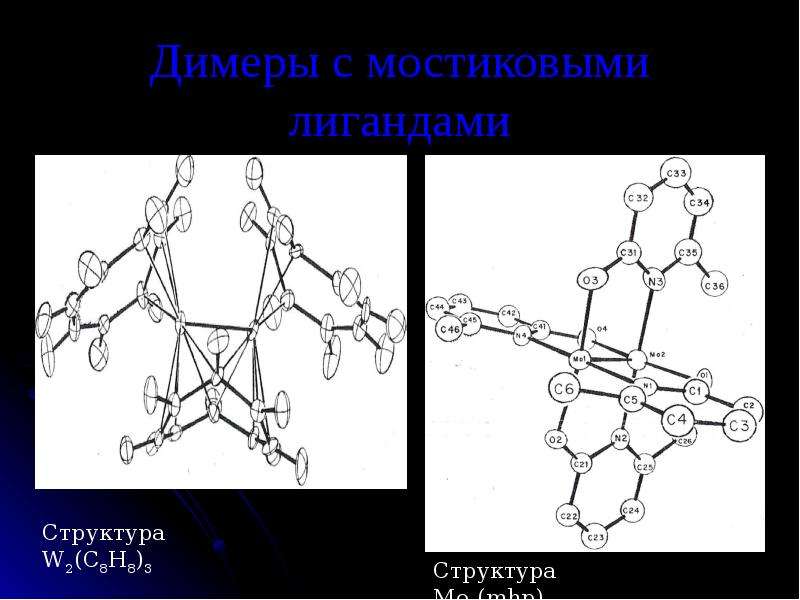
Содержание слайда: Димеры с мостиковыми лигандами




















