Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
32 слайда
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
10.13 MB
Просмотров:
76
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Углерод и его свойства.
9 класс.
№2 слайд
Содержание слайда: Цель : сформировать представления о свойствах углерода, уметь составлять схемы строения атома, аллотропии и его биологической роли, формирование умений решения задач.
Вопрос :
1. Почему на основе углерода строиться жизнь?
2. Почему углерод стал «началом вех начал» ?
№3 слайд
№4 слайд
Содержание слайда: Строение атома
Углерод (Carboneum-рождающий уголь)
№5 слайд
№6 слайд
Содержание слайда: Степени окисления атома углерода в соединениях:
-4 (SiC, CH4, Al4C3)
+2 (CO)
+4 (CO2 , CCl4 )
№7 слайд
Содержание слайда: Нахождение углерода в природе.
11 место по распространенности в природе.
4 место на Солнце ( Н2, Не, О2);
В земной коре: СаСО3 (известняк, мел, мрамор),
МgCO3CaCO3 (доломит), Сu2(OH)2CO3 (малахит), ZnCO3 (смитсонит);
горючие ископаемые;
в составе органических веществ;
в свободном состоянии в виде графита и алмаза.
№8 слайд
Содержание слайда: АЛЛОТРОПИЯ -
способность атомов одного химического элемента образовывать несколько простых веществ.
№9 слайд
№10 слайд
Содержание слайда: Простое вещество углерод.
Аллотропные модификации
углерода:
алмаз
графит
лонсдейлит
карбин
фуллерены
графен
№11 слайд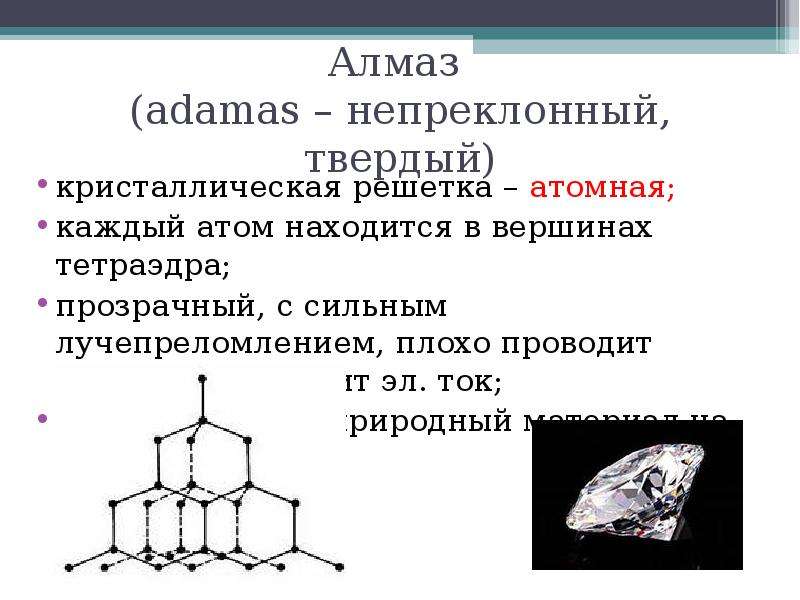
Содержание слайда: Алмаз
(adamas – непреклонный, твердый)
кристаллическая решетка – атомная;
каждый атом находится в вершинах тетраэдра;
прозрачный, с сильным лучепреломлением, плохо проводит тепло, не проводит эл. ток;
самый твердый, природный материал на Земле
№12 слайд
№13 слайд
Содержание слайда: Графит (grapho – пишу)
кристаллическая решетка - атомная
серо-черная, непрозрачная, жирная на ощупь, чешуйчатая, очень мягкая масса с металлическим блеском;
при 3700°С возгоняется;
проводит эл. ток
№14 слайд
№15 слайд
Содержание слайда: Взаимные превращения аллотропных модификаций углерода.
уголь графит (2600˚С, давление)
графит алмаз (1200МПа, 1500˚С)
алмаз графит (2000˚С)
№16 слайд
Содержание слайда: Карбин
мелкокристаллический порошок черного цвета;
по твердости между алмазом и графитом;
длинные цепочки атомов углерода, уложенные параллельно друг другу;
-С С – С С-
поликумулен = С = С = С = С =
№17 слайд
Содержание слайда: Фуллерены
получают испарением графита при высокой температуре при действии лазерного излучения в атмосфере гелия;
построены из шарообразных (С60) или дынеобразных (С70) молекул;
желтые или бурые кристаллы, хорошо растворимые в бензоле;
цена на фуллерены: С60 25 $ /г , С70 270 $ /г
№18 слайд
Содержание слайда: Аморфный углерод
Каменный и древесный уголь, кокс, сажа.
плотность, теплоемкость, теплопроводность и электропроводность выше, чем графита.
№19 слайд
Содержание слайда: Аморфный углерод
№20 слайд
Содержание слайда: Адсорбция
(ad — на, при; sorbeo — поглощаю)
№21 слайд
№22 слайд
Содержание слайда: Химические свойства углерода
Восстановительные свойства.
Записать уравнения реакций взаимодействия углерода
1) с фтором ,
2) с кислородом (избыток, недостаток),
3) с серой,
4) с оксидом меди (II) (восстановление меди)
5) с серной концентрированной кислотой,
6) с азотной концентрированной кислотой.
№23 слайд
Содержание слайда: Химические свойства углерода
Углерод вступает в реакции с солями кислородсодержащих кислот, связывая кислород:
BaSO4 + C = BaS + CO
Уравнять реакцию, составив схему электронного баланса.
№24 слайд
Содержание слайда: Химические свойства углерода
Окислительные свойства.
Записать реакции взаимодействия углерода
1) с металлами (Аl),
2) с водородом ,
3) с оксидом кремния (образование карборунда SiC).
№25 слайд
Содержание слайда: Реакции диспропорционирования:
При нагревании с оксидами активных металлов:
СаО + 3С = СаС2 + СО
2Аl2О3 + 9С = Аl4С3 + 6СО
№26 слайд
№27 слайд
№28 слайд
№29 слайд
№30 слайд
Содержание слайда: Домашняя работа
Составить схемы электронного баланса следующих реакций:
Ca + 2C = CaC2
4A1 + 3C = A14C3
C + 2FeO = 2Fe + CO2
№31 слайд
Содержание слайда: Какие утверждения верны:
Углерод содержится и в воздухе, и в земной коре, в болоте и в организме человека, а так же в растениях и животных.
Для очищения воздуха можно использовать уголь.
У углерода 2 аллотропные модификации: алмаз и графит.
Углерод проявляет только восстановительные свойства.
Углерод взаимодействует с щелочами.
Углерод является биогенным элементом.
№32 слайд
Содержание слайда: Решить задачу.
К 125 г раствора серной кислоты добавили избыток гидрокарбоната натрия. Общий объем выделившегося газа составил 11,2 л (н.у.). Определите массовую долю серной кислоты в растворе.









































