Презентация Введение. Теория строения органических соединений А. М. Бутлерова. Лекция 1 онлайн
На нашем сайте вы можете скачать и просмотреть онлайн доклад-презентацию на тему Введение. Теория строения органических соединений А. М. Бутлерова. Лекция 1 абсолютно бесплатно. Урок-презентация на эту тему содержит всего 54 слайда. Все материалы созданы в программе PowerPoint и имеют формат ppt или же pptx. Материалы и темы для презентаций взяты из открытых источников и загружены их авторами, за качество и достоверность информации в них администрация сайта не отвечает, все права принадлежат их создателям. Если вы нашли то, что искали, отблагодарите авторов - поделитесь ссылкой в социальных сетях, а наш сайт добавьте в закладки.
Презентации » Химия » Введение. Теория строения органических соединений А. М. Бутлерова. Лекция 1
Оцените!
Оцените презентацию от 1 до 5 баллов!
- Тип файла:ppt / pptx (powerpoint)
- Всего слайдов:54 слайда
- Для класса:1,2,3,4,5,6,7,8,9,10,11
- Размер файла:492.56 kB
- Просмотров:95
- Скачиваний:0
- Автор:неизвестен
Слайды и текст к этой презентации:
№2 слайд


Содержание слайда: Лекция № 1
Тема: «Введение. Теория строения органических соединений А.М.Бутлерова»
План:
1. Предмет и задачи органической химии. Значение орг. химии для медицины и фармации.
2. Роль русских ученых в становлении и развитии органической химии.
3. Теория строения орг. соединений А.М.Бутлерова. Гибридизация атома углерода. Виды гибридизации.
4. Классификация органических соединений.
№3 слайд


Содержание слайда: 1. Предмет и задачи органической химии. Значение орг. химии для медицины и фармации.
Объектом изучения органической химии являются соединения углерода, называемые органическими веществами. В связи с этим органическую химию называют химией соединений углерода.
Первые органические вещества, с которыми познакомился человек, были выделены из растительных и животных организмов или из продуктов их жизнедеятельности, а также каменный уголь, торф, природный газ, нефть. Каждый растительный или животный организм представляет собой своеобразную химическую лабораторию, в которой протекает множество сложнейших реакций, приводящих к образованию огромного числа органических веществ, как весьма простых (например, метан, муравьиная, щавелевая кислоты и т. п.), так и самых сложных (например, алкалоиды, стероиды, белки).
№4 слайд


Содержание слайда: В состав орг. соединений кроме углерода входят и другие элементы, чаще всего водород, кислород , азот, фосфор, сера. Существуют орг. соединения в своём составе атомы металлов.
Органическая химия способствует развитию смежных отраслей науки как биологии, биохимии, агрохимии, фармации и медицины. 95 % лекарственных веществ имеют органическую природу.
Велико значение для фармации органического синтеза, являющегося фундаментом для создания новых эффективных ЛС со специфическим фармакологическим действием.
№6 слайд


Содержание слайда: Зинин Николай Николаевич (1812-1880), русский химик-органик, академик Петербургской АН с 1865 г. По окончании Казанского университета (1833) преподавал там же физику и механику. По получении степени магистра химии (1836). В 1837 г. и командирован за границу, где посетил лаборатории и заводы Германии, Франции, Англии; свыше года (1839—40) работал у Ю. Либиха. После защиты докторской диссертации (1841) избран профессором Казанского университета; в 1848—64 профессор Медико-хирургической академии в Петербурге и там же директор химических работ
(1864—74).
№7 слайд


Содержание слайда: Марковников Владимир Васильевич (1837-1904), русский химик. Ученик А. М. Бутлерова. Окончил в 1860 Казанский университет; с 1862 читал там же лекции (с 1869 профессор). В 1871 вместе с группой передовых учёных ушёл из Казанского университета в знак протеста против увольнения профессора П. Ф. Лесгафта, в 1871—73 профессор Новороссийского университета (в Одессе). С 1873 профессор Московского университета.
№8 слайд


Содержание слайда: Зайцев Александр Михайлович(1841-1910),
русский химик-органик, член-корреспондент Петербургской АН (1885). Ученик А. М. Бутлерова. По окончании Казанского университета работал (1862—65) в лабораториях Кольбе и Вюрца. В 1870 защитил докторскую диссертацию «Новый способ превращения жирных кислот в соответствующие им алкоголи» и был утвержден профессором Казанского
университета.
№9 слайд


Содержание слайда: 3елинский Николай Дмитриевич(1861-1953), советский химик-органик, академик АН СССР (1929), один из основоположников учения об органическом катализе. Герой Социалистического Труда (1945). В 1884 окончил Новороссийский университет (Одесса), там же защитил магистерскую (1889) и докторскую (1891) диссертации. В 1893—1953 профессор Московского университета, кроме периода 1911—1917, когда он покинул университет вместе с группой учёных в знак протеста против реакционной политики царского министра народного просвещения Л. А. Кассо (в эти годы Зелинский был в Петербурге директором Центральной лаборатории министерства финансов и заведующим кафедрой в Политехническом институте). В 1935 активно участвовал в организации института органической химии АН СССР, в котором затем руководил рядом лабораторий; этот институт с 1953 носит его имя.
№10 слайд


Содержание слайда: Кучеров Михаил Григорьевич (1850-1911), русский химик-органик. В 1871 окончил Петербургский земледельческий (с 1877 — лесной) институт и работал там же (до 1910). Основные работы посвящены изучению непредельных углеводородов. В 1881 Кучеров открыл метод гидратации соединений ацетиленового ряда в присутствии ртутных солей (см. Кучерова реакция), за что получил (1885) премию Русского физико-химического общества. Это общество учредило (1915) премию имени Кучерова, присуждавшуюся начинающим исследователям в области химии.
№11 слайд


Содержание слайда: Лебедев Сергей Васильевич (1874-1934), советский химик, академик АН СССР (1932; член-корреспондент 1928). Ученик А. Е. Фаворского. Гимназическое образование получил в Варшаве. В 1900 окончил Петербургский университет. С 1902 работал в Петербургском университете, где в 1925 организовал Лабораторию по химической переработке нефти и каменного угля. В
1928—1930 Лебедев заведовал созданной по
его инициативе Лабораторией синтетического каучука. В 1934 организовал Лабораторию высокомолекулярных соединений АН СССР.
№12 слайд


Содержание слайда: Несмеянов Александр Николаевич (1899-1980),
советский химик-органик, академик АН СССР (1943; член-корреспондент 1939), общественный деятель, Герой Социалистического Труда (1969). Член КПСС с 1944. После окончания МГУ (1922) работает там же (с 1935 профессор, с 1944 заведующий кафедрой органической химии, в 1944—48 декан химического факультета, в 1948—51 ректор, руководил организацией строительства МГУ на Ленинских горах). Одновременно работал в институте удобрений и инсектофунгицидов (1930—34), в АН СССР: в институте органической химии (с 1934, в 1939—54 директор), академик-секретарь Химического отделения (1946—51). Президент АН СССР (1951—61), директор института элементоорганических соединений (с 1954), академик-секретарь Отделения общей и органической химии (с 1961). В 1947—1961 председатель Комитета по Ленинским и Государственным премиям в области науки и техники. Принимал деятельное участие в работе Всемирного Совета Мира и Советского комитета защиты мира.
№13 слайд


Содержание слайда: 3. Теория строения орг. соединений А.М.Бутлерова. Гибридизация атома углерода. Виды гибридизации.
Основные положения теории:
1. Атомы в молекулах соединены друг с другом химическими связями в соответствии с их валентностью, :
С – IV;
Н, Наl, щелочные металлы – I;
S, O – II;
N – III,V
Например:
Н
ǀ
Н- С – Н;
ǀ
Н
№15 слайд


Содержание слайда: 3. Свойства орг.соединений зависят не только от числа и природы входящих в их состав атомов, но и от химического строения молекул:
а). Изомеры - орг. соединения, имеющие одинаковый количественный и качественный состав, но различное химическое строение:
СН3 - СН2 – СН2 –СН3 бутан
СН3 - СН –СН3 изобутан
ǀ
СН3
б). Гомологи – орг. соединения, имеющие сходное химическое строение и качественный состав, но различный количественный состав:
СН4 метан
Н3С-СН3 этан
Н3С- СН2-СН3 пропан
СН3 - СН2 – СН2 –СН3 бутан
№16 слайд


Содержание слайда: 4. Атомы в молекулах орг. соединений оказывают взаимное влияние друг на друга. Наибольшее влияние оказывают атомы, непосредственно связанные друг с другом. Влияние атомов или групп атомов, не связанных непосредственно, ослабевает по мере их удаления друг от друга.
5. Химическое строение вещества можно определить в результате его химических превращений, и наоборот, по строению вещества можно характеризовать его свойства.
№17 слайд


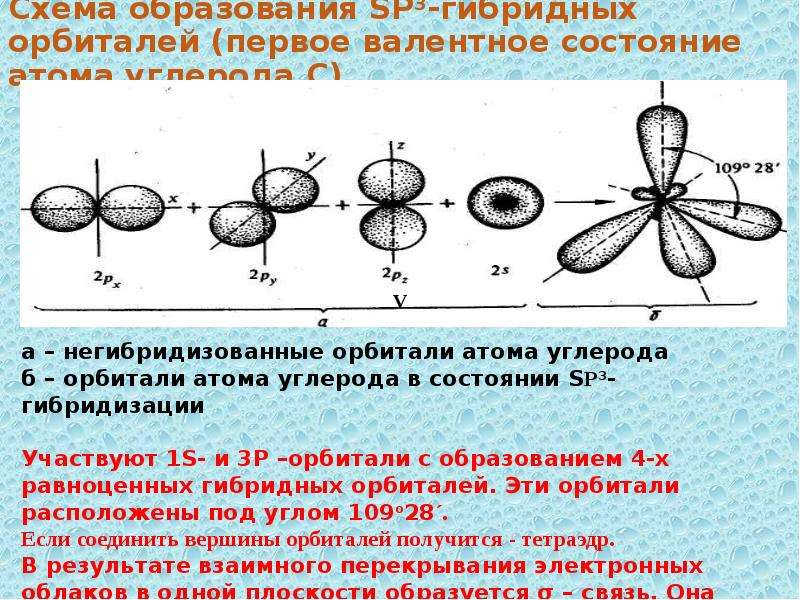
Содержание слайда: Гибридизация атомов углерода
Гибридизация – это смещение валентных электронных облаков и образование качественно новых, равноценных гибридных валентных электронных облаков.
В ПСХЭ Д.И.Менделеева углерод расположен в главной подгруппе IV группы, поэтому электронная структура атома С , если :
1) атом углерода С6 в невозбужденном состоянии - имеет электронную формулу - 1S22S22P2 , т. е на внешнем электронном слое находятся 2 неспаренных электрона (валентность – II)
2) атом углерода С6 в возбужденном состоянии - имеет электронную формулу - 1S22S12P3 , т.е. 4 неспаренных электрона
(валентность – IV)
S –орбиталь имеет сферическую форму;
Р-орбиталь - форму объёмной восьмерки, ориентированной в пространстве определенным образом
№20 слайд


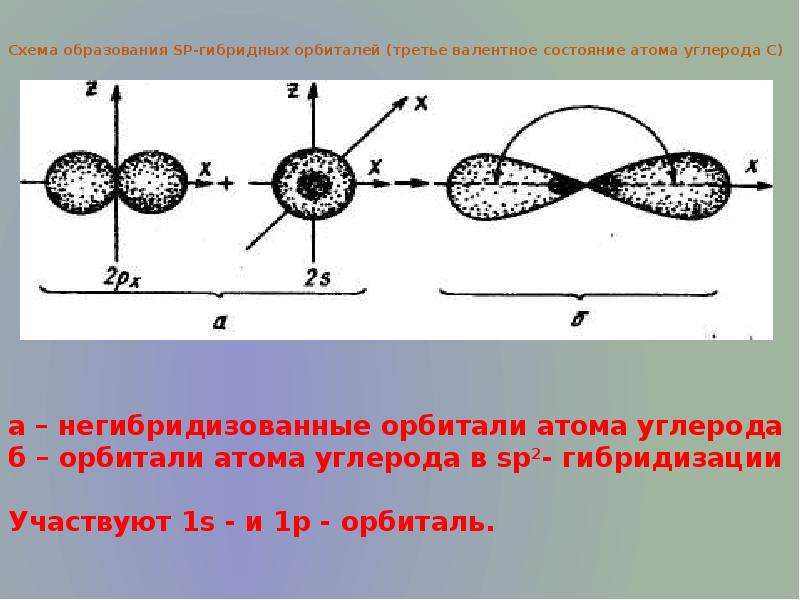
Содержание слайда: Отличие от sp3 –орбиталей –большая лопасть объёмной восьмёрки короче. sp2- орбитали лежат в одной плоскости и направлены по углом 120о друг к другу, их вершины образуют равносторонний треугольник.
Одна р-орбиталь остается свободной (негибридизованной). Она сохраняет форму правильной объёмной восьмёрки и располагается перпендикулярно плоскости, в которой лежат 3 sp2- гибридных орбитали. В результате перекрывания электронных облаков в 2-х взаимно перпендикулярных областях образуется π –связь. Этот тип гибридизации характерен для соединений с двойными связями, одна из которых σ – связь , вторая π –связь . Длина связи С-С равна 0,134 нм.
№22 слайд


Содержание слайда: В результате образуются две равноценные гибридные орбитали, имеющие форму объёмных восьмёрок с еще более короткой лопастью. Они расположены под углом 180о друг другу, т.е. на одной прямой и направлены в противоположные стороны от ядра атома
Две не участвующие в гибридизации р-орбитали сохраняют форму правильных восьмёрок и располагаются взаимно перпендикулярно. Этот тип гибридизации характерен для соединений с тройными связями, одна из которых σ – связь и две π – связи. Длина связи С-С равна 0,12 нм.
В органических соединениях в основном ковалентная химическая связь
№23 слайд


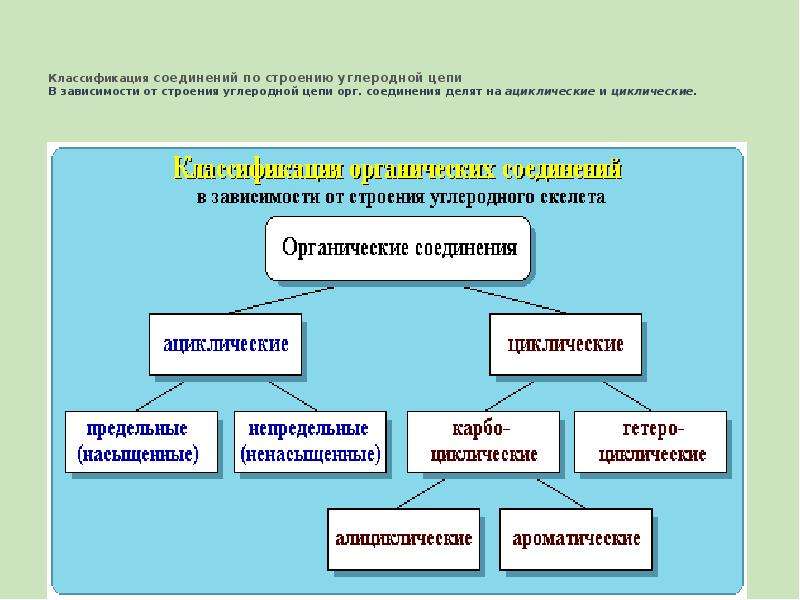
Содержание слайда: 4. Классификация органических соединений.
Органические соединения отличаются своей многочисленностью и разнообразием. Поэтому необходима их систематизация. Органические соединения классифицируют, учитывая два основных структурных признака:
- строение углеродной цепи (углеродного скелета);
- наличие и строение функциональных групп.
· Углеродный скелет (углеродная цепь) - последовательность химически связанных между собой атомов углерода.
· Функциональная группа - атом или группа атомов, определяющие принадлежность соединения к определенному классу и ответственные за его химические свойства.
№28 слайд


Содержание слайда: Циклические соединения - соединения с замкнутой углеродной цепью.
В зависимости от природы атомов, составляющих цикл, различают карбоциклические и гетероциклические соединения.
Карбоциклические соединения содержат в цикле только атомы углерода. Они делятся на две существенно различающихся по химическим свойствам группы: алифатические циклические - сокращенно алициклические - и ароматические соединения.
№31 слайд


Содержание слайда: Классификация соединений по функциональным группам
Соединения, в состав которых входят только углерод и водород, называются углеводородами. Другие, более многочисленные, органические соединения можно рассматривать как производные углеводородов, которые образуются при введении в углеводороды функциональных групп, содержащих другие элементы. В зависимости от природы функциональных групп органические соединения делят на классы. Некоторые наиболее характерные функциональные группы и соответствующие им классы соединений приведены в таблице:
№34 слайд


Содержание слайда: В состав молекул органических соединений могут входить две или более одинаковых или различных функциональных групп.
Например:
HO-CH2-CH2-OH (спирт : этиленгликоль);
NH2-CH2-COOH (аминокислота: глицин).
Все классы органических соединений взаимосвязаны. Переход от одних классов соединений к другим осуществляется в основном за счет превращения функциональных групп без изменения углеродного скелета.
№36 слайд


Содержание слайда: 1. Общая характеристика, гомологический ряд, номенклатура, изомерия.
Алканы – алифатические углеводороды, в молекулах которых атомы углерода связаны между собой одинарной σ – связью, а остальные их валентности предельно насыщены атомами водорода, отсюда их название – предельные (насыщенные углеводороды).
Простейший представитель - СН4.
Общая формула :
СnН2n+2
№39 слайд


Содержание слайда: Номенклатура
Для названия алканов с разветвлённой углеродной цепью необходимо знать названия органических радикалов –алкилов.
Алкил – частица, образующаяся при отщеплении от молекулы алкана одного атома водорода:
Общая формула алкилов (радикалов):
СnН2n+1
Алкил обозначают R или Alk
№41 слайд


Содержание слайда: Систематическая (научная) номенклатура – ИЮПАК
1. Выбираем самую длинную цепочку.
2. Нумеруем её с той стороны, где ближе разветвления
( радикалы).
3. Цифрой указываем номера углеродных атомов, у которых есть радикалы.
4. Называем эти радикалы. Если 2 одинаковых радикала – добавляем частицу «ди», если 3 - «три», если 4 – «тетра» и т.д.
5. Называем всю цепочку.
№42 слайд


Содержание слайда: Рациональная номенклатура
1. Выбираем центральный атом и обозначаем его *.
Центральный атом тот, который имеет максимальное количество связей С-С.
2. Отсекаем все связи, отходящие от центрального атома.
3. Называем радикалы от младшего к старшему, используя п.4 систематической номеклатуры. Если радикал имеет разветвление, то его названию добавляется частица «изо».
4. К названию радикалов добавляем слово «МЕТАН»
№44 слайд


Содержание слайда: 3. Щелочной гидролиз солей карбоновых кислот
( лабораторный способ получения – берём смесь Na2CO3 + Са(ОН)2, которая наз. Натронной известью:
CH3COONa + NaOH -> CH4 + Na2CO3
4. Гидролиз карбидов :
Al4C3 + 12H2O -> 3CH4 + 4Al(OH3)
5. Электролиз одноосновных карбоновых кислот:
СН3СООNа -> СНСОО- + Nа+
Аn(+) -2е
2СНСОО- -> 2СО2 ↑+ СН3 – СН3
6. Омыление элементорганических соединений:
СН3МgСl + НОН -> СН4+ МgОНСl
7. Восстановление галогенпроизводных углеводородов:
СН3Сl + НСl -> СН4+ Сl2
8. Прямой синтез из углерода и водорода при tº= 400º- 500 º и повышении давления в присутствии катализатора Кt:
С + 2Н2 -> СН4
№46 слайд


Содержание слайда: 1. Реакции галогенирования
Галогенирование – это реакция замещения одного или более атомов водорода в молекуле углеводорода на галоген. Продукты реакции называют галогенопроизводными углеводородов.
Реакция алканов с хлором и бромом идет на свету или при нагревании.
Хлорирование метана:
№49 слайд


Содержание слайда: 2. Реакция нитрования алканов
(реакция Коновалова)
На алканы действует pазбавленная азотная кислота пpи нагpевании и давлении. В pезультате пpоисходит замещение атома водоpода на остаток азотной кислоты – нитpогpуппу NO2. Эту pеакцию называют pеакцией нитpования, а пpодукты pеакции – нитpосоединениями. В молекулах алканов легче всего замещаются атомы водорода у третичных, затем вторичных и первичных атомов водорода.
Схема реакции:
№51 слайд


Содержание слайда: 4. Реакция дегидрирования алканов
По связям С–Н возможны реакции отщепления атома водорода (дегидрирование).
При нагревании алканов в присутствии катализаторов происходит их каталитическое дегидрирование за счет разрыва связей С-Н и отщепления атомов водорода от соседних углеродных атомов. При этом алкан превращается в алкен с тем же числом углеродных атомов в молекуле:
№53 слайд


Содержание слайда: 4. Отдельные представители.
Метан - СН4 – бесцветный газ, без запаха, мало растворим в воде, легче воздуха, называется болотным газом, т.к. образуется при гниении растительных остатков на дне болот без доступа воздуха. Метан – главная часть нефтяного и природного газа. Составляет сырьевую основу важнейших химических промышленных процессов получения углерода, водорода, ацетилена, кислородсодержащих орг. соединений – спиртов, альдегидов, кислот.
№54 слайд


Содержание слайда: Вазелиновое масло – смесь алканов до С15, безцветная жидкость, без запаха и вкуса, используется в медицине и парфюмерии.
Вазелин – смесь жидких и твёрдых алканов до С25. В медицине применяется как основа мазей, не всасывается кожей.
Парафин – смесь твёрдых алканов С18 - С35 . Белая масса без запаха и вкуса. В медицине используется для физиотерапевтическх процедур (парафинолечение)
Скачать все slide презентации Введение. Теория строения органических соединений А. М. Бутлерова. Лекция 1 одним архивом:
Похожие презентации
-
 ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ А. М. БУТЛЕРОВА Становление органической химии. Предпосылки теории строения
ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ А. М. БУТЛЕРОВА Становление органической химии. Предпосылки теории строения -
 ТЕОРИЯ СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ А. М. БУТЛЕРОВА.
ТЕОРИЯ СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ А. М. БУТЛЕРОВА. -
 ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ А. М. БУТЛЕРОВА Становление органической химии. Предпосылки теории строе
ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ А. М. БУТЛЕРОВА Становление органической химии. Предпосылки теории строе -
 Теория химического строения органических соединений А. М. Бутлерова
Теория химического строения органических соединений А. М. Бутлерова -
 Теория химического строения органических соединений А. М. Бутлерова (ТХС)
Теория химического строения органических соединений А. М. Бутлерова (ТХС) -
 По Химии "Теория строения органических соединений" - скачать смотреть
По Химии "Теория строения органических соединений" - скачать смотреть -
 Теория химического строения органических веществ А. М. Бутлерова
Теория химического строения органических веществ А. М. Бутлерова -
 Основы строения органических соединений. Теория строения органических соединений
Основы строения органических соединений. Теория строения органических соединений -
 Теория строения химических соединений А. М. Бутлерова
Теория строения химических соединений А. М. Бутлерова -
 Теория строения химических соединений А. М. Бутлерова
Теория строения химических соединений А. М. Бутлерова