Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
23 слайда
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
1.36 MB
Просмотров:
85
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
№2 слайд
№3 слайд
№4 слайд
№5 слайд
Содержание слайда: Содержание кислорода в природе
Распространение элементов в природе (по массе, в %)
№6 слайд
Содержание слайда: Кремний ( IV) оксиды– SiO2
№7 слайд
Содержание слайда: Алюминий оксиды- Al2O3
№8 слайд
№9 слайд
№10 слайд
Содержание слайда: Кислород – в организме
Белки, жиры, углеводы, гормоны, ферменты
№11 слайд
Содержание слайда: II.Кислород –простое вещество
№12 слайд
Содержание слайда: Карл Шееле,
Швеция 1772 год:
«Атмосферный воздух состоит из двух частей: «огненный воздух» - поддерживает дыхание и горение, «испорченный воздух» - не поддерживает горения».
№13 слайд
Содержание слайда: Джозеф Пристли,
Англия, 1774 год
Терекөмеш оксидын таркатып кислород таба
2HgO = 2Hg + O2
№14 слайд
Содержание слайда: Джозеф Пристли
№15 слайд
Содержание слайда: Антуан Лоран Лавуазье, Франция, 1777 год
Подлинная природа этого газа была установлена во Франции. Название Oxygenium – кислотообразующий, предложено Лавуазье.
№16 слайд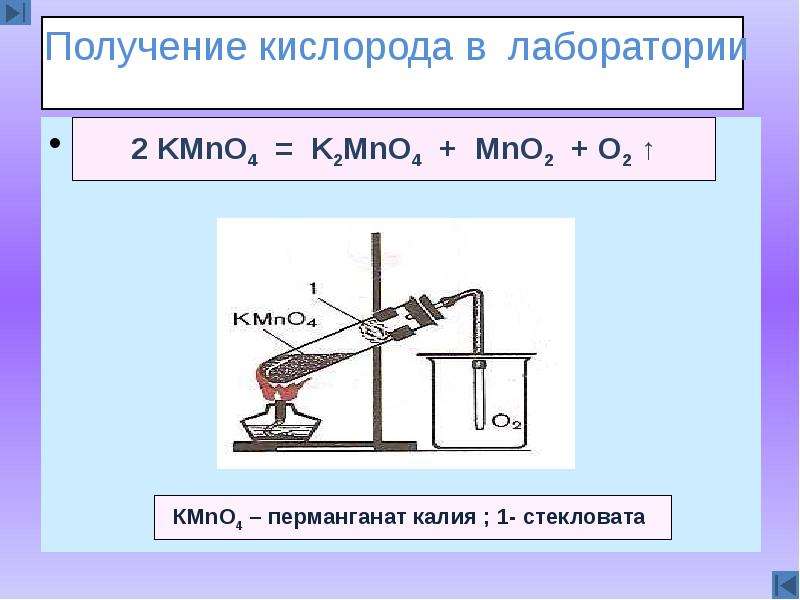
Содержание слайда: Сказка
№17 слайд
Содержание слайда: Физические войства:
Газ
Без цвета, запаха, вкуса
Малорастворим в воде
Һавадан бераз авыр
32> 29 тяж.возд.
Суда аз эри
Сжижается при -183 С- превращается в жидкость
При температуре -218,8 C, превращается в кристаллическое состояние
№18 слайд
Содержание слайда: Химические свойства
Реакции горения неметаллов
С+ O2 = С O2
S + O2 = S O2
4P + 5O2 = 2 P2O5
2H2 + O2 = 2H2O
Реакции горения металлов
2Mg + O2 = 2MgO
3Fe + 2O2 = Fe3O4
2С a+ O2 = 2CaO
№19 слайд
Содержание слайда: Химические свойства
Реакции горения сложных веществ
СН4+ 2O2 = СO2 + 2H2O
СS2 + 3O2 = 2S O2 + СO2
C2H6О + 3O2 = 2CO2 + 3H2O
№20 слайд
№21 слайд
Содержание слайда: Повторим
1. Охарактеризуйте кислород как химический элемент.
2.Где содержится кислород?
3. Кто открыл кислород?
4.Как получают кислород?
5.Какими физическими свойствами обладает кислород?
6.В какие реакции вступает кислород?
7.Где применяется?
№22 слайд
Содержание слайда: Задания для закрепления
1.Сколько молекул содержится в 2 моль кислорода?
2.В каком природном соединении больше кислорода ( % по массе) в известняке СаСО3 или поташе К2СО3 ?
3.Расставьте коэффициенты в следующих уравнениях хим.реакции:
AgNO3 → Ag +NO2 +O2 Mg(NO3)2 → MgO + NO2 +O2
4. Составьте уравнения хим.реакции горения следующих веществ: С2Н4, Сu2S
5. Из предложенного перечня выпишите формулы всех кислородсодержащих соединении
Н2О, МgS , SiO2, NaOH, F eS2, H2SO4, CaCO3, Al2S3, ZnO.
Сайт http://flsh.ucoz.ru
№23 слайд
Содержание слайда: Всем спасибо за урок!
































