Презентация Общая характеристика металлов главных подгрупп I-III онлайн
На нашем сайте вы можете скачать и просмотреть онлайн доклад-презентацию на тему Общая характеристика металлов главных подгрупп I-III абсолютно бесплатно. Урок-презентация на эту тему содержит всего 30 слайдов. Все материалы созданы в программе PowerPoint и имеют формат ppt или же pptx. Материалы и темы для презентаций взяты из открытых источников и загружены их авторами, за качество и достоверность информации в них администрация сайта не отвечает, все права принадлежат их создателям. Если вы нашли то, что искали, отблагодарите авторов - поделитесь ссылкой в социальных сетях, а наш сайт добавьте в закладки.
Презентации » Образование » Общая характеристика металлов главных подгрупп I-III
Оцените!
Оцените презентацию от 1 до 5 баллов!
- Тип файла:ppt / pptx (powerpoint)
- Всего слайдов:30 слайдов
- Для класса:1,2,3,4,5,6,7,8,9,10,11
- Размер файла:3.14 MB
- Просмотров:52
- Скачиваний:0
- Автор:неизвестен
Слайды и текст к этой презентации:
№2 слайд
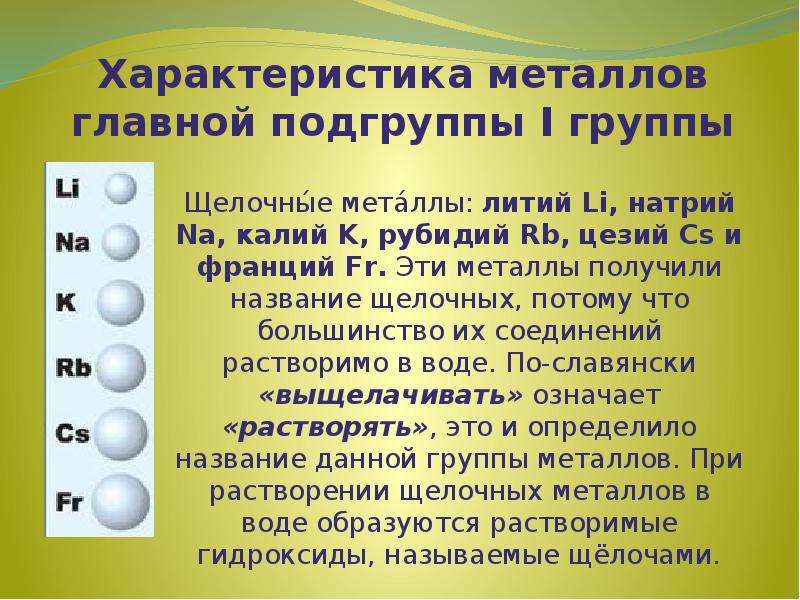

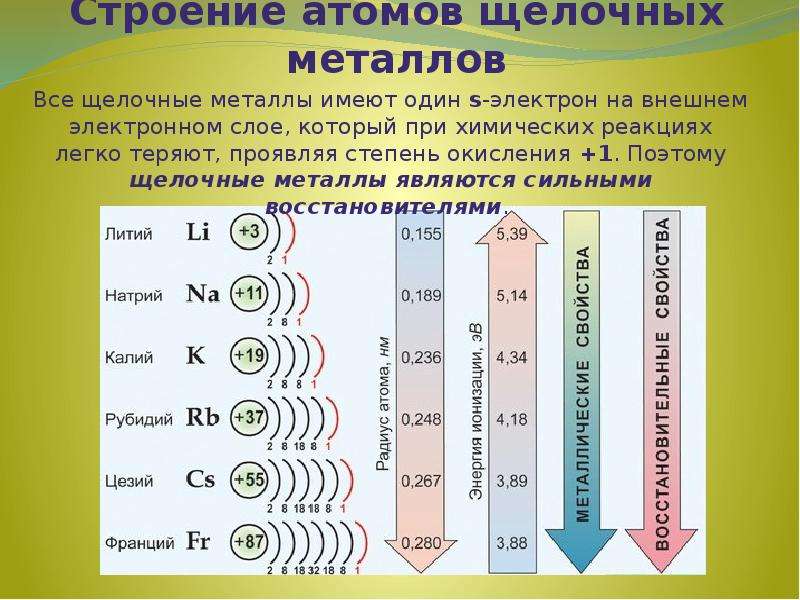
Содержание слайда: Характеристика металлов главной подгруппы I группы
Щелочны́е мета́ллы: литий Li, натрий Na, калий K, рубидий Rb, цезий Cs и франций Fr. Эти металлы получили название щелочных, потому что большинство их соединений растворимо в воде. По-славянски «выщелачивать» означает «растворять», это и определило название данной группы металлов. При растворении щелочных металлов в воде образуются растворимые гидроксиды, называемые щёлочами.
№4 слайд


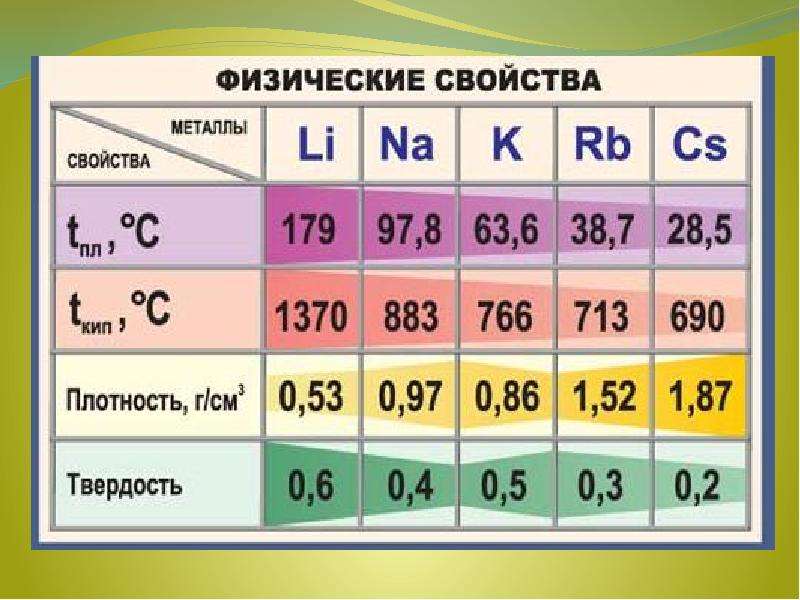
Содержание слайда: Физические свойства
Все металлы этой подгруппы имеют серебристо-белый цвет (кроме серебристо-жёлтого цезия), они очень мягкие, их можно резать скальпелем. Литий, натрий и калий легче воды и плавают на её поверхности, реагируя с ней. Поэтому хранят эти металлы под слоем керосина или парафина.
№6 слайд


Содержание слайда: Получение щелочных металлов
1. Для получения щелочных металлов используют в основном электролиз расплавов их галогенидов, чаще всего — хлоридов, образующих природные минералы:
катод: Li+ + e → Li
анод: 2Cl- — 2e → Cl2
2. Иногда для получения щелочных металлов проводят электролиз расплавов их гидроксидов:
катод: Na+ + e → Na
анод: 4OH- — 4e → 2H2O + O2
Поскольку щелочные металлы в электрохимическом ряду напряжений находятся левее водорода, то электролитическое получение их из растворов солей невозможно; в этом случае образуются соответствующие щёлочи и водород.
№7 слайд


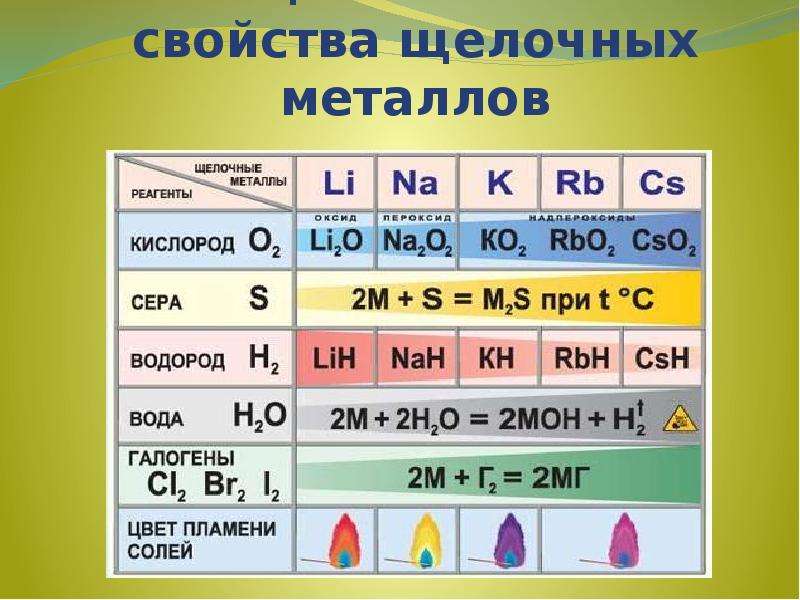
Содержание слайда: Химические свойства
Реакции с неметаллами
(образуются бинарные соединения):
4Li + O2 2Li2O(оксид лития)
2Na + O2 Na2O2(пероксид натрия)
K + O2 KO2(надпероксид калия)
2Li + Cl2 = 2LiCl(галогениды)
2Na + S = Na2S(сульфиды)
2Na + H2 = 2NaH(гидриды)
6Li + N2 = 2Li3N(нитриды)
2Li + 2C = 2Li2C2(карбиды)
№11 слайд
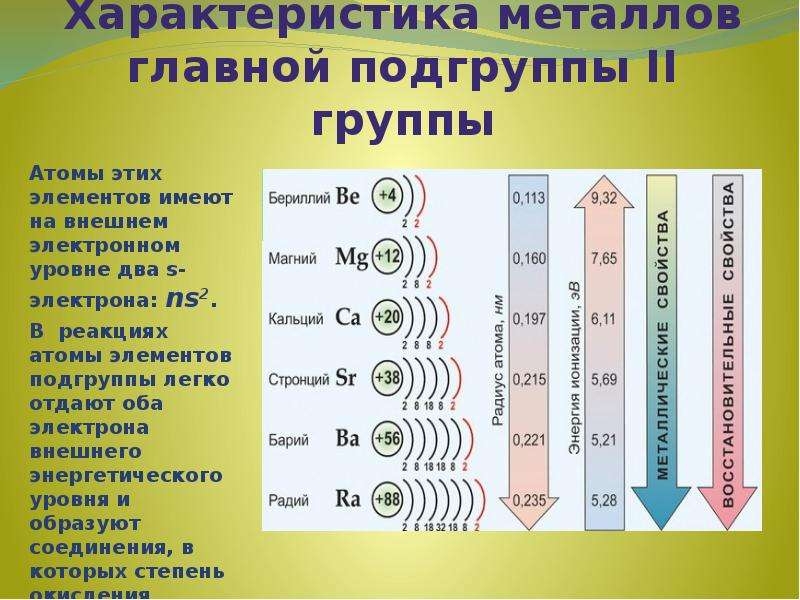

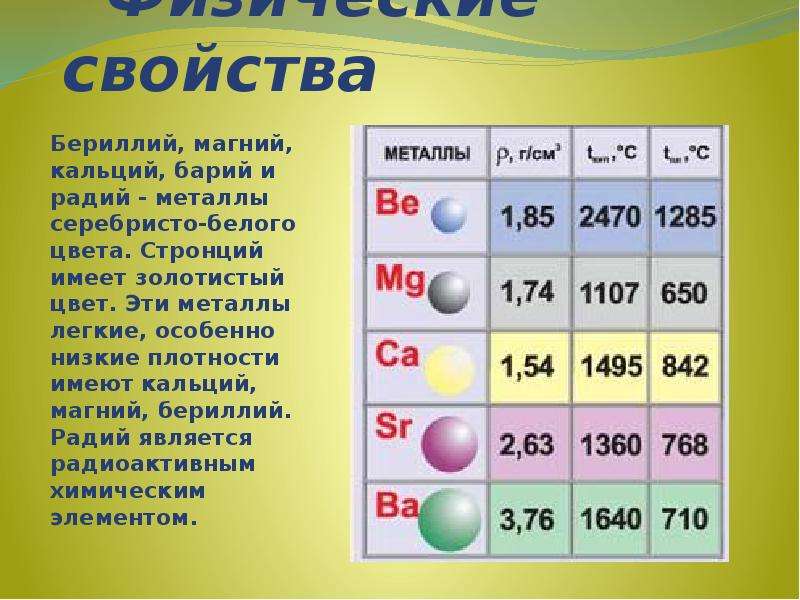
Содержание слайда: Характеристика металлов главной подгруппы II группы
Атомы этих элементов имеют на внешнем электронном уровне два s-электрона: ns2.
В реакциях атомы элементов подгруппы легко отдают оба электрона внешнего энергетического уровня и образуют соединения, в которых степень окисления элемента равна +2.
№15 слайд


Содержание слайда: Взаимодействие с простыми веществами
Все легко взаимодействуют с кислородом и серой, образуя оксиды и сульфаты:
2Be + O2 = 2BeO
Ca + S = CaS
Бериллий и магний реагируют с кислородом и серой при нагревании, остальные металлы - при обычных условиях.
Все металлы этой группы легко реагируют с галогенами:
Mg + Cl2 = MgCl2
При нагревании все реагируют с водородом, азотом, углеродом, кремнием и другими неметаллами:
Ca + H2 = CaH2 (гидрид кальция)
3Mg + N2 = Mg3N2 (нитрид магния)
Ca + 2C = CaC2 (карбид кальция)
№16 слайд


Содержание слайда: Взаимодействие с кислотами
Все взаимодействуют с хлороводородной и разбавленной серной кислотами с выделением водорода:
Be + 2HCl = BeCl2 + H2
Разбавленную азотную кислоту металлы восстанавливают главным образом до аммиака или нитрата аммония:
2Ca + 10HNO3(разб.) = 4Ca(NO3)2 + NH4NO3 + 3H2O
В концентрированных азотной и серной кислотах (без нагревания) бериллий пассивирует, остальные металлы реагируют с этими кислотами.
№18 слайд


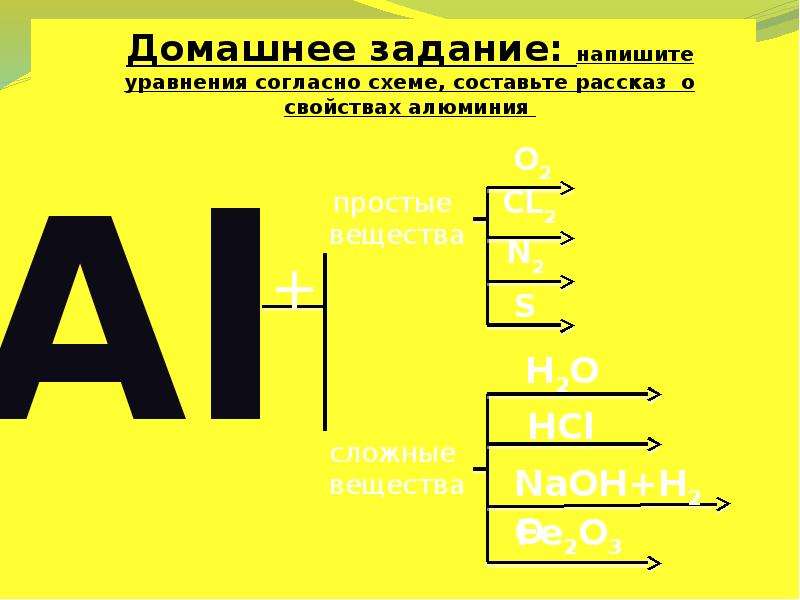
Содержание слайда: Алюминий
13Al [Ne] 3s23p1
Алюминий находится в главной п/группе III группы периодической системы.
На внешнем энергетическом уровне имеются свободные р-орбитали, что позволяет ему переходить в возбужденное состояние. В возбужденном состоянии атом алюминия образует три ковалентные связи или полностью отдает три валентных электрона, проявляя степень окисления +3.
№19 слайд


Содержание слайда: Физические свойства
Металл серебристо-белого цвета, легкий, плотность 2,7 г/см³, температура плавления у технического 658 °C, у алюминия высокой чистоты 660 °C, температура кипения 2500 °C, временное сопротивление литого 10-12 кг/мм², деформируемого 18-25 кг/мм2,сплавов 38-42 кг/мм².
Твердость по Бринеллю 24-32 кгс/мм², высокая пластичность: у технического 35 %, у чистого 50 %, прокатывается в тонкий лист и даже фольгу.
№20 слайд


Содержание слайда: Химические свойства
С простыми веществами:
1) С кислородом:
4Al0 + 3O2 → 2Al+32O3
2) С галогенами:
2Al0 + 3Br20 → 2Al+3Br3
3) С другими неметаллами (азотом, серой, углеродом) реагирует при нагревании:
2Al0 + 3S t°→ Al2+3S3(сульфид алюминия)
2Al0 + N2 t° → 2Al+3N(нитрид алюминия)
4Al0 + 3С → Al4+3С3(карбид алюминия)
Сульфид и карбид алюминия полностью гидролизуются:
Al2S3 + 6H2O → 2Al(OH)3¯ + 3H2S
Al4C3 + 12H2O → 4Al(OH)3¯+ 3CH4
№21 слайд


Содержание слайда: Со сложными веществами:
Со сложными веществами:
4) С водой (после удаления защитной оксидной пленки):
2Al0 + 6H2O ® 2Al+3(OH)3 + 3H2
5) Со щелочами:
2Al0 + 2NaOH + 6H2O ® 2Na[Al+3(OH)4]
(тетрагидроксоалюминат натрия) + 3H2
6) Легко растворяется в соляной и разбавленной серной киcлотах:
2Al + 6HCl ® 2AlCl3 + 3H2
2Al + 3H2SO4(разб) ® Al2(SO4)3 + 3H2
При нагревании растворяется в кислотах - окислителях:
2Al + 6H2SO4(конц) ® Al2(SO4)3 + 3SO2 + 6H2O
Al + 6HNO3(конц) ® Al(NO3)3 + 3NO2 + 3H2O
7) Восстанавливает металлы из их оксидов (алюминотермия):
8Al0 + 3Fe3O4 ® 4Al2O3 + 9Fe
2Al + Cr2O3 ® Al2O3 + 2Cr
№23 слайд


Содержание слайда: Применение
алюминия
— в электротехнике
— для производства легких сплавов (дюралюмин, силумин) в самолето- и автомобилестроении
— для алитирования чугунных и стальных изделий с целью повышения их коррозионной стойкости
— для термической сварки
— для получения редких металлов в свободном виде
— в строительной промышленности
— для изготовления контейнеров, фольги и т.п.
№26 слайд


Содержание слайда: Вставьте пропущенное слово:
Наиболее выраженные металлические свойства проявляет:
? алюминий
? натрий
? магний
? бериллий
? железо
Активнее других реагирует с кислородом....
? алюминий
? серебро
? цинк
? барий
При комнатной температуре вытесняет водород из воды...
? медь
? железо
? литий
? цинк
№27 слайд


Содержание слайда: Калий взаимодействует с водой с образованием.... и ....
Калий взаимодействует с водой с образованием.... и ....
? соли
? водорода
? щелочи
? оксида калия
В химических реакциях атом алюминия - ...
? окислитель
? восстановитель
? окислитель и восстановитель
? не отдает и не принимает электроны
Какой металл не используют для вытеснения менее активных металлов из растворов их солей?
? железо
? магний
? натрий
? цинк
№28 слайд


Содержание слайда: Решите задачи:
Задача № 1 При обработке 8г смеси магния и оксида магния соляной кислотой выделилось 5,6 л водорода(н.у.). Какова массовая доля (в %) магния в исходной смеси?
Задача № 2 Калий массой 3,9 г растворили в воде массой 206,2 г. Определите массовую долю полученного раствора.
Скачать все slide презентации Общая характеристика металлов главных подгрупп I-III одним архивом:
Похожие презентации
-
 Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода)
Общая характеристика элементов главной подгруппы VI группы (подгруппы кислорода) -
 ГОСУДАРСТВЕННЫЕ ЦЕННЫЕ БУМАГИ I. Общая характеристика II. Виды государственных ценных бумаг III. Ценные бумаги региональных ор
ГОСУДАРСТВЕННЫЕ ЦЕННЫЕ БУМАГИ I. Общая характеристика II. Виды государственных ценных бумаг III. Ценные бумаги региональных ор -
 Общая характеристика неметаллов
Общая характеристика неметаллов -
 Ацтеки Общая характеристика
Ацтеки Общая характеристика -
 ГЕОГРАФИЯ ОТРАСЛЕЙ ПРОМЫШЛЕННОСТИ 10 класс Урок к разделу I «Общая характеристика мира» по учебнику В. П. Максаковского «Экономи
ГЕОГРАФИЯ ОТРАСЛЕЙ ПРОМЫШЛЕННОСТИ 10 класс Урок к разделу I «Общая характеристика мира» по учебнику В. П. Максаковского «Экономи -
 "Общая характеристика институционального направления" - скачать презентации по Экономике
"Общая характеристика институционального направления" - скачать презентации по Экономике -
 Общая характеристика профессионально-педагогической специальности
Общая характеристика профессионально-педагогической специальности -
 Образование как общественное явление и педагогический процесс. Общая характеристика пед. профессии Модуль 1. Учебный элемент 1. 2.
Образование как общественное явление и педагогический процесс. Общая характеристика пед. профессии Модуль 1. Учебный элемент 1. 2. -
 Искусство древней Греции Общая характеристика культуры и искусства древней Греции
Искусство древней Греции Общая характеристика культуры и искусства древней Греции -
 Классическая политическая экономия. Общая характеристика и этапы развития. А. Смит и Д. Рикардо ЛЕКЦИЯ 26
Классическая политическая экономия. Общая характеристика и этапы развития. А. Смит и Д. Рикардо ЛЕКЦИЯ 26