Презентация Фотометрические методы биохимического анализа онлайн
На нашем сайте вы можете скачать и просмотреть онлайн доклад-презентацию на тему Фотометрические методы биохимического анализа абсолютно бесплатно. Урок-презентация на эту тему содержит всего 64 слайда. Все материалы созданы в программе PowerPoint и имеют формат ppt или же pptx. Материалы и темы для презентаций взяты из открытых источников и загружены их авторами, за качество и достоверность информации в них администрация сайта не отвечает, все права принадлежат их создателям. Если вы нашли то, что искали, отблагодарите авторов - поделитесь ссылкой в социальных сетях, а наш сайт добавьте в закладки.
Презентации » Физика » Фотометрические методы биохимического анализа
Оцените!
Оцените презентацию от 1 до 5 баллов!
- Тип файла:ppt / pptx (powerpoint)
- Всего слайдов:64 слайда
- Для класса:1,2,3,4,5,6,7,8,9,10,11
- Размер файла:11.07 MB
- Просмотров:174
- Скачиваний:0
- Автор:неизвестен
Слайды и текст к этой презентации:
№3 слайд


Содержание слайда: Методы сравнения стандартного и опытного образца
Анализируемая и стандартная проба обрабатываются в одинаковых условиях
При больших сериях – стандартную пробу исследовать в начале серии и через каждые 20 проб
Расчет ведут по ствндарту или по фактору
Расчет по стандарту: Сi = Di х Cст/Dст
Расчет по фактору: С = D х F
№5 слайд


Содержание слайда: Методы определения без использования калибратора
Определение концентрации по молярному показателю поглощения – применение закона Бургера
С = D/lхξ (концентрация определяется делением измеренной оптической плотности на известный для данного вещества молярный показатель поглощения при длине волны измерения: С = D/ξ)
Учитывать разведение образца
№13 слайд


Содержание слайда: Измерение по конечной точке
Реакция развивается за некоторый период времени и достигает определенного конечного состояния (конечная точка)
При измерении по конечной точке уровень сигнала соответствует количеству продуктов реакции в инкубационной среде после фиксированного времени инкубации
Поглощение измеряется после окончания реакции при стабильном значении сигнала
№14 слайд
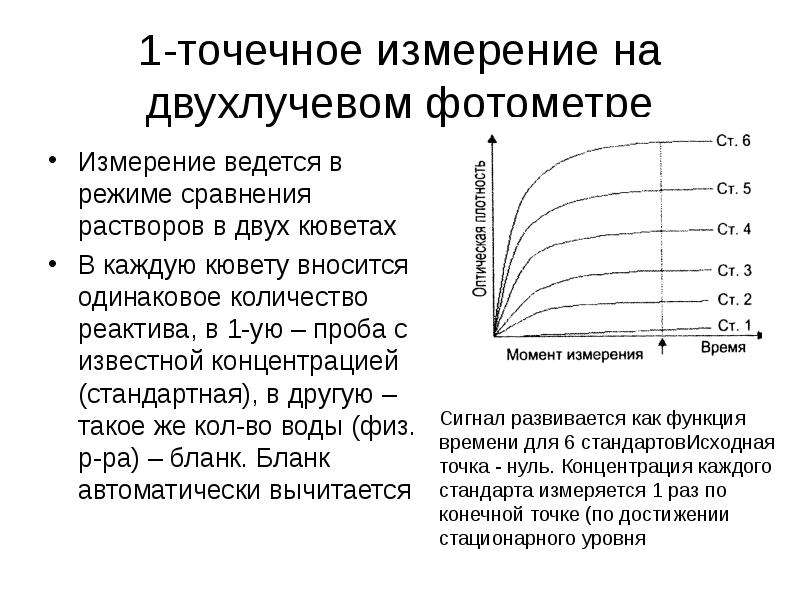

Содержание слайда: 1-точечное измерение на двухлучевом фотометре
Измерение ведется в режиме сравнения растворов в двух кюветах
В каждую кювету вносится одинаковое количество реактива, в 1-ую – проба с известной концентрацией (стандартная), в другую – такое же кол-во воды (физ. р-ра) – бланк. Бланк автоматически вычитается
№15 слайд


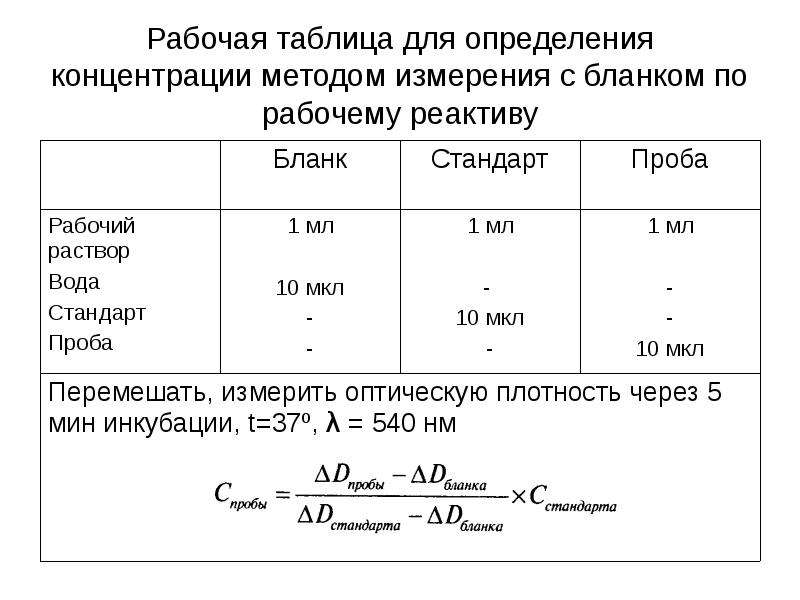
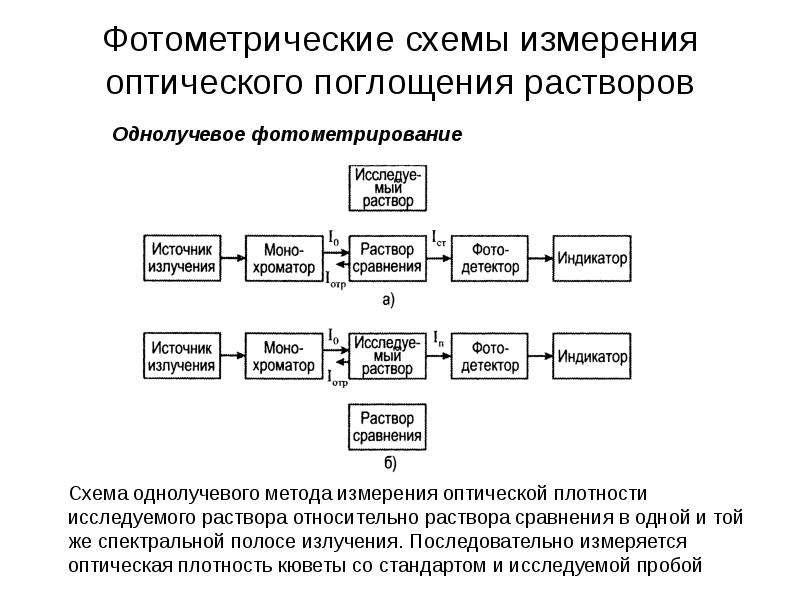
Содержание слайда: Измерение с бланком на однолучевом фотометре
Для исключения систематического влияния (рабочий реактив, отражение от стенок кювет, темновой ток) используют измерение относительно холостой пробы (бланка)
Бланк определяют по рабочему реактиву перед измерением пробы
Dпробы = Dконечной точки – Dбланка
Процедура сходна с одноточечным измерением, но учет бланка проводится в ручном режиме
№17 слайд


Содержание слайда: Измерение с прозоной
Разновидность измерения с бланком
Измерение в одной кювете, отсутствует кювета сравнения
Проводят определение до прибавления биопробы
Характерен для биохимических анализаторов (двухточечное измерение с прозоной)
Прозона – временной период до добавления в кювету пробы.
При добавлении нескольких реактивов прозона определяется при достижении стабильного состояния после внесения всех реактивов перед пробой
№18 слайд
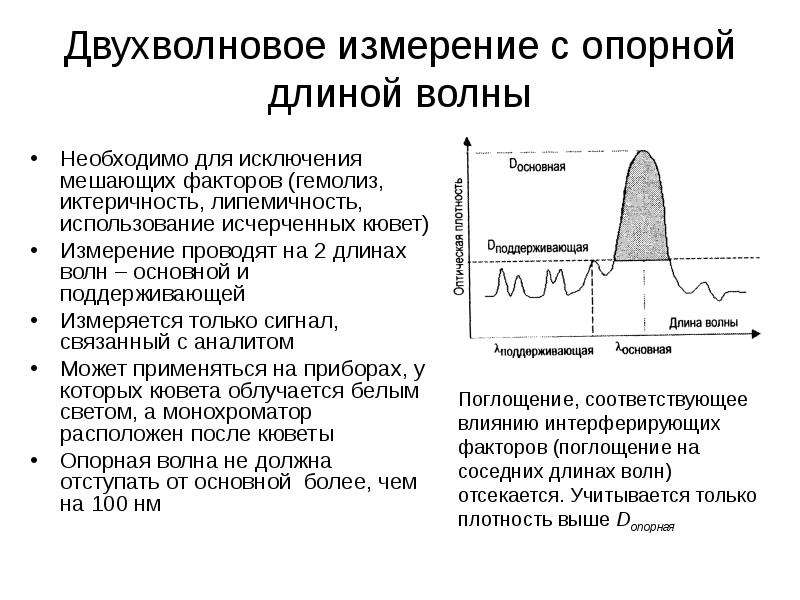

Содержание слайда: Двухволновое измерение с опорной длиной волны
Необходимо для исключения мешающих факторов (гемолиз, иктеричность, липемичность, использование исчерченных кювет)
Измерение проводят на 2 длинах волн – основной и поддерживающей
Измеряется только сигнал, связанный с аналитом
Может применяться на приборах, у которых кювета облучается белым светом, а монохроматор расположен после кюветы
Опорная волна не должна отступать от основной более, чем на 100 нм
№19 слайд


Содержание слайда: Принцип получения информации о степени иктеричности, липемичности и гемолиза сывортки
20 мкл сыворотки, смешать с 200 мкл дистиллированной воды, добавить 600 мкл 0,15 М фосфатный буфер (рН = 7,4)
Раствор измеряется при длинах волн 460, 500, 576, 597, и 750 нм Вычисляются
∆D 460/500 (разность плотностей) (иктеричность)
∆D 576/597 (разность плотностей) (гемолитичность)
∆D 597/750 (разность плотностей) (липемичность)
№21 слайд


Содержание слайда: Кинетические измерения
Определение меняющейся в ходе реакции оптической плотности
Широко используется для определения активности ферментов
Требует точного поддержания температуры в измерительной кювете (+ 0,1º С), правильного отсчета временных интервалов
Условия обязательны, доступны только при использовании современных фотометров и биохимических анализаторов
№24 слайд


Содержание слайда: Измерение по двум точкам
При постоянной скорости кинетической реакции измерение можно проводить на любом отрезкелинейной кривой, приводя поглощение к 1 мин.
Достоинства – простота, возможность измерения без стандарта, независимость в пределах линейного диапазона.
Допустим при повторном использовании разовых кювет
Следует убедиться что измерение проводится в линейном диапазоне
№25 слайд
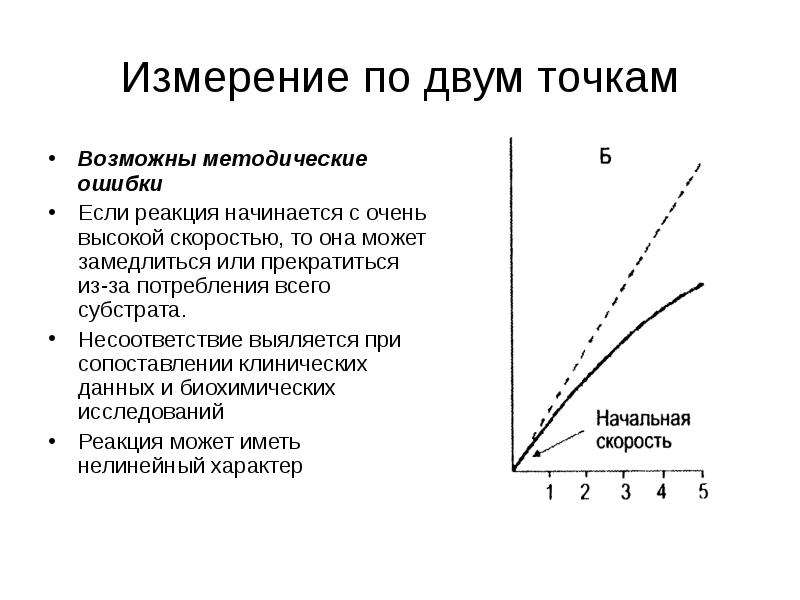

Содержание слайда: Измерение по двум точкам
Возможны методические ошибки
Если реакция начинается с очень высокой скоростью, то она может замедлиться или прекратиться из-за потребления всего субстрата.
Несоответствие выяляется при сопоставлении клинических данных и биохимических исследований
Реакция может иметь нелинейный характер
№26 слайд
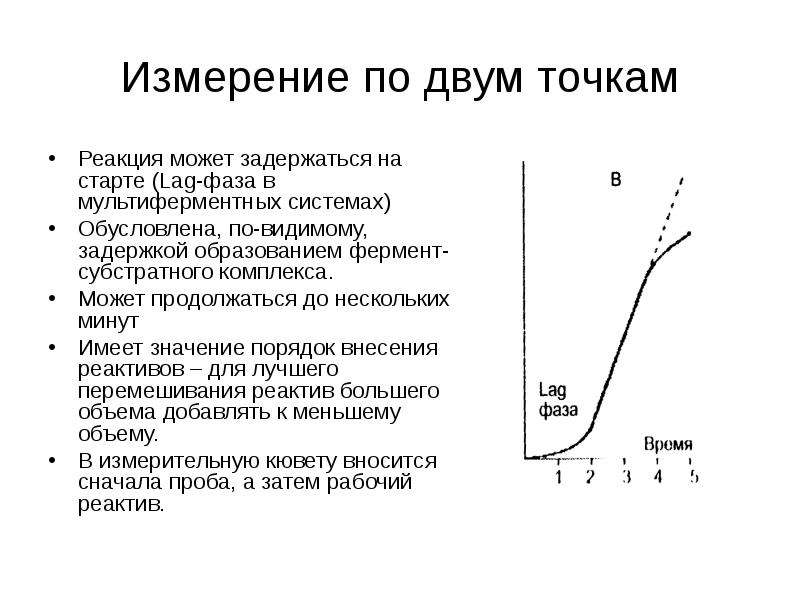

Содержание слайда: Измерение по двум точкам
Реакция может задержаться на старте (Lag-фаза в мультиферментных системах)
Обусловлена, по-видимому, задержкой образованием фермент-субстратного комплекса.
Может продолжаться до нескольких минут
Имеет значение порядок внесения реактивов – для лучшего перемешивания реактив большего объема добавлять к меньшему объему.
В измерительную кювету вносится сначала проба, а затем рабочий реактив.
№27 слайд


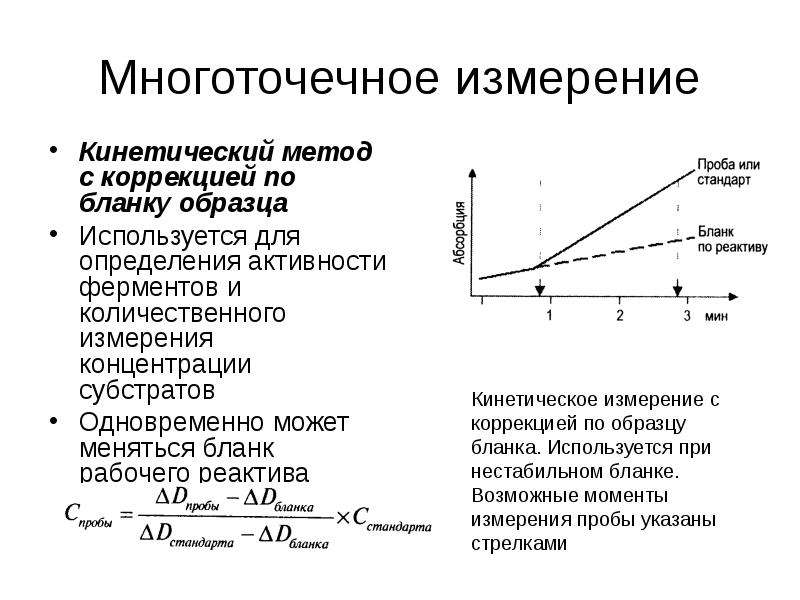
Содержание слайда: Многоточечное измерение
Позволяет оценивать характер кинетики и выбирать для расчетов линейный участок
Является наиболее точным методом определения активности ферментов
Изменение оптического поглощения должно быть одинаковым за равные промежутки времени (отклонение от линейности не должно превышать 10%)
№28 слайд
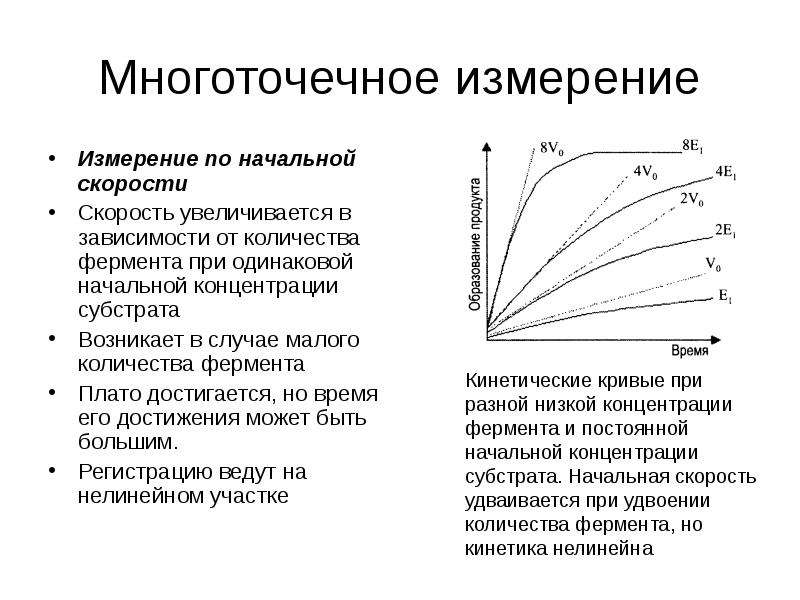

Содержание слайда: Многоточечное измерение
Измерение по начальной скорости
Скорость увеличивается в зависимости от количества фермента при одинаковой начальной концентрации субстрата
Возникает в случае малого количества фермента
Плато достигается, но время его достижения может быть большим.
Регистрацию ведут на нелинейном участке
№29 слайд
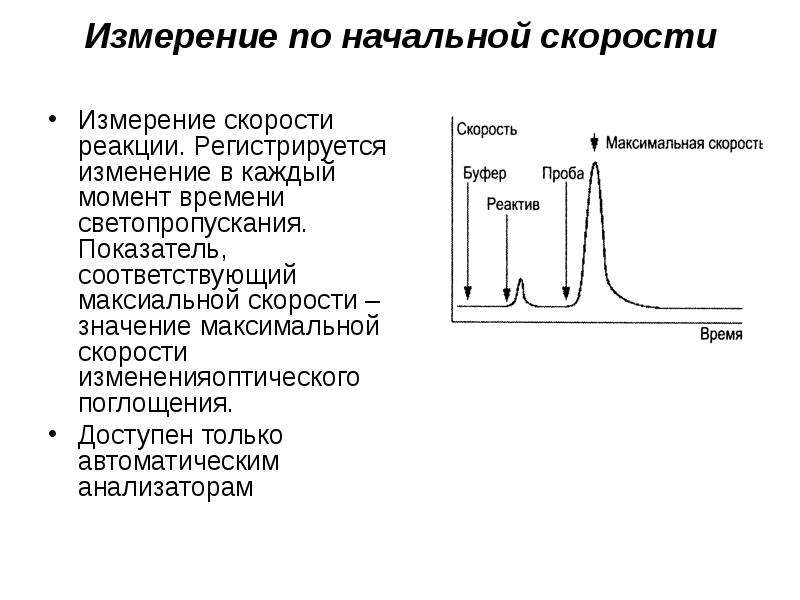

Содержание слайда: Измерение по начальной скорости
Измерение скорости реакции. Регистрируется изменение в каждый момент времени светопропускания. Показатель, соответствующий максиальной скорости – значение максимальной скорости измененияоптического поглощения.
Доступен только автоматическим анализаторам
№31 слайд


Содержание слайда: Современные приборы способны определять и отслеживать избыток антигенов автоматически (регистрация ускорения реакции после добавления дополнительного количества антигена –малые дозы калибратора)
При постановке на обычном фотометре необходимо знать диагноз. Избыток антигена наблюдается в чрезвычайной ситуации. При миеломной болезни концентрация IgG может быть очень высокой, и исследование попадает в зону избытка антигена. Необходимо электрофоретическое исследование
В качестве стандартов и контрольных материалов необходимо использовать стандарты и сыворотки, содержащие индивидуальные белки, концентрация которых измерена с использованием иммунохимической реакции
№40 слайд


Содержание слайда: Рассеяние света
Трансмиссия и рассеивание зависят от
- длины волны светового потока
- частоты светового потока
- интенсивности светового потока
- свойств рассеивающей среды (размера и формы частиц, количества, способности к поляризации и др)
Если в процессе измерения размер частиц в растворе меняется, будет меняться поток проходящего и рассеивающего света
№43 слайд


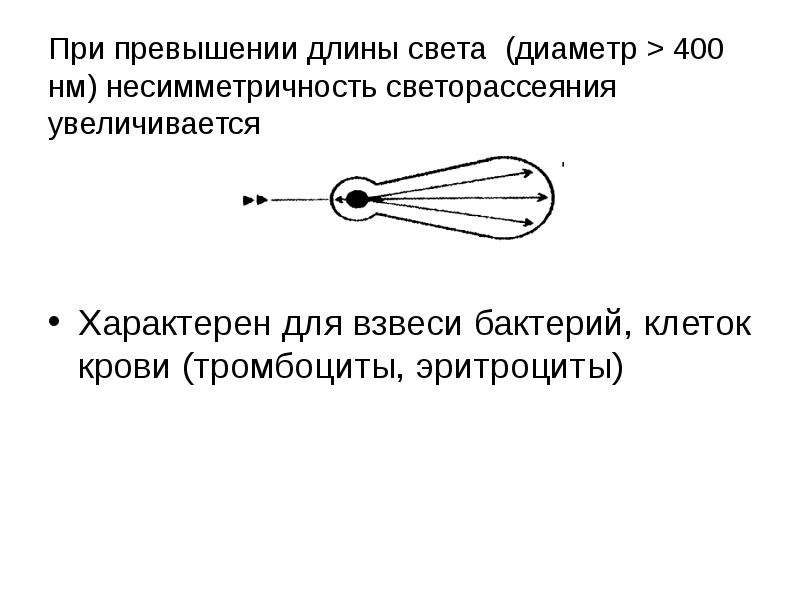
Содержание слайда: В основе рассеяния малых частиц лежит явление дифракции
Рассеяние света каждой частицей не зависит друг от друга.
Рассеянный свет распространяется во всех направлениях
Максимальное количество света рассеивается под углом 0 и 180º
При λ 400нм – такой тип рассеивания характерен для частиц диаметром < 40 нм (иммуноглобулины,β- липопротеины, альбумин)
№49 слайд


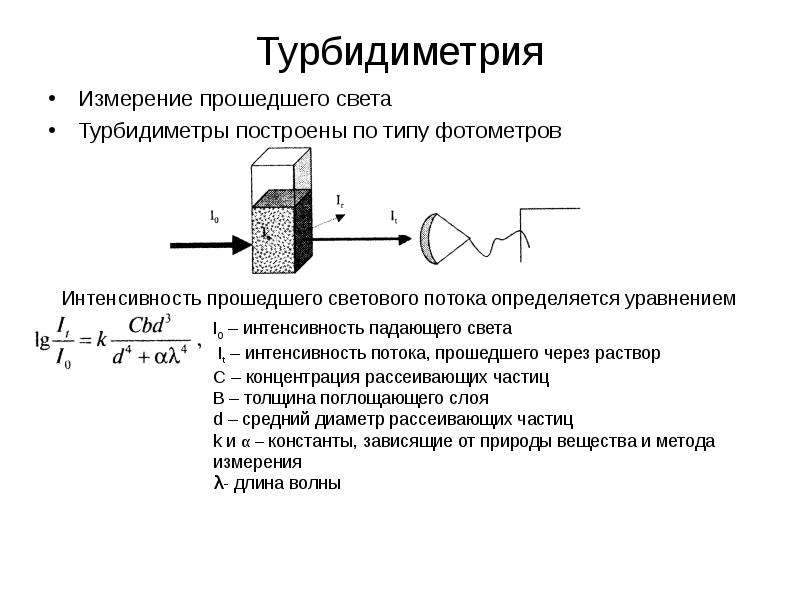
Содержание слайда: Турбидиметрия
Выражение, подобное закону Бугера-Ламберта для окрашенных растворов
t – молярный коэффициент мутности раствора (турбидность)
В качестве турбидиметров можно использовать большинство фотометров и биохимических анализаторов
Обычно используются короткие волны (340 нм), т.к. доля рассеянного света увеличивается обратно пропорционально четвертой степени длины волны – т.е. при меньшей длине волны прошедший свет будет составлять большую часть от падающего, для более короткого ультрафиолета нужна специальная оптика
№55 слайд
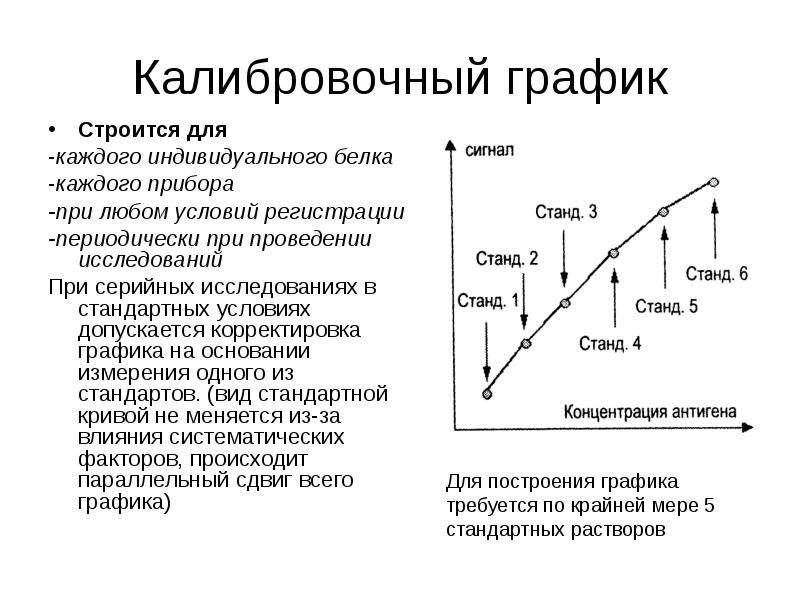

Содержание слайда: Калибровочный график
Строится для
-каждого индивидуального белка
-каждого прибора
-при любом условий регистрации
-периодически при проведении исследований
При серийных исследованиях в стандартных условиях допускается корректировка графика на основании измерения одного из стандартов. (вид стандартной кривой не меняется из-за влияния систематических факторов, происходит параллельный сдвиг всего графика)
№56 слайд


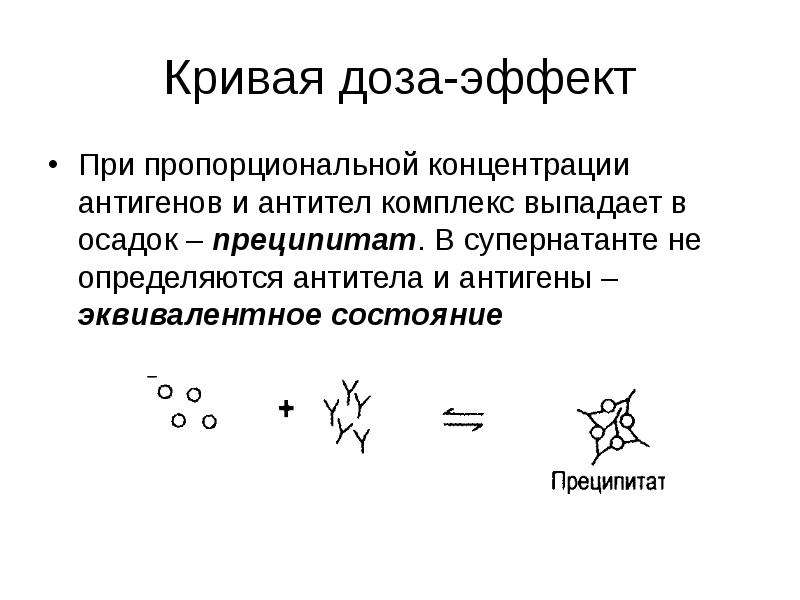
Содержание слайда: Состав реакционной смеси подбирается так, чтобы измерение производилось в зоне избытка антител.
При очень высокой концентрации белка антител недостаточно, частицы преципитата становятся мелкими (нисходящая часть кривой) – с увеличением концентрации белка сигнал прибора уменьшается. Может быть выдан неправильный результат.
Проводят разведение биологической жидкости
Если сигнал увеличивается – определение проводилось в нисходящей части кривой
Разведение проводят до степени избытка антител
№57 слайд


Содержание слайда: Современные приборы способны определять и отслеживать избыток антигенов автоматически (регистрация ускорения реакции после добавления дополнительного количества антигена –малые дозы калибратора)
При постановке на обычном фотометре необходимо знать диагноз. Избыток антигена наблюдается в чрезвычайной ситуации. При миеломной болезни концентрация IgG может быть очень высокой, и исследование попадает в зону избытка антигена. Необходимо электрофоретическое исследование
В качестве стандартов и контрольных материалов необходимо использовать стандарты и сыворотки, содержащие индивидуальные белки, концентрация которых измерена с использованием иммунохимической реакции
Скачать все slide презентации Фотометрические методы биохимического анализа одним архивом:
Похожие презентации
-
 Фотометрические методы биохимического анализа. Турбидиметрия и нефелометрия
Фотометрические методы биохимического анализа. Турбидиметрия и нефелометрия -
 По физике "Спектральные методы анализа" - скачать
По физике "Спектральные методы анализа" - скачать -
 Методы анализа лекарственных средств
Методы анализа лекарственных средств -
 Фотометрия. Приборы для фотометрического анализа
Фотометрия. Приборы для фотометрического анализа -
 Оптические методы анализа. Введение. Рефрактометрический анализ
Оптические методы анализа. Введение. Рефрактометрический анализ -
 Роль физико-химических методов анализа потребительских товаров при установлении их безопасности и качества
Роль физико-химических методов анализа потребительских товаров при установлении их безопасности и качества -
 Анализ качества шоколада методом рентгеновской дифракции
Анализ качества шоколада методом рентгеновской дифракции -
 Методы люминисцентного анализа
Методы люминисцентного анализа -
 Спектроскопические методы анализа
Спектроскопические методы анализа -
 Фотометрия. Спектрофотометрический метод. Фотометрический метод. Метод визуальной колориметрии
Фотометрия. Спектрофотометрический метод. Фотометрический метод. Метод визуальной колориметрии