Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
21 слайд
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
235.50 kB
Просмотров:
241
Скачиваний:
1
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Глава 27. Теория атома водорода по Бору
Большую роль в развитии атомистической теории сыграл Д. И. Менделеев, разработавший в 1869 г. Периодическую систему элементов, в которой впервые на научной основе был поставлен вопрос о единой природе атомов.
Во второй половине XIX в. экспериментально было доказано, что электрон является одной из основных составных частей любого вещества.
Эти выводы, а также многочисленные экспериментальные данные привели к тому, что в начале XX в. серьезно встал вопрос о строении атома.
№2 слайд
Содержание слайда: Модель атома Дж. Дж. Томсона (1903)
Согласно этой модели, атом представляет собой непрерывно заряженный положительным зарядом шар радиусом порядка 10-10м, внутри которого около своих положений равновесия колеблются электроны.
Суммарный отрицательный заряд электронов равен положительному заряду шара, поэтому атом в целом нейтрален.
№3 слайд
Содержание слайда: Ядерная (планетарная) модель атома Резерфорда (1911)
Согласно этой модели,
вокруг положительного ядра, имеющего заряд Ze (Z — порядковый номер элемента в системе Менделеева, е — элементарный заряд), размер 10-15 — 10-14 м и массу, практически равную массе атома,
в области с линейными размерами порядка 10-10 м по замкнутым орбитам движутся электроны, образуя электронную оболочку атома.
Так как атомы нейтральны, то заряд ядра равен суммарному заряду электронов, т. е. вокруг ядра должно вращаться Z электронов.
№4 слайд
Содержание слайда: Второй закон Ньютона для электрона, движущегося по окружности под действием кулоновской силы, имеет вид
Уравнение (208.1) содержит два неизвестных: r и v. Следовательно, существует бесчисленное множество значений радиуса и соответствующих ему значений скорости (а значит, и энергии), удовлетворяющих этому уравнению. Поэтому величины r, v (следовательно, и Е) могут меняться непрерывно, т. е. может испускаться любая, а не вполне определенная порция энергии.
Тогда спектры атомов должны быть сплошными.
В действительности же опыт показывает, что атомы имеют линейчатый спектр.
№5 слайд
Содержание слайда: Из выражения (208.1) следует, что при r 10-10 м скорость движения электронов v 106 м/с, а ускорение v2/r = 1022 м/с2.
Согласно электродинамике, ускоренно движущиеся электроны должны излучать электромагнитные волны и вследствие этого непрерывно терять энергию. В результате электроны будут приближаться к ядру и в конце концов упадут на него. Таким образом, атом Резерфорда оказывается неустойчивой системой, что опять-таки противоречит действительности.
Преодоление возникших трудностей потребовало создания качественно новой — квантовой — теории атома.
№6 слайд
Содержание слайда: § 209. Линейчатый спектр атома водорода
Швейцарский ученый И. Бальмер (1825—1898) подобрал эмпирическую формулу, описывающую все известные в то время спектральные линии атома водорода в видимой области спектра:
№7 слайд
Содержание слайда: В дальнейшем (в начале XX в.) в спектре атома водорода было обнаружено еще несколько серий.
В ультрафиолетовой области спектра находится серия Лаймана:
№8 слайд
Содержание слайда: В инфракрасной области спектра были также обнаружены:
серия Пашена
серия Брэкета
серия Пфунда
серия Хэмфри
№9 слайд
Содержание слайда: Все приведенные выше серии в спектре атома водорода могут быть описаны одной формулой, называемой обобщенной формулой Бальмера:
m имеет в каждой данной серии постоянное значение, m = 1, 2, 3, 4, 5, 6 (определяет серию), n принимает целочисленные значения начиная с m + 1 (определяет отдельные линии этой серии)
№10 слайд
Содержание слайда: § 210. Постулаты Бора
Первый постулат Бора (постулат стационарных состояний):
в атоме существуют стационарные (не изменяющиеся со временем) состояния, в которых он не излучает энергии. Стационарным состояниям атома соответствуют стационарные орбиты, по которым движутся электроны. Движение электронов по стационарным орбитам не сопровождается излучением электромагнитных волн.
В стационарном состоянии атома электрон, двигаясь по круговой орбите, должен иметь дискретные квантованные значения момента импульса, удовлетворяющие условию
(210.1)
№11 слайд
Содержание слайда: Второй постулат Бора (правило частот):
при переходе электрона с одной стационарной орбиты на другую излучается (поглощается) один фотон с энергией равной разности энергий соответствующих стационарных состояний ( до и после излучения).
(210.2)
при < происходит излучение фотона, в противном случае – поглощение фотона.
Набор возможных дискретных частот
= ( — )/h квантовых переходов и определяет линейчатый спектр атома.
№12 слайд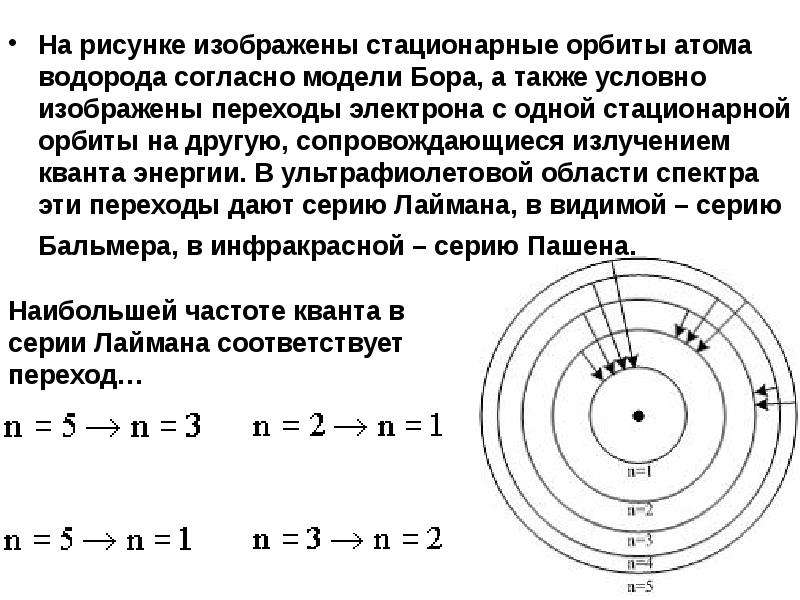
Содержание слайда: На рисунке изображены стационарные орбиты атома водорода согласно модели Бора, а также условно изображены переходы электрона с одной стационарной орбиты на другую, сопровождающиеся излучением кванта энергии. В ультрафиолетовой области спектра эти переходы дают серию Лаймана, в видимой – серию Бальмера, в инфракрасной – серию Пашена.
№13 слайд
Содержание слайда: § 211. Опыты Франка и Герца
Немецкие физики Д. Франк и Г. Герц, изучая столкновения электронов с атомами газов (1913), экспериментально доказали дискретность значений энергии атомов.
Опыты Франка и Герца показали, что электроны при столкновении с атомами передают им только определенные порции энергии.
Следовательно, идея Бора о существовании в атомах стационарных состояний блестяще выдержала экспериментальную проверку.
№14 слайд
Содержание слайда: § 212. Спектр атома водорода по Бору
Постулаты, выдвинутые Бором, позволили рассчитать спектр атома водорода и водородоподобных систем — систем, состоящих из ядра с зарядом Ze и одного электрона (например, ионы Не+, Li2+), а также теоретически вычислить постоянную Ридберга.
Решая совместно уравнение (208.1) и уравнение (210.1), получим выражение для радиуса n-й стационарной орбиты:
№15 слайд
Содержание слайда: Для атома водорода (Z = l) радиус первой орбиты электрона при n = 1, называемый первым боровским радиусом (а), равен
(212.2)
№16 слайд
Содержание слайда: Учитывая квантованные для радиуса n-й стационарной орбиты значения (212.1), получим, что энергия электрона может принимать только следующие дозволенные дискретные значения:
№17 слайд
Содержание слайда: Целое число n в выражении (212.3), определяющее энергетические уровни атома, называется главным квантовым числом.
Энергетическое состояние с n = 1 является основным (нормальным) состоянием;
состояния с n > 1 являются возбужденными.
Энергетический уровень, соответствующий основному состоянию атома, называется основным (нормальным) уровнем;
все остальные уровни являются возбужденными.
Атом водорода обладает, таким образом, минимальной энергией (E1 = –13,55 эВ) при n = 1 и максимальной ( = 0) при n = ∞ (при удалении электрона из атома). Следовательно, значение = 0 соответствует ионизации атома (отрыву от него электрона).
№18 слайд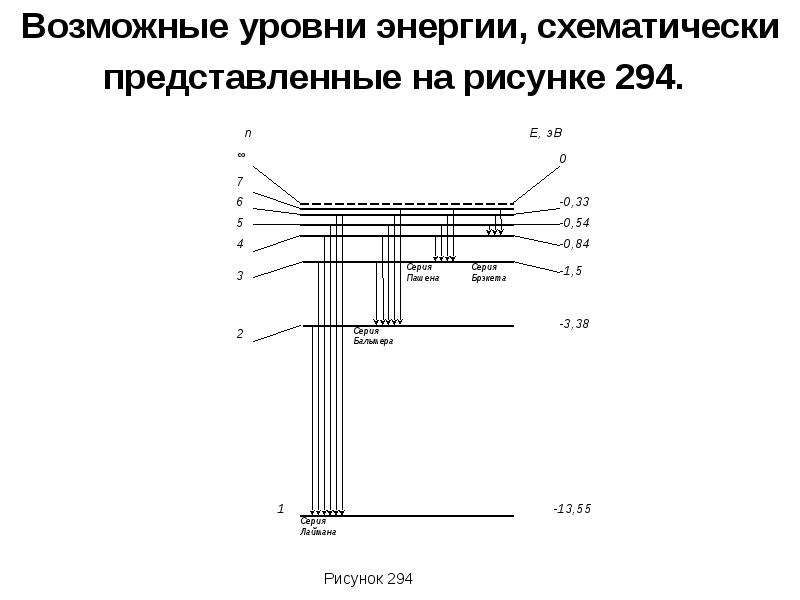
Содержание слайда: Возможные уровни энергии, схематически представленные на рисунке 294.
№19 слайд
Содержание слайда: Согласно второму постулату Бора (см. (210.2)), при переходе атома водорода (Z = l) из стационарного состояния n с большей энергией в стационарное состояние m с меньшей энергией испускается квант
№20 слайд
Содержание слайда: Спектр поглощения атома водорода является линейчатым, но содержит только серию Лаймана.
Он также объясняется теорией Бора. Так как свободные атомы водорода обычно находятся в основном состоянии (стационарное состояние с наименьшей энергией при n = 1), то при сообщении атомам извне определенной энергии могут наблюдаться лишь переходы атомов из основного состояния в возбужденные (возникает серия Лаймана).
Теория Бора была крупным шагом в развитии атомной физики и явилась важным этапом в создании квантовой механики.
№21 слайд
Содержание слайда: Однако теория Бора обладает внутренними противоречиями (с одной стороны, применяет законы классической физики, а с другой — основывается на квантовых постулатах). Она рассмотрела спектры атома водорода и водородоподобных систем и вычислила частоты спектральных линий, однако не смогла объяснить их интенсивности и ответить на вопрос: почему совершаются те или иные переходы?
Серьезным недостатком теории Бора была невозможность описания с ее помощью спектра атома гелия — одного из простейших атомов, непосредственно следующего за атомом водорода.






























