Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
25 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
4.78 MB
Просмотров:
118
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Первый закон термодинамики
Закон сохранения энергии для тепловых процессов
№2 слайд
Содержание слайда: Что надо выяснить:
Выполнение закона сохранения энергии в тепловых процессах.
Как применить закон сохранения энергии к изопроцессам.
Что такое адиабатный процесс.
Роль ученых в открытии закона сохранения энергии.
№3 слайд
Содержание слайда: Способы изменения внутренней энергии
№4 слайд
Содержание слайда: Первый закон термодинамики
Авн- работа внешних сил
Q-количество теплоты
∆ U-изменение внутренней энергии
№5 слайд
Содержание слайда: В изолированной системе
Изолированная система не обменивается теплотой с окружающими телами(Q=0).
Над ней не совершается работа внешними силами(Авн = 0)
№6 слайд
Содержание слайда: Работа, совершаемая газом, и первый закон термодинамики
∆ U = Q + Авн; Авн= Fвнh, F' = -Fвн,
значит Авн= - А', сл-но: (A‘=А, F‘= F)
№7 слайд
Содержание слайда: Первый закон термодинамики для изопроцессов
Изохорный процесс
Изотермический процесс
Изобарный процесс
Адиабатный процесс
№8 слайд
Содержание слайда: Изохорный процесс
(V = const)
∆V=0, поэтому
газ работы не совершает
т.е. А = 0.
Q = ∆U
∆U = U2 –U1;
U2 = imRT2/2M;
U1= imRT1/2M;
№9 слайд
Содержание слайда: Применение первого закона термодинамики (V=сonst)
№10 слайд
Содержание слайда: Изотермический процесс
(T = const)
∆T = 0, следовательно,
внутренняя энергия
не изменяется: ∆U = 0.
Q =A.
№11 слайд
Содержание слайда: Применение первого закона термодинамики (T = const)
№12 слайд
Содержание слайда: Изобарный процесс
(p = const)
При изобарном расширении газа подведённое к нему количество теплоты расходуется как на увеличение его внутренней энергии, так и на совершение работы газом.
Для изобарного расширения газа, при котором увеличивается его температура, требуется большее количество теплоты, чем при изотермическом процессе, где температура газа не меняется.
№13 слайд
Содержание слайда: Применение первого закона термодинамики (p = const)
№14 слайд
Содержание слайда: Адиабатный процесс
Теплоизолированная система – это система, не обменивающаяся энергией с окружающими телами.
Адиабатный процесс – термодинамический процесс в теплоизолированной системе.
Q = 0
№15 слайд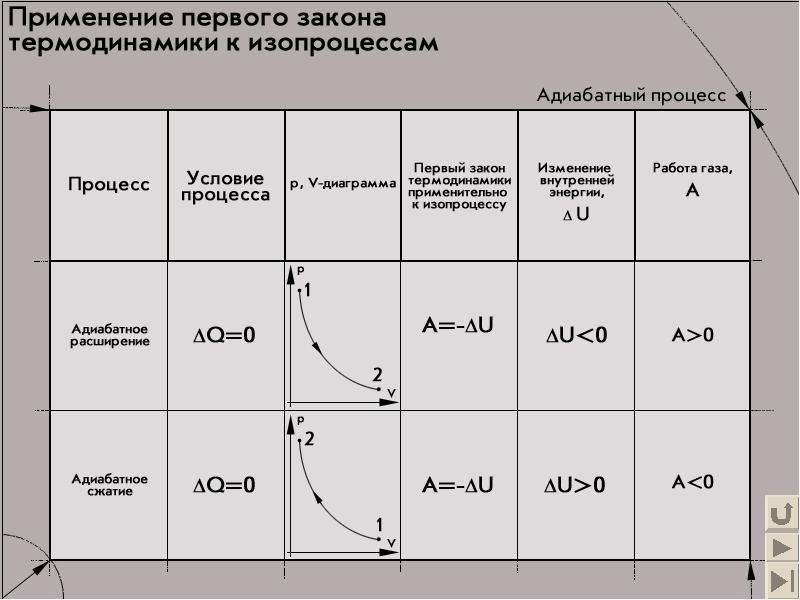
Содержание слайда: Применение первого закона термодинамики (∆Q)
№16 слайд
Содержание слайда: Адиабатные процессы в природе
Образование облаков.
Осадки.
№17 слайд
Содержание слайда: Образование облаков
№18 слайд
Содержание слайда: Осадки
№19 слайд
Содержание слайда: Из истории открытия первого закона термодинамики
Роберт Юлиус Майер
Джеймс Прескотт Джоуль
Герман Гельмгольц
Эмиль Христианович Ленц
№20 слайд
Содержание слайда: Роберт Юлиус Майер
Майер по профессии врач, работал некоторое время судовым врачом. Однажды штурман сказал ему, что во время сильной бури вода нагревается. Майер занес замечание штурмана в свой дневник и впоследствии проверил его (наши восьмиклассники тоже проверяли, а вы сможете это сделать?).
В порту у берегов Явы он заметил, что кровь матросов значительно светлее венозной крови жителей умеренных поясов. Местные врачи объяснили, что такой цвет крови - обычное явление для этих мест.
Роберт Майер установил количественное соотношение между теплотой и работой и первый вычислил значение механического эквивалента тепла.
№21 слайд
Содержание слайда: Джеймс Прескотт Джоуль
№22 слайд
Содержание слайда: Герман Гельмгольц
№23 слайд
Содержание слайда: Эмиль Христианович Ленц
В1820 году поступил в университет, в1823 – 1826г.г. в должности физика принимал участие в кругосветной экспедиции.
При изучении теплового действия тока Ленц открыл независимо от Джоуля закон, который носит теперь имя Джоуля – Ленца.
Свой результат Ленц получил раньше Джоуля, метод был более совершенным, результаты более точными, однако публикация Джоуля опередила публикацию Ленца.
№24 слайд
Содержание слайда: Вопросы по теме
«Первый закон термодинамики»
В чём заключается смысл закона сохранения энергии?
К каким системам применим закон сохранения энергии?
Как формулируется первый закон термодинамики?
В каких системах применим первый закон термодинамики?
Что является доказательством справедливости первого закона термодинамики?
Как найти работу при изобарном расширении?
Как можно сравнить работу, совершенную газом в различных процессах?
Почему работа газа при его сжатии отрицательна?
Почему работа газа в круговом процессе не равна нулю?
Как изменяется внутренняя энергия газа при изотермическом процессе?
Какая связь между изменением внутренней энергии идеального газа и переданным ему количеством теплоты при изохорном процессе?
Как изменяется внутренняя энергия идеального газа при изобарном сжатии?
Какой процесс изменения состояния газа называется адиабатным? Как этот процесс может быть осуществлён?
Как изменяется при этом температура газа?
№25 слайд
Содержание слайда: Информационные материалы:
Дягилев Ф.М. Из истории физики и жизни её творцов.- М.: Просвещение, 1986.
Блудов М.И. Беседы по физике. ч.1.- М. Просвещение, 1972.
Мощанский В.Н. История физики в средней школе.- М.: Просвещение,1981.
Касьянов В.А. Физика 10.- М.: Дрофа, 2000.
Физика 10. Под редакцией А.А. Пинского.- М.: Просвещение, 2001.
Microsoft Office 2000: Использование Microsoft Office в школе. Учебно – методическое пособие для учителей.
Виртуальная школа Кирилла и Мефодия, 2003.