Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
9 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
163.50 kB
Просмотров:
137
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Теория нормального горения
Лекция 5 по теории горения и взрыва ДБЖ-09
№2 слайд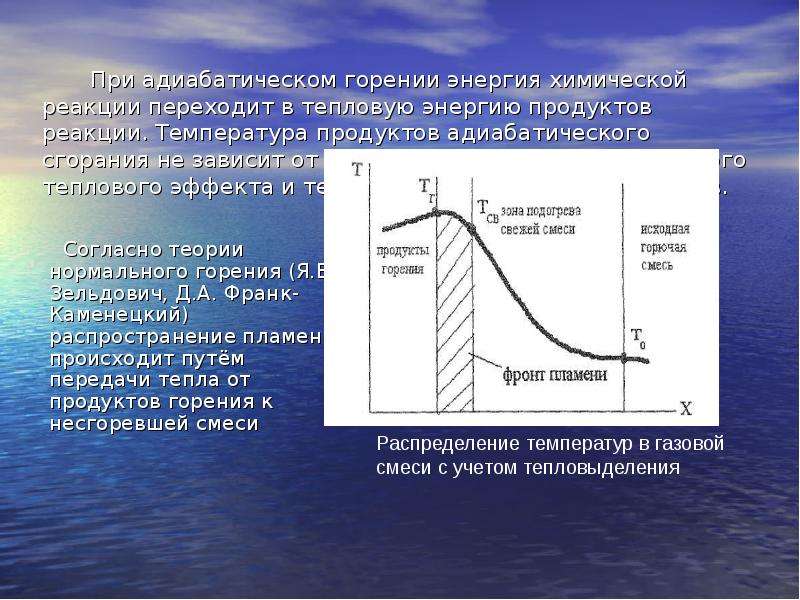
Содержание слайда: При адиабатическом горении энергия химической реакции переходит в тепловую энергию продуктов реакции. Температура продуктов адиабатического сгорания не зависит от скорости реакции, а от суммарного теплового эффекта и теплоёмкости конечных продуктов.
Согласно теории нормального горения (Я.Б. Зельдович, Д.А. Франк-Каменецкий) распространение пламени происходит путём передачи тепла от продуктов горения к несгоревшей смеси
№3 слайд
Содержание слайда: Химическая реакция сосредоточена в узкой зоне и уравнение теплопроводности в зоне подогрева выглядит:
с·ρ·dT/dt=η·d2T/dx2
μ=η/(с·ρ)
Скорость горения:
U·dt/dx=μ·d2T/dx2
Адиабатическая температура горения:
Т=Т0+(TВ-Т0)·e-U·x/μ
Температура воспламенения горючего вещества:
(ТВ-Т0)/(Т-Т0)=e-U·x/μ
№4 слайд
Содержание слайда: Важной характеристикой является зона прогрева и толщина прогрева: если зона прогрева и зона химической, то U·x/μ=1; x=μ/U
толщина зоны прогрева обратно пропорциональна скорости горения, если скорость горения 0,1/с, то толщина зоны прогрева равна 10-2 см, а если скорость горения 10 м/с, а толщина зоны прогрева 10-4 см
Толщина зоны прогрева зависит от времени протекания химической реакции: x=U·t
t – время протекания химической реакции
тогда скорость горения
U=√μ·Ф/t
№5 слайд
Содержание слайда: Тепломассообмен при горении
Количество тепла подводимого путем теплопроводности описывается уравнением: Q=λ·(T-T0)·δ
λ – коэффициент теплопроводности; δ – ширина фронта пламени.
Тепло расходуемое на нагрев свежей смеси от Т0 до Т
Q=U·c·ρ(T-T0)
с – удельная теплоемкость; ρ – плотность смеси.
Скорость распространения пламени, при условии равенства скорости подачи газа: U=λ/c·ρ·δ
Коэффициент температуропроводности
a=λ/c·ρ
№6 слайд
Содержание слайда: Согласно кинетической теории газов время химической реакции:
t=λ·γ/c
где λ – длина свободного пробега молекулы; с – скорость теплового движения молекул (численно равна скорости звука); γ – число столкновений молекул, обладающих энергией активации
а температуропроводность: μ=⅓ λ·с
тогда скорость распространения пламени: U=c/√γ·√Ф/3
если √γ>1, то скорость распространения пламени намного
меньше скорости звука.
№7 слайд
Содержание слайда: Уравнение теплового баланса:
сР·ρ·dT/dt=U·cP·ρ·dT/dt+η·d2T/dx2+F
где сР·ρ·dT/dt – изменение температуры в какой-то точке в единице объёма; U·cP·ρ·dT/dt – тепло, которое вносит газ, обладающий температурой Т и втекающий в зону реакции; η·d2T/dx2 - тепло которое образуется в результате теплопроводности вещества в зоне горения; F – количество тепла, выделяющееся в единицу времени и единицу объема
Упрощения:
при стационарном режиме сР·ρ·dT/dt =0
зона реакции чрезвычайно тонкая, поэтому пренебрегаем количеством тепла которое вносит протекающий через него газ: U·cP·ρ·dT/dt =0
№8 слайд
Содержание слайда: Тогда упрощенный вид уравнения теплового баланса будет выглядеть: η·d2T/dx2+F=0
Вводим дополнительные переменные:
φ=d2T/dx2
dx=dT/φ
d2T/dx2=φ·dφ
Тогда уравнение теплового баланса:
η·φ·dφ=-F·dT
№9 слайд
Содержание слайда: Скорость горения определяется теплопроводностью газа и объемной скоростью тепловыделения.
Концентрацию продуктов реакции рассчитывают по уравнению:
с=(Тг-Т)/(Тг-Т0)
Массовая скорость принимает вид:


















