Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
14 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
255.50 kB
Просмотров:
40
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
№2 слайд
Содержание слайда: Алканы – углеводороды с общей формулой CnH2n+2 , которые не присоединяют водород и другие элементы.
Алканы – углеводороды с общей формулой CnH2n+2 , которые не присоединяют водород и другие элементы.
Все связи в молекулах алканов одинарные. Перекрывание происходит по оси, соединяющей ядра атомов, т.е. это сигма- связи. Длина связи С – С равна 0,154нм. Связи С – Н несколько короче. Электронная плотность несколько смещена в сторону более э.о атома углерода, т.е. связь С – Н является слабополярной.
№3 слайд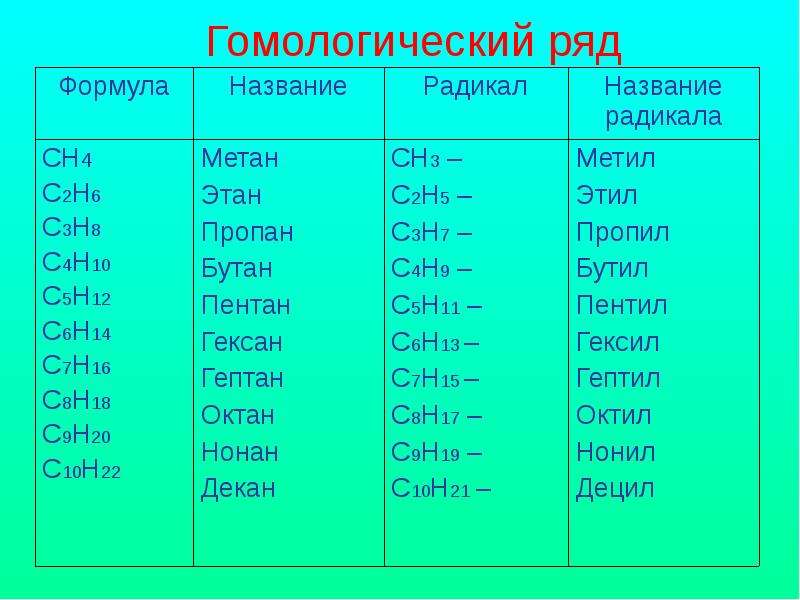
Содержание слайда: Гомологический ряд
№4 слайд
Содержание слайда: Изомерия
Структурная
Изомерия углеродного скелета
С5Н12 : СН3 – СН2 – СН2 – СН2 – СН3
н-пентан СН3
СН3 – СН – СН2 – СН3 І
l СН3 ─ С ─ СН3
СН3 І
2-метилбутан СН3
2,2-диметилпропан
Пространственная: не характерна
№5 слайд
Содержание слайда: Физические свойства
С увеличением относительных молекулярных масс предельных углеводородов закономерно повышаются их температуры кипения и плавления.
№6 слайд
Содержание слайда: МЕТАН, CH4, бесцветный газ, tкип 164 °C. Основной компонент природных (77-99%), попутных нефтяных (31-90%), рудничного и болотного газов. Горит бесцветным пламенем. С воздухом образует взрывоопасные смеси. Сырье для получения многих ценных продуктов химической промышленности — формальдегида, ацетилена, сероуглерода, хлороформа, синильной кислоты, сажи. Применяется как топливо.
МЕТАН, CH4, бесцветный газ, tкип 164 °C. Основной компонент природных (77-99%), попутных нефтяных (31-90%), рудничного и болотного газов. Горит бесцветным пламенем. С воздухом образует взрывоопасные смеси. Сырье для получения многих ценных продуктов химической промышленности — формальдегида, ацетилена, сероуглерода, хлороформа, синильной кислоты, сажи. Применяется как топливо.
№7 слайд
Содержание слайда: ЭТАН, С2Н6, бесцветный газ, tкип -88,6 °С. Содержится в нефтяных и природных газах. Сырье в промышленном органическом синтезе.
ЭТАН, С2Н6, бесцветный газ, tкип -88,6 °С. Содержится в нефтяных и природных газах. Сырье в промышленном органическом синтезе.
ПРОПАН, СН3СН2СН3, бесцветный газ, tкип -42,1 °С. Содержится в природных и нефтяных газах, образуется при крекинге нефтепродуктов. Применяется, напр., для получения пропилена, нитрометана. В смеси с бутаном используется как бытовой газ.
№8 слайд
Содержание слайда: БУТАНЫ, бесцветные газы: нормальный бутан CH3(CH2)3CH3 ( tкип -0,5 °С) и изобутан (CH3)2CHCH3 ( tкип -11,7 °С). Содержатся в нефтяных и природных газах и в газах нефтепереработки. Из нормального бутана получают бутадиен, из изобутана — изобутилен. В смеси с пропаном применяются как топливо.
БУТАНЫ, бесцветные газы: нормальный бутан CH3(CH2)3CH3 ( tкип -0,5 °С) и изобутан (CH3)2CHCH3 ( tкип -11,7 °С). Содержатся в нефтяных и природных газах и в газах нефтепереработки. Из нормального бутана получают бутадиен, из изобутана — изобутилен. В смеси с пропаном применяются как топливо.
№9 слайд
Содержание слайда: ПЕНТАНЫ, насыщенные ациклические углеводороды C5H12; бесцветные жидкости: нормальный пентан ( tкип 36,1 °С), изопентан ( tкип 27,9 °С) и неопентан. Содержатся в нефти, сланцевой смоле. Входят в состав моторных топлив. Применяются как растворители. Из изопентана получают изопрен.
ПЕНТАНЫ, насыщенные ациклические углеводороды C5H12; бесцветные жидкости: нормальный пентан ( tкип 36,1 °С), изопентан ( tкип 27,9 °С) и неопентан. Содержатся в нефти, сланцевой смоле. Входят в состав моторных топлив. Применяются как растворители. Из изопентана получают изопрен.
№10 слайд
Содержание слайда: ГАЛОГЕНОПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ (галогенсодержащие углеводороды), углеводороды, в молекулах которых один или несколько атомов водорода замещены на атомы галогена. Сырье в промышленном органическом синтезе, растворители, хладоны.
ГАЛОГЕНОПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ (галогенсодержащие углеводороды), углеводороды, в молекулах которых один или несколько атомов водорода замещены на атомы галогена. Сырье в промышленном органическом синтезе, растворители, хладоны.
№11 слайд
Содержание слайда: Получение
1) В промышленности алканы выделяют из продуктов переработки нефти и попутных нефтяных газов
2) Взаимодействие галогенопроизводных алканов с активными металлами
С4Сl2Н10 + 2Na → СН4 + Na2СО3
3) Нагревание прокаленного ацетата натрия с твердым гидроксидом натрия
СН3СОО Na + NaОН → СН4 + Na2СО3
№12 слайд
Содержание слайда: Химические свойства
1) Реакции замещения
СН4 + Сl2 → СН3Сl + НСl
СН4 + Сl2 → СН2Сl2 + 2НСl
СН4 + 3Сl2 → СНСl3 + 3НСl
СН4 + 4Сl2 → ССl4 + 4НСl
№13 слайд
Содержание слайда: 2) Реакции окисления
2) Реакции окисления
горение
С3Н8 + 5О2 → 3СО2 + 4Н2О
в присутствии катализаторов окисляются:
а) СН4 + О2 -------→ НСОН +Н2О
б) 2СН3(СН2)34СН3 + 5О2 →
→4СН3─(СН2)16СООН + 2Н2О
№14 слайд
Содержание слайда: 3) Реакции дегидрирования
3) Реакции дегидрирования
2СН4 ---→ Н─С≡С─Н + 3Н2
СН3─СН3 ---→ Н2С═СН2 + Н2
4) Реакции с водяным паром
СН4 + Н2О → СО + 3Н2
5) Ароматизация (для алканов с шестью или более углеродными атомами)
С6Н14 ---→ С6Н6 + 4Н2























