Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
14 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
1.38 MB
Просмотров:
75
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Изучение свойств оксидов металлов
Комиссаров Кирилл, ГОУ ЦО № 1455 г. Москвы
№2 слайд
Содержание слайда: Цель: определить характер оксидов металлов, имеющихся в школьной лаборатории (оксиды бария, железа, кальция, меди, свинца), изучить их свойства.
Цель: определить характер оксидов металлов, имеющихся в школьной лаборатории (оксиды бария, железа, кальция, меди, свинца), изучить их свойства.
Задачи:
Изучить физические свойства оксидов (агрегатное состояние, цвет, растворимость в воде).
Изучить химические свойства оксидов металлов (взаимодействие с кислотами и основаниями).
№3 слайд
Содержание слайда: Внешний вид оксидов
№4 слайд
№5 слайд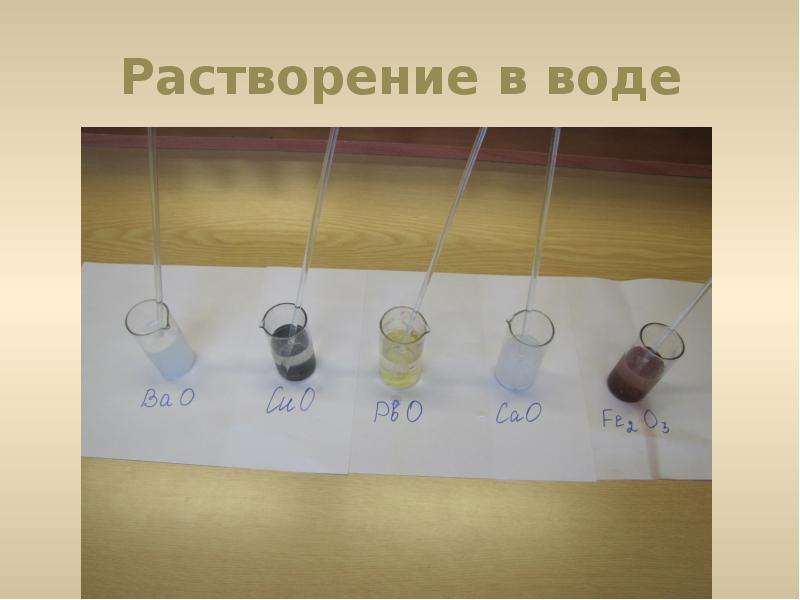
Содержание слайда: Растворение в воде
№6 слайд
№7 слайд
№8 слайд
Содержание слайда: Оксид кальция
Как основный оксид реагирует с кислотными оксидами и кислотами, образуя соли:
CaO + SO2 = CaSO3
CaO + 2HCl = CaCl2 +H2O
С растворами щелочей не взаимодействует
№9 слайд
Содержание слайда: Оксид бария
Как основный оксид реагирует с кислотными оксидами и кислотами, образуя соли:
ВaO + СO2 = ВaСO3
ВaO + 2HCl = ВaCl2 +H2O
С растворами щелочей не
взаимодействует
№10 слайд
Содержание слайда: Оксид железа
Амфотерный оксид с большим преобладанием основных свойств. Медленно реагирует с кислотами и щелочами.
Fe2О3 + 6НСl = 2FeСl3 + 3Н2О.
Fe2О3 + 2NaOН = 2NaFeO2 + Н2О.
№11 слайд
Содержание слайда: Оксид меди
При взаимодействии с кислотами образуются соли:
CuO + H2SO4 = CuSO4 + H2O
С растворами щелочей не взаимодействует
При сплавлении со щелочами образуются купраты:
CuO + 2NaOH = Na2CuO2 + H2O
№12 слайд
Содержание слайда: Оксид свинца
Проявляет амфотерные свойства, реагирует с кислотами и щелочами.
PbО + 2СН3СООН = Pb (СН3СОО)2 + Н2О.
PbО + КОН = К2PbО2 + Н2О.
№13 слайд
Содержание слайда: Выводы
Оксиды кальция и бария растворяются в воде с образованием оснований. Оксиды меди, свинца и железа не растворимы в воде.
С растворами кислот взаимодействуют все оксиды, но хуже всего реагирует оксид железа.
С растворами щелочей взаимодействуют оксиды свинца и железа.
Оксиды кальция, бария и меди – основные; оксиды свинца и железа – амфотерные.
№14 слайд
Содержание слайда: Источники информации
Венецкий С.И. О редких и рассеянных. Рассказы о металлах. М: Металлургия, 1980.
Николаев А.Л. Первые в рядах элементов. М: Просвещение, 1983
http://dic.academic.ru
http://ru.wikipedia.org
http://www.kontren.narod.ru/
http://ru.science.wikia.com























