Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
30 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
108.00 kB
Просмотров:
177
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Классы неорганических соединений
Подготовка к ЕГЭ
№2 слайд
Содержание слайда: Оксиды
Образованы двумя химическими элементами
Один из элементов кислород, имеющий степень окисления -2
Примеры: MgO, H2O
№3 слайд
Содержание слайда: Оксидами являются оба вещества в паре
1)MgO и H2O2
2)Na 2O2 и BaO
3)Mn2О7 и N2O3
4)F2О и P2O5
№4 слайд
Содержание слайда: Классификация оксидов
Несолеобразующие (безразличные)
№5 слайд
Содержание слайда: Основные оксиды
Оксиды металлов, в которых металл имеет степень окисления +1 или +2 как правило
Основным оксидам соответствуют основания (основные гидроксиды):
Na2O – NaOH
MgO – Mg(OH)2
№6 слайд
Содержание слайда: Свойства основных оксидов
Реагируют с кислотами:
MgO + H2SO4 = MgSO4 + H2O
Некоторые реагируют с водой (оксиды щелочных и щелочно-земельных металлов):
Na2O + H2O = 2NaOH
Реагируют с кислотными оксидами:
CaO + CO2 = CaCO3
№7 слайд
Содержание слайда: Кислотные оксиды
Оксиды неметаллов и металлов, в которых элемент имеет степень окисления +4 и выше как правило
Кислотным оксидам соответствуют кислоты (кислотные гидроксиды):
CO2 – H2CO3 Mn2O7 – HMnO4
SO3 – H2SO4 CrO3 – H2CrO4, H2Cr2O7
№8 слайд
Содержание слайда: Свойства кислотных оксидов
Реагируют со щелочами (растворимыми в воде основаниями):
CO2 + 2NaOH = Na2CO3 + H2O
Большинство реагирует с водой:
SO3 + H2O = H2SO4
Реагируют с основными оксидами:
P2O5 + 3CaO = Ca3(PO4)2
№9 слайд
Содержание слайда: Амфотерные оксиды
Оксиды металлов, в которых металл проявляет степень окисления +3 или +4 как правило
Амфотерным оксидам соответствуют амфотерные гидроксиды:
Al2O3 – Al(OH)3 ZnO – Zn(OH)2
Cr2O3 – Cr(OH)3 BeO – Be(OH)2
MnO2 – Mn(OH)4
№10 слайд
Содержание слайда: Свойства амфотерных оксидов
Амфотерность – двойственность свойств
Реагируют с кислотами, проявляя свойства основных оксидов:
Al2O3 + 6HCl = 2AlCl3 + 3H2O
Реагируют со щелочами, проявляя свойства кислотных оксидов:
Al2O3 + 2NaOH + 3H2O= 2Na[Al(OH)4]
Al2O3 + 2NaOH = 2NaAlO2 + H2O (при сплавлении)
№11 слайд
Содержание слайда: С водой реагируют оксиды:
1)BaO и SiO2
2)СuO и SO3
3)BaO и SO3
4)FeO и СО2
№12 слайд
Содержание слайда: Оксид серы (IV) взаимодействует с каждым из двух веществ:
1)H2O и KCl
2)Ba(OH)2 и CaO
3)CaCO3 и ZnSO3
4)Ca(OH)2 и N2
№13 слайд
Содержание слайда: С соляной кислотой реагируют каждый из двух оксидов
1)K2O и SO3
2)Al2O3 и CaO
3)CO2 и ZnO
4)CrO3 и Na2O
№14 слайд
Содержание слайда: И с раствором гидроксида натрия и с серной кислотой реагирует
1)ВаO
2) Cr2O3
3) SiO2
4) MgO
№15 слайд
Содержание слайда: Гидроксиды
Основные – основания (щелочи и нерастворимые в воде)
Кислотные – кислоты кислородсодержащие
Амфотерные
№16 слайд
Содержание слайда: Только кислоты расположены в ряду
1)HNO3, Ca(NO3)2, NO2
2)KHCO3, Ba(HSO4)2, Zn(OH)Cl
3)HNO2, HNO3, CH3COONa
4)H2S, Н2SO3, CH3COOH
№17 слайд
Содержание слайда: Оцените правильность следующих суждений:
А) Гидроксиды по свойствам делятся на кислоты, основания и амфотерные гидроксиды.
Б) Гидроксиды элементов главных подгрупп первой и второй групп Периодической системы – растворимые основания (щелочи).
1)верно только А
2)верно только Б
3)верны оба суждения
4)оба суждения неверны
№18 слайд
Содержание слайда: Щелочи – растворимые в воде основания
Щелочи образуют металлы 1 группы главной подгруппы (щелочные металлы) и щелочноземельные металлы (Ca, Sr, Ba)
Примеры: NaOH, Ca(OH)2
№19 слайд
Содержание слайда: Свойства щелочей
Реагируют с кислотами:
2NaOH + H2SO4 = Na2SO4 + 2H2O
Реагируют с кислотными оксидами:
2NaOH + CO2 = Na2CO3 + H2O
Реагируют с растворами солей, если выпадает осадок:
2NaOH+ CuSO4 = Cu(OH)2↓ + Na2SO4
Реагируют с металлами, образующими амфотерные оксиды и гидроксиды:
2NaOH + Zn +2H2O = Na2[Zn(OH)4] + Н2
№20 слайд
Содержание слайда: Нерастворимые в воде основания
Реагируют с кислотами:
Mg(OH)2 + 2HNO3 = Mg(NO3)2 +2H2O
Разлагаются при нагревании:
Mg(OH)2 = MgO +H2O
№21 слайд
Содержание слайда: Кислотные гидроксиды – кислородсодержащие кислоты
Реагируют с основаниями:
KOH + HNO3 = KNO3 + H2O
Реагируют с основными оксидами:
MgO + H2SO4 = MgSO4 + H2O
Реагируют с металлами, стоящими в ряду напряжений до водорода:
Mg + H2SO4 = MgSO4 + H2
Реагируют с солями:
Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2
№22 слайд
Содержание слайда: Амфотерные гидроксиды
Реагируют с кислотами, проявляя свойства оснований:
Al(OH)3 + 3HCl = AlCl3 + 3H2O
Реагируют со щелочами, проявляя свойства кислот:
Al(OH)3 + NaOH = Na[Al(OH)4]
№23 слайд
Содержание слайда: Гидроксид натрия не взаимодействует с
1)CuCl2
2)SO2
3)PbS
4)HNO3
№24 слайд
Содержание слайда: Гидроксид натрия реагирует со всеми веществами ряда:
1)Zn, Na 2CO3, CuO
2)CO2, H3 PO4 CuO
3)S O3, H3PO 4, AI2O3
4)SO3, MgO, H3PO4,
№25 слайд
Содержание слайда: Гидроксид калия реагирует со всеми веществами группы
1)Zn, SiO2, H2O
2)HNO3, Na2CO3, Mg
3)CuSO4, SO3, H3PO4
4)CuO, Cа(OH)2, N2O5
№26 слайд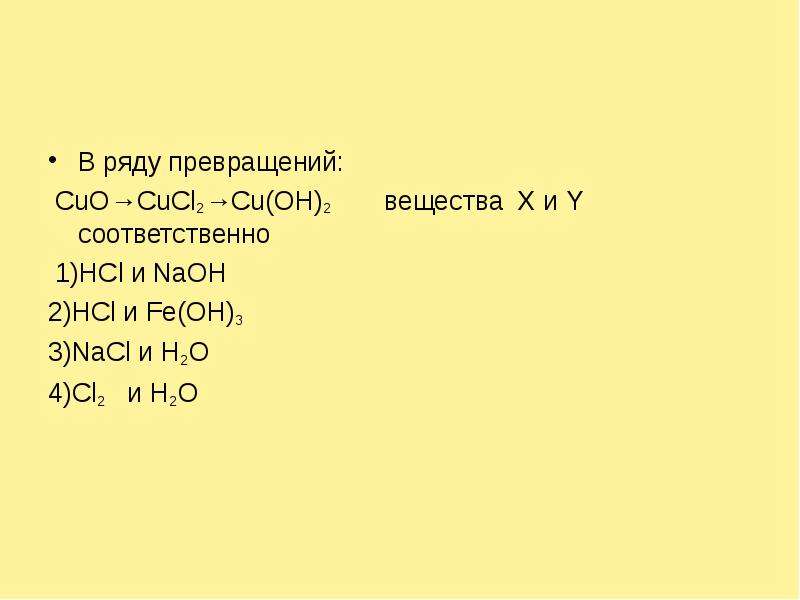
Содержание слайда: В ряду превращений:
CuO→CuCl2→Cu(OH)2 вещества X и Y соответственно
1)НСl и NaOH
2)HCl и Fe(OH)3
3)NaCl и Н2O
4)Cl2 и H2O
№27 слайд
Содержание слайда: В ряду превращений
NaOH→Na 2CO3→CO2
веществa X и Y соответственно
1)Н2CO3 и NaOH
2)CaCO3 и NaOH
3)CO2 и H2O
4)CO2 и H2 SO4
№28 слайд
Содержание слайда: Каждое из перечисленных веществ: CuCl2, SO3, H3PO4, Zn(OH)2
реагирует с
1)серной кислотой 2)водой
3)гидроксидом натрия 4)оксидом углерода(VI)
№29 слайд
Содержание слайда: При действии избытка раствора гидроксида натрия на раствор сульфата цинка образуется
1) ZnO
2) Zn(OH)2
3) Na2ZnO2
4)Na2[Zn(OH)4]
№30 слайд
Содержание слайда: Исходные вещества
А) Al + NaOH + H2O
Б) Al2O3+ NaOH ( плавление)
В) Al2O3+ NaOH+ H2O
Г) Al(OH)3+ NaOH







































