Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
84 слайда
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
858.50 kB
Просмотров:
80
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
№2 слайд
Содержание слайда: УДК 546.04
ББК 24.1
Рецензент: д.х.н. Киселев Ю.М. (химический факультет МГУ)
Рекомендовано к изданию кафедрой неорганической химии МИТХТ
(протокол № 3 от 10.11.2010)
Е.В. Савинкина 2010
МИТХТ им. М.В. Ломоносова 2010
Утверждено Библиотечно-издательской комиссией МИТХТ им. М.В.Ломоносова в качестве учебного пособия для студентов 1 курса бакалавриата по направлениям 020100 62 (Химия), 240100 62 (Химическая технология и биотехнология), 150600 62 (Материаловедение и технология новых материалов), 280200 (Защита окружающей среды), 200500 62 (Метрология, стандартизация и сертификация), 080500 (Менеджмент).
Один оптический диск
Объем данных 0,9 Мб
№3 слайд
Содержание слайда: Растворы
Общие свойства растворов
№4 слайд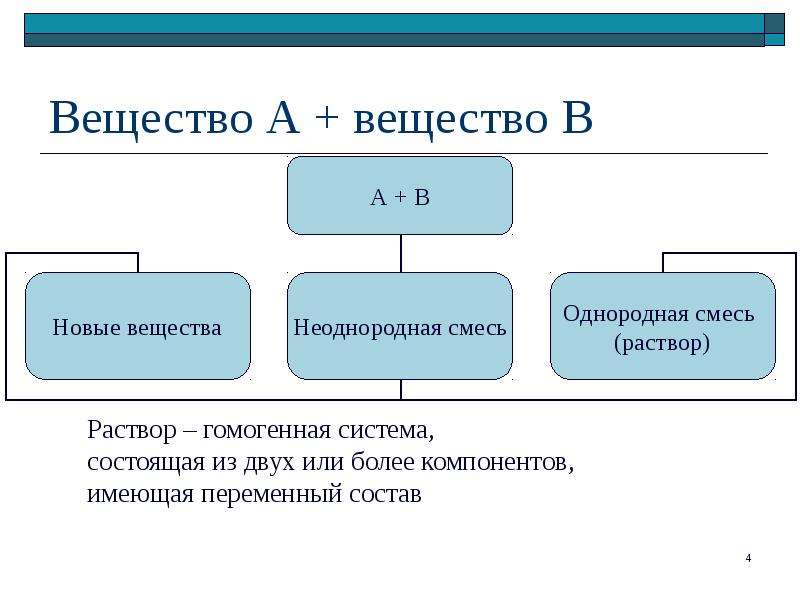
Содержание слайда: Вещество А + вещество В
№5 слайд
Содержание слайда: Смеси веществ
Смеси
Грубодисперсные системы (взвеси)
Тонкодисперсные системы (коллоидные системы)
Истинные растворы
№6 слайд
Содержание слайда: Грубодисперсные системы
Дисперсионная среда – газообразная
Дисперсная фаза:
твердая – пыль, дым, порошок
жидкая – смог, облако, туман
Дисперсионная среда – жидкая
Дисперсионная фаза:
твердая – суспензия, паста
жидкая – эмульсия
газообразная – пена, газированная вода
Дисперсионная среда – твердая
Дисперсная фаза:
твердая – горные породы, цветные стекла, композиты
жидкая – твердые эмульсии
газообразная – твердые пены
№7 слайд
Содержание слайда: Истинные растворы
Агрегатное состояние: газообразные, жидкие, твердые растворы
Состав раствора: растворитель + растворенное вещество
Параметры раствора: температура, давление, содержание растворенного вещества
№8 слайд
Содержание слайда: Количественный состав раствора
Массовая доля
Молярная концентрация (молярность)
Эквивалентная концентрация (нормальность)
Коэффициент растворимости
Мольная доля
Массовая концентрация
Моляльная концентрация (моляльность)
№9 слайд
Содержание слайда: Растворы
Идеальные
ΔV = 0; ΔQ = 0
Реальные
ΔV ≠ 0
1 л H2O + 1 л C2H5OH → 1,93 л раствора
ΔQ ≠ 0
Qрастворение = – Qразрыв связей + Qобразование связей
№10 слайд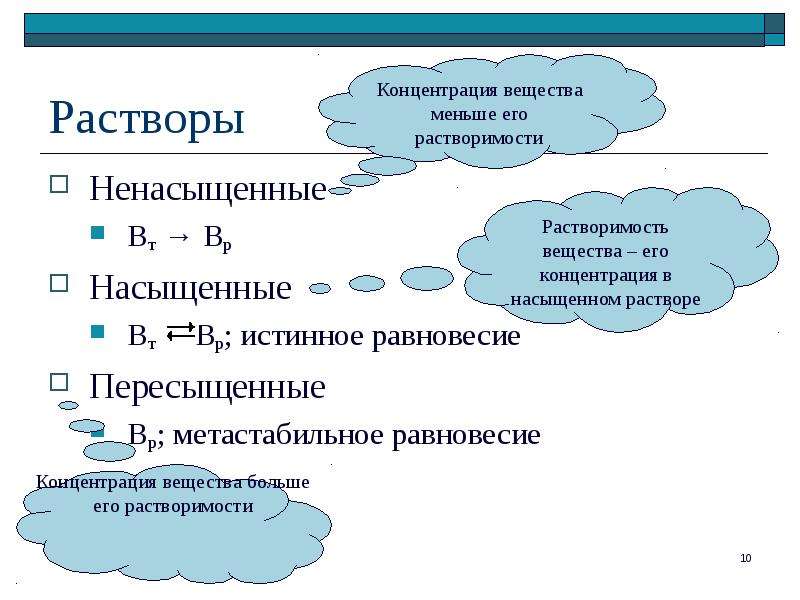
Содержание слайда: Растворы
Ненасыщенные
Вт → Вр
Насыщенные
Вт Вр; истинное равновесие
Пересыщенные
Вр; метастабильное равновесие
№11 слайд
Содержание слайда: Растворимость газов в жидкостях
Если нет химического взаимодействия
Ar(г) Ar(р)
Влияние давления
= 1 0 (принцип Ле Шателье)
Увеличение давления →
(растворимость увеличивается)
Уменьшение давления ←
(растворимость уменьшается)
№12 слайд
Содержание слайда: Растворимость газов в жидкостях
Влияние температуры
Qразрыв связей ≈ 0
Qобразование связей > 0
Процесс экзотермический (принцип Ле Шателье)
Уменьшение температуры →
(растворимость увеличивается)
Увеличение температуры ←
(растворимость уменьшается)
№13 слайд
Содержание слайда: Растворимость газов в жидкостях
Если есть химическое взаимодействие
Cl2(г) Cl2(р)
Cl2(р) + 2Н2О Н3О+ + Cl + НClО
НClО + Н2О Н3О+ + ClО
№14 слайд
Содержание слайда: Растворимость твердых веществ в жидкостях
Влияние давления
ΔV ≈ 0; давление не влияет
Влияние температуры
№15 слайд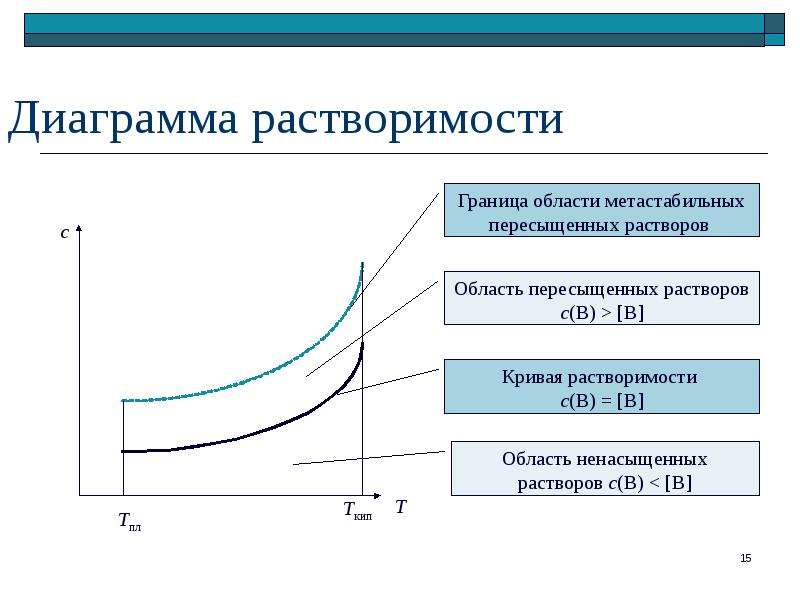
Содержание слайда: Диаграмма растворимости
№16 слайд
Содержание слайда: Перекристаллизация
№17 слайд
Содержание слайда: Растворы электролитов
Электролитическая диссоциация
№18 слайд
Содержание слайда: Сильные электролиты
MA M+(р) + A–(р)
[MA] = 0, [M+] = [A–] = c0
Степень диссоциации:
№19 слайд
Содержание слайда: Слабые электролиты
MA MA(р) + M+(р) + A–(р)
[MA] > 0, [M+] = [A–] < c0
Степень диссоциации:
№20 слайд
Содержание слайда: Слабые электролиты
MxAy(р) x Ma+(р) + y Ab–(р)
Константа диссоциации KD
№21 слайд
Содержание слайда: Закон разбавления Оствальда
МА М+ + А–
[M+] [A–]
KD = –––––––––
[MA]
[M+] = [A–] = c0
[MA] = (1 – ) c0
KD = 2 c0 / (1 – )
№22 слайд
Содержание слайда: Гетерогенные ионные равновесия
М+ + А–
МА(т)
№23 слайд
Содержание слайда: Растворимость (L), моль/л
МхАу(т) х Ма+ + у Аb–
[Ma+] = x L; [Ab–] = y L
ПР(МхАу) = (x L)x (y L)y = xx yy Lx+y
№24 слайд
Содержание слайда: Задача
Рассчитать растворимость сульфата серебра, если ПР(Ag2SO4) = 1,2 . 10–5
Ag2SO4(т) 2Ag+ + SO42–
L 2L L
ПР = [Ag+ ]2 [SO42–] = (2L)2L = 4L3
№25 слайд
Содержание слайда: Условия осаждения и растворения осадков
№26 слайд
Содержание слайда: Введение одноименного иона
МхАу(т) х Ма+ + у Аb–
Увеличение с(Ма+) или с(Аb–)
Сдвиг равновесия в сторону образования осадка
№27 слайд
Содержание слайда: Удаление одноименного иона
МхАу(т) х Ма+ + у Аb–
Уменьшение с(Ма+) или с(Аb–)
Сдвиг равновесия в сторону растворения осадка
№28 слайд
Содержание слайда: Удаление одноименного иона
Связывание в виде менее растворимого вещества (осадок AgCl осадок AgI)
Связывание в виде комплексного иона (осадок PbSO4 [Pb(OH)4]2–)
Перевод в другую форму
(осадок BaCrO4 Cr2O72–)
№29 слайд
Содержание слайда: Переосаждение
PO43–
Ag2SO4(т) Ag3PO4(т)
SO42–
3 Ag2SO4(т) + 2 PO43– 2 Ag3PO4(т) + 3 SO42– (1)
KС = [SO42–]3 / [ PO43–]2
ПР1 = [Ag+]2[SO42–]
ПР2 = [Ag+]3[ PO43–]
(1) = 3(2) – 2(3)
KС = (ПР1)3 / (ПР2)2 ~ (10–5)3/(10–18)2 > 1
№30 слайд
Содержание слайда: В каком минимальном объеме воды можно растворить 1 г гипса?
Условие задачи
V(H2O) = ?
m(CaSO4.2H2O) = 1 г
ПР(CaSO4) = 4.10–5
M(CaSO4.2H2O) = 172 г/моль
№31 слайд
Содержание слайда: Выпадет ли осадок при сливании равных объемов миллимолярных растворов нитрата серебра(I) и хлорида натрия?
№32 слайд
Содержание слайда: Протолитическая теория кислот и оснований
1923 г.
Йоханес Брёнстед
Томас Лаури
№33 слайд
Содержание слайда: Протолитическая теория
кислотные или основные свойства частиц обусловлены их способностью отдавать или присоединять катион водорода (протон Н+)
NH4+ + S2– NH3 + HS–
Кт Ос Ос Кт
Пары "сопряженная кислота / сопряженное основание":
NH4+/NH3 и HS –/ S2–
№34 слайд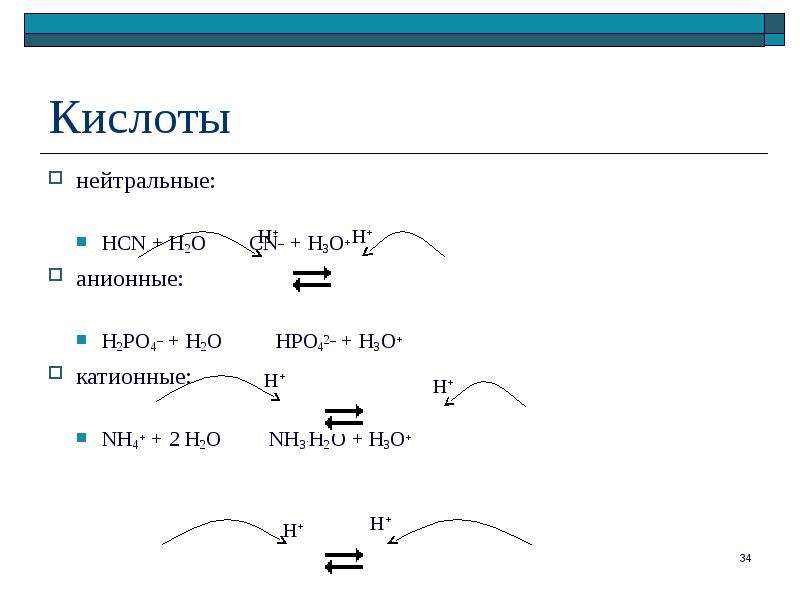
Содержание слайда: Кислоты
нейтральные:
HCN + H2O CN– + H3O+
анионные:
H2PO4– + H2O HPO42– + H3O+
катионные:
NH4+ + 2 H2O NH3.H2O + H3O+
№35 слайд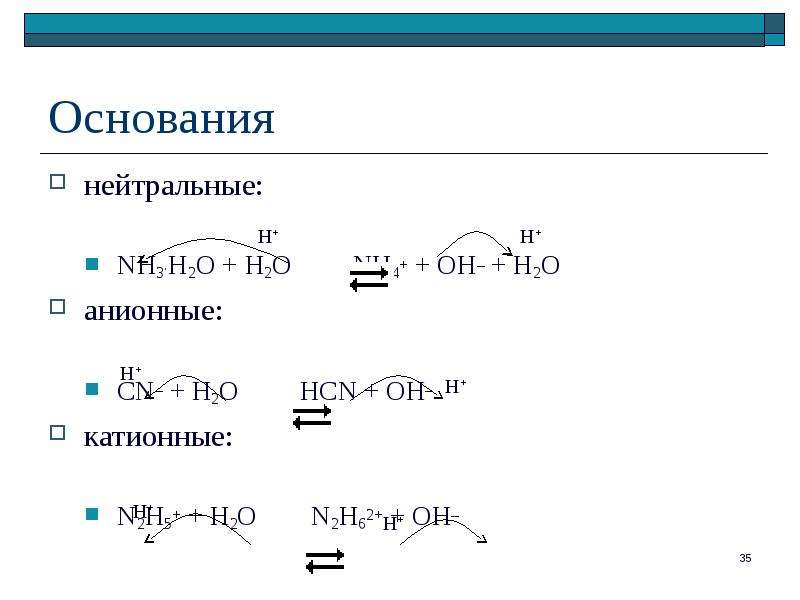
Содержание слайда: Основания
нейтральные:
NH3.H2O + H2O NH4+ + OH– + H2O
анионные:
CN– + H2O HCN + OH–
катионные:
N2H5+ + H2O N2H62+ + OH–
№36 слайд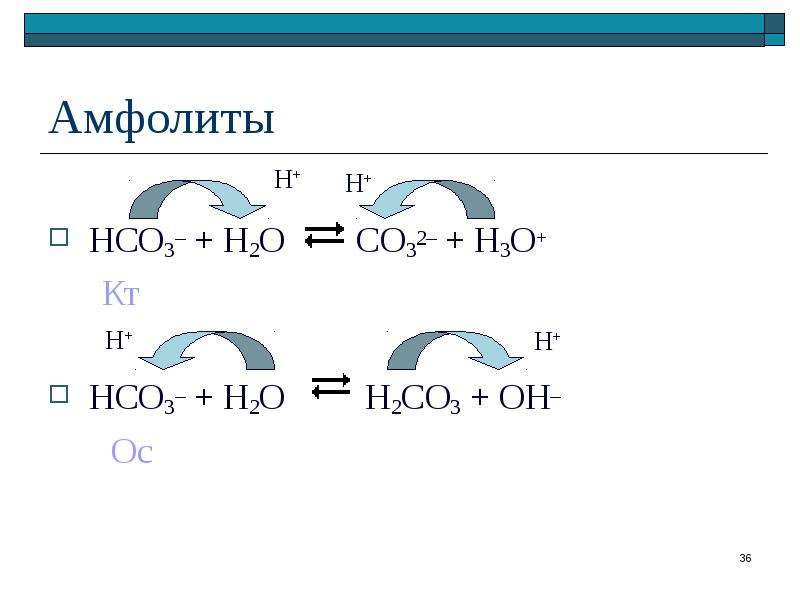
Содержание слайда: Амфолиты
HCO3– + H2O CO32– + H3O+
Кт
HCO3– + H2O H2CO3 + OH–
Ос
№37 слайд
Содержание слайда: Растворители
Апротонные:
C6H6, CS2, CCl4
Протонные
H2O, NH3, C2H5OH
(амфолиты)
№38 слайд
Содержание слайда: Ионное произведение воды
H2O + H2O H3O+ + OH–
При стандартной температуре 298 К (25 С):
KB (Kw) = [H3O+] [OH–] = 1.10–14
В чистой воде при 25 С
[H3O+] = [OH–] = KB = 10–7 моль/л
№39 слайд
Содержание слайда: Водородный показатель (рН)
рН = –lg[H3O+]
[H3O+] = 10–рН
Гидроксидный показатель (рОН)
pOH = –lg[OH–]
[OH–] = 10–рОН
рН + рОН = –lgKB = 14
№40 слайд
Содержание слайда: Водородный показатель (рН)
В чистой воде при 25С
рН = рОН = 7
Среда нейтральная
Если [H3O+] > 1.10–7, то рН < 7
Среда кислотная
Если [OH–] > 1.10–7, то рОН < 7 и pH > 7
Среда щелочная
№41 слайд
Содержание слайда: Шкала рН
При [H3O+] = 0,1 моль/л
(например, в 0,1 М растворе HCl)
pH = 1 (нижний предел).
При [OH–] = 0,1 моль/л
(например, в 0,1 М растворе KOH)
рН = 13 (верхний предел).
№42 слайд
Содержание слайда: Константа кислотности
HA + H2O A– + H3O+
№43 слайд
Содержание слайда: Слабые кислоты
Сопряженная пара KК
СН3СООН / СН3СОО– 1,7.10–5
Al3+.H2O / AlOH2+ 9,6.10–6
H2S / HS– 1,1.10–7
B(OH)3.H2O/[B(OH)4]– 5,8.10–10
№44 слайд
Содержание слайда: Сильные кислоты
HA + H2O = A– + H3O+
Бескилородные кислоты: HCl, HBr, HI
Кислородсодержащие кислоты состава НхЭОу, если у – х 2 (правило Полинга)
Протолиз сильных кислот необратим
Анионы сильных кислот являются непротолитами и не участвуют в реакциях протолиза
№45 слайд
Содержание слайда: Сила кислот в неводных растворителях
Уравнение реакции протолиза Сопряженная пара KК
№46 слайд
Содержание слайда: Константа основности
A– + H2O HA + ОН–
№47 слайд
Содержание слайда: Слабые основания
№48 слайд
Содержание слайда: Сильные основания
Анионы:
амид-ион NH2–
метилат-ион CH3O– и другие алкоголят-ионы
гидроксид-ион ОН–
Соединения, дающие эти ионы при диссоциации
MOH, где М – щелочной элемент или Tl(I)
M(OH)2, где М – Ba, Ra
и др.
№49 слайд
Содержание слайда: Малорастворимые гидроксиды
Ni(OH)2(т) Ni2+ + 2OH—
Слабое основание?
Сильное основание?
ПР = [Ni2+][OH—]2
№50 слайд
Содержание слайда: Связь Kк и Ko для пары НА/А–
№51 слайд
Содержание слайда: Степень протолиза ()
– отношение числа частиц, подвергшихся протолизу, к исходному числу частиц
Для реакции протолиза слабой кислоты:
HA + H2O A– + H3O+
([H3O+] = [A–] при отсутствии в растворе других протолитов)
№52 слайд
Содержание слайда: Закон разбавления Оствальда
При << 1 ( < 0,05):
_____
= Kк / c0
№53 слайд
Содержание слайда: Степень протолиза
№54 слайд
Содержание слайда: Учет автопротолиза воды
HA + H2O A– + H3O+
H2O + H2O OH– + H3O+
№55 слайд
Содержание слайда: Учет автопротолиза воды
Kкc0 – Kк[A–] = [A–][H3O+]
№56 слайд
Содержание слайда: Учет автопротолиза воды
При бесконечном разбавлении:
с0 → 0; [H3O+] → 10–7 моль/л
при Kк ≥ 10–5 α → 1
при Kк = 10–7 α → 0,5
№57 слайд
Содержание слайда: Сдвиг протолитических равновесий
Изменение концентрации слабого протолита
закон разбавления Оствальда
разбавление
Изменение температуры
протолиз – эндотермический процесс
нагревание
Изменение концентрации одноименных ионов
принцип Ле Шателье
введение одноименных ионов
№58 слайд
Содержание слайда: Сдвиг протолитических равновесий
Протолиз слабой кислоты в присутствии сильной кислоты:
HA + H2O A– + H3O+
= Kк / [H3O+]
№59 слайд
Содержание слайда: Определите рН в 0,001 М растворе серной кислоты.
H2SO4 + 2H2O = SO42 + 2H3O+
с0(H2SO4) = 0,001 мольл
pH = –lg [H3O+] = – lg(2c0) = – lg (2.10–3) = 2,7
№60 слайд
Содержание слайда: Определите рН в растворе азотной кислоты с концентрацией с0 = 1.10–11 моль/л.
HNO3 + H2O = NO3– + H3O+
[H3O+] = c0 = 1.10–11
pH = – lg[H3O+] = 11
H2O + H2O H3O+ + OH–
[H3O+] = 1.10–7
Ответ: рН 7
№61 слайд
Содержание слайда: Определите рН в 0,002М растворе хлорноватистой кислоты при 25 °C.
HClO + H2O ClO– + Н3O+; Kк = 2,82 . 10–8
[ClO–] = [H3O+]; [HClO] = c0
№62 слайд
Содержание слайда: Определите pH в 0,002М растворе аммиака при 25 °С.
KK = 5,75 . 10–10
KB = 1 . 10–14
[NH4+] = [OH–]; [NH3 . H2O] = c0
№63 слайд
Содержание слайда: Обратимый гидролиз солей
1. Диссоциация
2. Протолиз
№64 слайд
Содержание слайда: Гидролиз солей
KCl = K+ + Cl–
непротолиты
Нет гидролиза, нейтральная среда, рН 7
NH4NO3 = NH4+ + NO3–
Кт непротолит
NH4+ + 2H2O NH3.H2O + H3O+
Гидролиз по катиону, кислотная среда, pH < 7
№65 слайд
Содержание слайда: Гидролиз солей
ZnSO4 = Zn2+ + SO42–
Zn2+.H2O + H2O ZnOH+ + H3O+
Гидролиз по катиону, кислотная среда, рН < 7
KNO2 = K+ + NO2–
NO2– + H2O HNO2 + OH–
Гидролиз по аниону, щелочная среда, pH > 7
№66 слайд
Содержание слайда: Гидролиз солей
NH4CN = NH4+ + CN–
NH4+ + 2H2O NH3.H2O + H3O+
CN– + H2O HCN + OH–
Гидролиз по катиону и аниону, рН ?
Ko > Kк
Слабощелочная среда, pH > 7
№67 слайд
Содержание слайда: Гидролиз кислых солей
NaHCO3 = Na+ + HCO3–
HCO3– + H2O CO32– + H3O+
Кт
HCO3– + H2O H2CO3 + OH–
Ос
Ko > Kк; слабощелочная среда, pH > 7
№68 слайд
Содержание слайда: Гидролиз солей
Усиление (α↑)
Повышение температуры
Понижение концентрации
Связывание одноименных ионов
№69 слайд
Содержание слайда: Необратимый гидролиз
PIIICl–I3(ж) + 3H2Oизб. = H2[PHO3](p) + 3HCl(p)
H2[PHO3] + H2O H[PHO3]– + H3O+
HCl + H2O = Cl– + H3O+
pH < 7
№70 слайд
Содержание слайда: Необратимый гидролиз
Mg3N + 8H2O = 2NH3.H2O + Mg(OH)2
NH3·H2O + H2O NH4+ + OH– + H2O
Если Mg(OH)2 в осадке:
Mg(OH)2(т) Mg2+ + 2OH–
Если Mg(OH)2 в растворе:
Mg(OH)2 = Mg2+ + 2OH–
pH > 7
№71 слайд
Содержание слайда: Необратимый гидролиз
Al2S3(т) + 6H2O = 2Al(OH)3↓ + 3H2S↑
Совместный гидролиз:
2Al3+ +3S2– + 6H2O = 2Al(OH)3↓ + 3H2S↑
№72 слайд
Содержание слайда: Определите рН 0,1 М раствора хлорида железа(III).
FeCl3 = Fe3+ + 3 Cl–
Fe3+.H2O + H2O FeOH2+ + H3O+
[Fe(H2O)6]3+ + H2O [Fe(H2O)5(OH)]2+ + H3O+
№73 слайд
Содержание слайда: Определите рН 0,1 М раствора хлорида железа(III).
Более строгий подход:
если считать [Fe3+] = с0(1 – α)
2с0
Kк = –––––––––
(1 – )
№74 слайд
Содержание слайда: Определите рН 0,1 М раствора хлорида железа(III).
При с0 = 0,1 моль /л и Kк = 7103 = 0,007:
0,007 = 2 0,1 {1 }
0,12 + 0,007 0,007 = 0
= 0,23; второй корень отрицательный
рH = lg[H3O+] = lgс0 = lg 0,23 0,1 = 1,6
№75 слайд
Содержание слайда: FeCl3 + H2O + Zn = ?
FeCl3 = Fe3+ + 3 Cl–
Fe3+.H2O + H2O FeOH2+ + H3O+
Zn + 2H3O+ = Zn2+ + H2 + 2H2O
№76 слайд
Содержание слайда: Определите рН в 0,1 М растворе ортофосфата натрия.
Na3PO4 = 3 Na+ + PO43–
PO43– + H2O HPO42– + OH–
№77 слайд
Содержание слайда: Na3PO4 + H2O + Zn = ?
Na3PO4 (т) = 3 Na+ + PO43–
PO43– + H2O HPO42– + OH–
Zn + 2H2O + 2OH– = [Zn(OH)4]2– + H2
№78 слайд
Содержание слайда: Определите рН раствора, содержащего 0,001 моль/л уксусной кислоты и 0,1 моль/л ацетата натрия.
CH3COONa = Na+ + CH3COO–
CH3COOH + H2O CH3COO– + Н3О+
[CH3COOH] = c0 – x
[CH3COO–] = c1 + x
№79 слайд
Содержание слайда: Определите рН раствора, содержащего 0,001 моль/л уксусной кислоты и 0,1 моль/л ацетата натрия.
№80 слайд
Содержание слайда: Определите pH в водном растворе NaHA
HA– – амфолит
(HCO3–, HS–, H2PO4–, HPO42– и т.д.)
Диссоциация:
NaHA = Na+ + HA–
Протолиз иона-амфолита HA– как основания:
HA– + H2O H2A + OH–;
Kо(H2A/HA–) = Kв/Kк(H2A/HA–)
Протолиз иона-амфолита HA– как кислоты:
HA– + H2O A2– + H3O+;
Kк(HA–/A2–)
№81 слайд
Содержание слайда: Определите pH в водном растворе NaHA
Без вывода:
рН не зависит от концентрации амфолита
№82 слайд
Содержание слайда: Определите pH в водном растворе NaHA
HA– pKк(H2A/HA–) pKк(HA–/A2–) pH
HCO3– 6,37 10,33 8,35
HSO3– 1,78 7,20 4,49
HS– 6,98 12,91 9,94
H2PO4– 2,14 7,21 4,68
HPO42– 7,21 12,34 9,78
№83 слайд
Содержание слайда: Кислотно-основные индикаторы
№84 слайд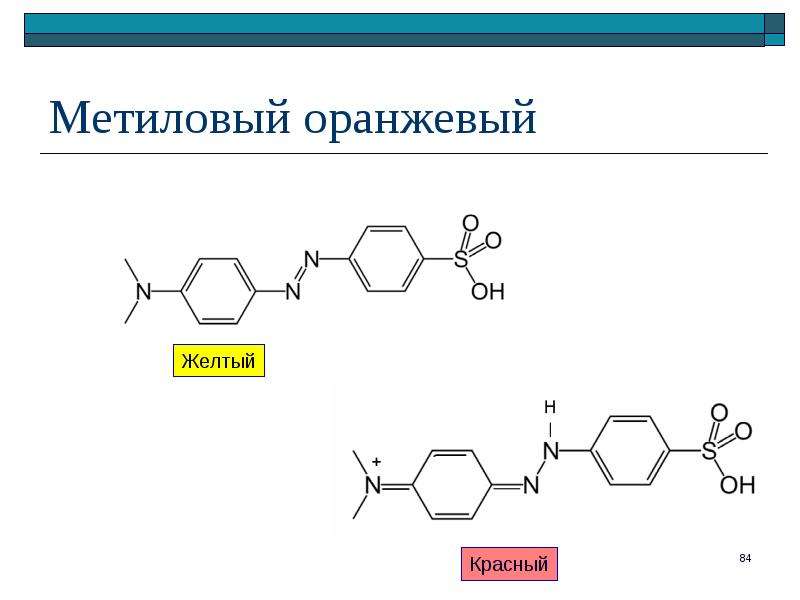
Содержание слайда: Метиловый оранжевый






 По Химии "Классификация реакций в неорганической химии. " - скачать смотреть бесплатно
По Химии "Классификация реакций в неорганической химии. " - скачать смотреть бесплатно По Химии "Взаимосвязь между классами неорганических соединений" - скачать смотреть бесплатно
По Химии "Взаимосвязь между классами неорганических соединений" - скачать смотреть бесплатно По Химии "Классификация реакций в неорганической химии" - скачать смотреть
По Химии "Классификация реакций в неорганической химии" - скачать смотреть По Химии "Химия, нефтехимия. Производство неорганических веществ" - скачать смотреть
По Химии "Химия, нефтехимия. Производство неорганических веществ" - скачать смотреть По Химии "Классификация и номенклатура неорганических соединений" - скачать смотреть
По Химии "Классификация и номенклатура неорганических соединений" - скачать смотреть По Химии "Основные классы Неорганических соединений" - скачать смотреть
По Химии "Основные классы Неорганических соединений" - скачать смотреть По Химии "Генетика и селекция" - скачать смотреть
По Химии "Генетика и селекция" - скачать смотреть По Химии "Неорганические кислоты" - скачать смотреть
По Химии "Неорганические кислоты" - скачать смотреть По Химии "Язык химии. Вещества" - скачать смотреть бесплатно
По Химии "Язык химии. Вещества" - скачать смотреть бесплатно По Химии "Органическая химия" - скачать смотреть бесплатно
По Химии "Органическая химия" - скачать смотреть бесплатно















































































