Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
19 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
311.50 kB
Просмотров:
83
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Теоретические основы аналитической химии
Химическое равновесие в гомогенной системе
№2 слайд
Содержание слайда: Скорость химической реакции и химическое равновесие
Скоростью химической реакции называется изменение концентрации веществ в ходе реакции в единицу времени:
Кинетическое уравнение реакции:
V = к∙[A]·[B] – выражение ЗДМ
Для обратимой реакции A + B ↔ C + D в соответствии с ЗДМ
Тогда в момент равновесия
Концентрационная константа равновесия
№3 слайд
Содержание слайда: Основные положения теории растворов электролитов.
Процесс электролитической диссоциации изображают химическими уравнениями, например:
Степень электролитической диссоциации
По способности к диссоциации электролиты разделяют на 3 группы:
1. сильные электролиты (α = 1)
2. слабые электролиты (α < 1)
3. электролиты средней силы.
Общая концентрация ионов в растворе сi
ci = m∙α∙C
Al2(SO4)3 → 2Al3+ + 3SO42- (α = 1) c(Al3+) = 2∙1∙0,1 = 0,2 моль/л
c(SO42-) = 3∙1∙0,1 = 0,3 моль/л
№4 слайд
Содержание слайда: Константа диссоциации слабого электролита
№5 слайд
Содержание слайда: Закон разбавления Оствальда
№6 слайд
Содержание слайда: Кислотно-основные равновесия в водных растворах
В соответствие с протолитической теорией Бренстеда и Лоури все частицы, способные при ионизации отщеплять протон, называются кислотами, все частицы, способные присоединять протон – основаниями.
Кислоты HCN (к) ↔ H+ + CN- (осн)
HS- (к) ↔ H+ + S2- (осн)
Основания CN- (осн) + H+ ↔ HCN (к)
NН3 (осн) + H+ ↔ NH4+ (к)
Такие кислоты и основания, находящиеся в кислотно-основном равновесии, называются сопряженными, то есть HCN и CN- - сопряженные кислота и основание, аммиак и ион аммония – сопряженные основание и кислота.
Амфолит (амфотерное вещество)
НСО3- ↔ Н+ + СО32-
НСО3- + Н+ ↔ Н2СО3
№7 слайд
Содержание слайда: Кислотно-основные равновесия в водных растворах
Согласно современным представлениям в воде осуществляется протолитическое равновесие – автопротолиз воды:
Н2О + Н2О ↔ Н3О+ + ОН- или упрощенно: Н2О ↔ Н+ + ОН-
Концентрационная константа диссоциации
При температуре 298 K (250С) значение , а молярная концентрация воды в чистой воде
Величина KW называется константа автопротолиза воды или ионное произведение воды. При повышении температуры степень ионизации воды увеличивается и значение константы автопротолиза растет.
№8 слайд
Содержание слайда: Кислотно-основные равновесия в водных растворах
№9 слайд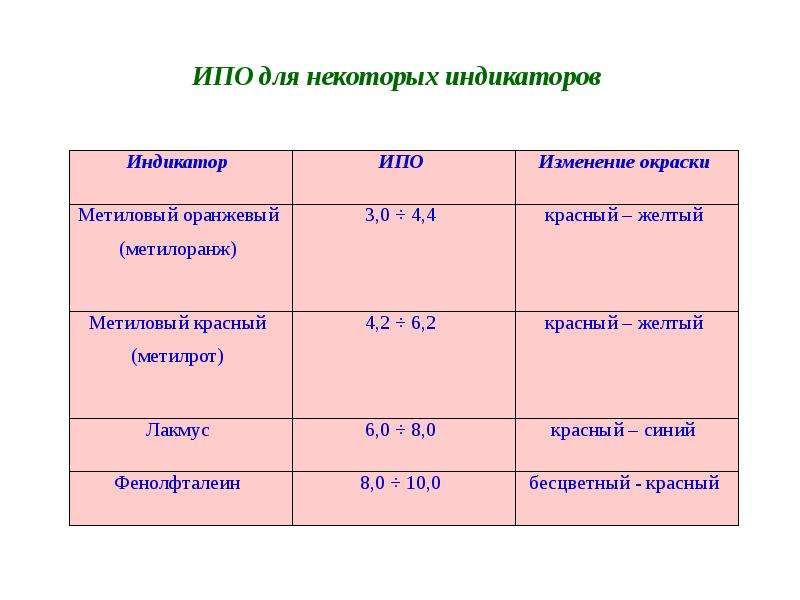
Содержание слайда: ИПО для некоторых индикаторов
№10 слайд
Содержание слайда: Действие одноименнных ионов
Степень диссоциации слабого электролита понижается при введении в раствор какого-либо сильного электролита, содержащего одноименный с ним ион.
Свойства некоторых растворов сохранять практически постоянную концентрацию ионов водорода при добавлении небольших количеств кислоты, щелочи, а также при разбавлении, называют буферным действием, а растворы, которые обладают таким свойством – буферными растворами.
ацетатный буферный раствор – смесь уксусной кислоты и ацетата натрия , аммонийный буферный раствор – смесь аммиака и хлорида аммония.
№11 слайд
Содержание слайда: Буферные растворы
Количественной характеристикой способности буферного раствора поддерживать заданную величину pH является буферная емкость, под которой понимают количество молей сильной кислоты или сильного основания, прибавление которого к 1 л буферного раствора изменяет его pH на единицу.
Протолитические равновесия в растворах солей (гидролиз солей).
Гидролиз солей – это взаимодействие ионов растворенной соли с молекулами воды (ионами Н+ и ОН-, возникающими при диссоциации воды Н2О ↔ Н+ + ОН-), в результате которого образуются малодиссоциированные соединения (слабые кислоты и слабые основания).
Реакция гидролиза процесс обратимый и в растворе устанавливается химическое равновесие между продуктами реакции и исходным соединением, которое характеризуется соответствующей константой равновесия – константой гидролиза Kh.
№12 слайд
Содержание слайда: Гидролиз солей
Количественно гидролиз характеризуется степенью гидролиза h, которая равна отношению числа прогидролизровавшихся частиц nгидр к общему числу исходных ионов nисх и численно выражается в долях единицы или процентах(%):
Степень гидролиза увеличивается с уменьшением концентрации гидролизующейся соли (разбавлением) и с ростом температуры (нагревание).
Гидролизу в водных растворах подвергаются соли, содержащие катионы слабых оснований и анионы слабых кислот.
1. Гидролиз солей, содержащих катион сильного основания и анион слабой одноосновной кислоты (МА). Такие соли нацело диссоциируют в водном растворе с образованием катиона сильного основания М+ и аниона слабой кислоты А-: МА → М+ + А-
Анион слабой кислоты гидролизуется по уравнению:
А- + Н2О ↔ НА + ОН- (pH > 7)
№13 слайд
Содержание слайда: Гидролиз солей
№14 слайд
Содержание слайда: Гидролиз солей
3. Гидролиз солей, содержащих катион слабого однокислотного основания и анион слабой одноосновной кислоты (ВА). Гидролиз такого типа солей происходит с участием обоих ионов, входящих в состав соли:
В+ + А- + Н2О ↔ ВОН + НА
NH4CN, NH4ClO, AgNO2, CH3COONH4, C6H5NH3F и др.
4. Гидролиз солей, содержащих катион сильного однокислотного основания и анион слабой многоосновной кислоты (МnА).
Соли М2А нацело диссоциируют в водном растворе с образованием катиона сильного основания М+ и аниона слабой двухосновной кислоты А2-, который гидролизуется ступенчато по уравнениям:
А2- + Н2О ↔ НА- + ОН- (I ступень)
НА- + Н2О ↔ Н2А + ОН- (II ступень) pH > 7
№15 слайд
Содержание слайда: Гидролиз солей
№16 слайд
Содержание слайда: Произведение растворимости
Гетерогенная (неоднородная) система – это система, состоящая из нескольких гомогенных фаз, разделенных между собой поверхностью раздела.
Равновесие, устанавливающееся в гетерогенной системе на границе раздела фаз, называется гетерогенным равновесием.
Гетерогенная система «осадок – раствор» BaSO4 (т) ↔ Ba2+ + SO42- (р)
Концентрация вещества в насыщенном растворе называется растворимостью. Растворимость является количественной характеристикой способности вещества растворяться. Различают молярную и массовую растворимость вещества.
Молярная растворимость вещества (S, моль/л) – это количество растворенного вещества, содержащееся в одном литре его насыщенного раствора:
Массовая растворимость вещества (Т, г/л) – это масса растворенного вещества, содержащаяся в одном литре его насыщенного раствора:
№17 слайд
Содержание слайда: Произведение растворимости
№18 слайд
Содержание слайда: Произведение растворимости
№19 слайд
Содержание слайда: Произведение растворимости
Произведение растворимости является одной из основных характеристик малорастворимых электролитов и по значению ПР:
1. можно рассчитать условия осаждения;
2. определить растворимость данного осадка в данных условиях;
3. выяснить какой осадок будет выпадать первым.
Из всего сказанного вытекают два следствия:
I. а) Если произведение концентрации ионов (ИП) меньше величины произведения растворимости (ПР), то раствор ненасыщен относительно данного труднорастворимого соединения и осадок не образуется;
б) если произведение концентрации ионов (ИП) равно произведению растворимости (ПР), то раствор насыщен относительно данного труднорастворимого соединения; в растворе наступает подвижное равновесие и осадок не выпадает;
в) Если произведение концентрации ионов (ИП) больше произведения растворимости (ПР), то раствор пересыщен относительно данного труднорастворимого соединения и осадок образуется. Осадок выделяется до тех пор, пока не будет достигнута величина ПР.
II. Из двух труднорастворимых соединений в первую очередь выпадет в осадок тот, чье произведение растворимости (ПР) будет наименьшим.




























