Презентация Производные пирролидина, пиразолона и пиразолидиндиона: их свойства, анализ, хранение, применение онлайн
На нашем сайте вы можете скачать и просмотреть онлайн доклад-презентацию на тему Производные пирролидина, пиразолона и пиразолидиндиона: их свойства, анализ, хранение, применение абсолютно бесплатно. Урок-презентация на эту тему содержит всего 106 слайдов. Все материалы созданы в программе PowerPoint и имеют формат ppt или же pptx. Материалы и темы для презентаций взяты из открытых источников и загружены их авторами, за качество и достоверность информации в них администрация сайта не отвечает, все права принадлежат их создателям. Если вы нашли то, что искали, отблагодарите авторов - поделитесь ссылкой в социальных сетях, а наш сайт добавьте в закладки.
Презентации » Химия » Производные пирролидина, пиразолона и пиразолидиндиона: их свойства, анализ, хранение, применение
Оцените!
Оцените презентацию от 1 до 5 баллов!
- Тип файла:ppt / pptx (powerpoint)
- Всего слайдов:106 слайдов
- Для класса:1,2,3,4,5,6,7,8,9,10,11
- Размер файла:2.28 MB
- Просмотров:85
- Скачиваний:1
- Автор:неизвестен
Слайды и текст к этой презентации:
№2 слайд


Содержание слайда: План
План
Лекарственные средства из группы пирролидина: пирацетам (ноотропил), поливинилпирролидон.
Лекарственные средства – производные пиразолона-5: феназон (антипирин), метамизола натриевая соль (анальгин), пропифеназон.
Лекарственные средства из группы пиразолидин-3,5-диона: фенилбутазон (бутадион), трибузон, кебузон.
Лекарственные средства из группы производных имидазола: тиамазол (мерказолил), метронидазол (трихопол).
Лекарственные средства из группы производных имидазолина (нафазолина нитрат (нафтизин санорин), ксилометазолин (галазолин), клонидина гидрохлорид (клофелин).
Лекарственные средства из группы триазола – тиотриазолин.
№3 слайд

Содержание слайда: Лекарственные средства – производные пирролидина
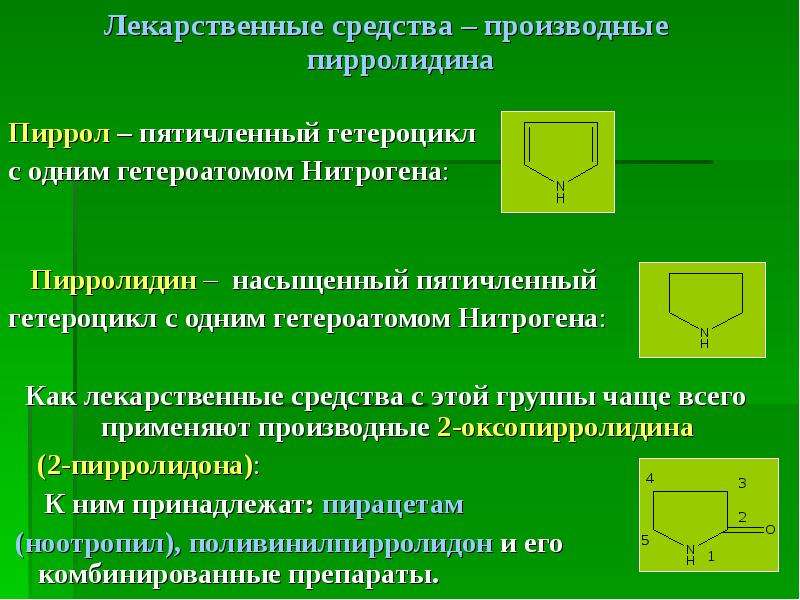
Лекарственные средства – производные пирролидина
Пиррол – пятичленный гетероцикл
с одним гетероатомом Нитрогена:
Пирролидин – насыщенный пятичленный
гетероцикл с одним гетероатомом Нитрогена:
Как лекарственные средства с этой группы чаще всего применяют производные 2-оксопирролидина
(2-пирролидона):
К ним принадлежат: пирацетам
(ноотропил), поливинилпирролидон и его комбинированные препараты.
№10 слайд


Содержание слайда: Комбинированные препараты
Комбинированные препараты
1. Гемодез (Haemodesum) – водно-солевой раствор, содержащий 6 % низкомолекулярного ПВП (М = 12600 2700), йоны Na+, K+, Mg2+, Cl–. Это прозрачная жидкость светло-желтого цвета. За рубежом выпускают под названием Neocompresan.
ПВП связывает токсины с крови больного и быстро выводит их с организма, усиливает диурез, работу почек. Вводят в/в капельно в подогретом до 35–36 С виде взрослым до 300–500 мл, детям по 5–10 мл/кг массы.
2. Неогемодез (Neohaemodesum) – прозрачная жидкость светло-желтого цвета. Отличается от гемодеза меньшей молекулярною массой ПВП (М = 8000 2000).
3. Гемодез-Н – по составу и применению аналогичен неогемодезу, однако отличается несколько измененной технологией приготовления.
4. Глюконеодез – раствор, содержащий ПВП с молекулярной массой М = 8000 2000 – 60 г; глюкозу – 50 г; воду для инъекций – до 1000 мл.
Уменьшение молекулярной массы ПВП ускоряет выведение его из организма почками и улучшает дезинтоксикационные свойства препарата.
№65 слайд


Содержание слайда: 3. Реакция хлороформного раствора препарата с метилйодидом. Если к раствору препарата в хлороформе CHCl3 прибавить метилйодид CH3J, выпадают белые иголчастые кристаллы S-метилмерказолила, имеющего температуру плавления 148 С.
3. Реакция хлороформного раствора препарата с метилйодидом. Если к раствору препарата в хлороформе CHCl3 прибавить метилйодид CH3J, выпадают белые иголчастые кристаллы S-метилмерказолила, имеющего температуру плавления 148 С.
4. Реакция водного раствора препарата с раствором йода. Если к водному раствору препарата прибавить раствор йода J2, то он сперва обесцвечивается, а затем выпадает бурый осадок.
№66 слайд


Содержание слайда: Испытания на чистоту
Испытания на чистоту
1. Прозрачность, цветность и рН раствора
0,2 г препарата растворяют в 10 мл воды. Раствор должен быть прозрачным, бесцветным и нейтральным.
2. Общие примеси хлоридов, сульфатов, тяжелых металлов – в пределах эталонов.
3. Потеря в массе при высушивании. Около 0,5 г (точная навеска) препарата сушат при температуре 100–105 С до постоянной массы. Потеря в массе не должна превышать 0,5 %.
4. Сульфатная зола.
Хранение
Список сильнодействующих веществ. В плотно закупоренном контейнере, в защищенном от света месте.
В. р. д. внутрь 0,01 г.
В. с. д. внутрь 0,04 г.
№67 слайд


Содержание слайда: Количественное определение
Количественное определение
1. Алкалиметрия по заместителю.
Метод состоит в том, что при добавлении AgNO3 образуется нерастворимая Ag-соль и эквивалентное количество нитратной кислоты HNO3, которую титруют раствором NaOH. Еm = М.м.
HNO3 + NaOH → NaNO3 + H2O
Такая же методика количественного определения мерказолила в таблетках 0,005 г, которого должно быть 0,0045–0,0055 г, в пересчете на среднюю массу таблетки.
№88 слайд


Содержание слайда: Свойства
Свойства
Описание. Крист. порошок белого или почти белого цвета.
Растворимость. Растворим в воде Р и 96 % спирте Р, практически нерастворим в СНСІ3 Р и эфире Р. рН водного раствора 4,0–5,0
Идентификация
А. УФ-спектроскопия
УФ-спектр поглощения раствора субстанции в 0,01 М р-ре HCl должен содержать два максимума при 272 нм и 279 нм и плечо при длине волны около 265 нм. Удельный показатель поглощения в максимумах должен быть около 18 и около 16 соответственно.
№91 слайд


Содержание слайда: Испытания на чистоту
Испытания на чистоту
1. Прозрачность раствора. Раствор S (р-р субстанции в воде, свободной от СО2, Р) должен быть прозрачным.
2. Цветность раствора. Окрашивание р-ра S не должно быть более интенсивным, чем определенный эталон.
3. рН. От 4,0 до 5,0. Измеряют рН раствора S.
4. Сопутствующие примеси полупродуктов синтеза определяют методом тонкослойной хроматографии, используя тонкий слой силикагеля G Р.
На хроматограмме испыт. р-ра любое пятно, кроме основного, не должно быть более интенсивным, чем пятно на хроматограмме р-ра сравнения.
5. Потеря в массе при высушивании. Не более 0,5 %. 1,00 г субстанции сушат при темп. от 100 C до 105 C.
6. Сульфатная зола. Не более 0,1 %. Определение проводят с 1,0 г субстанции.
7. N. Остаточные количества органических растворителей.
№93 слайд


Содержание слайда: б) Метод Фольгарда, обратное титрование. Сущность методики состоит в том, что к исследуемому р-ру прибавляют двукратный избыток станд. р-ра AgNO3. Его избыток оттитровывают р-ром NH4SCN в присутствии индикатора (NH4)Fe(SO4)2 до красно-розового окрашивания.
б) Метод Фольгарда, обратное титрование. Сущность методики состоит в том, что к исследуемому р-ру прибавляют двукратный избыток станд. р-ра AgNO3. Его избыток оттитровывают р-ром NH4SCN в присутствии индикатора (NH4)Fe(SO4)2 до красно-розового окрашивания.
КлонидинHCl + AgNO3 КлонидинHNO3 + AgCl↓
AgNO3 + NH4SCN = AgSCN + NH4NO3
3NH4SCN + (NH4)Fe(SO4)2 = Fe(SCN)3 + 2(NH4)2SO4
Еm = М. м.
№94 слайд


Содержание слайда: 3. Ацидиметрия, неводное титрование
3. Ацидиметрия, неводное титрование
Навеску субстанции растворяют в среде ацетангидрида (СН3СО)2О и формиатной кислоты НСООН (или ледяной СН3СООН) и титруют станд. р-ром перхлоратной кислоты HClО4 в присутствии меркурий(ІІ) ацетата Hg(CH3COO)2 (для связывания хлорид-ионов в малодиссоциирующую соль) и индикатора – кристаллического фиолетового (изменение окрашивания с фиолетового до желто-зеленого).
При титровании клонидина гидрохлорида, являющегося солью органического основания, происходят такие химические реакции.
№98 слайд


Содержание слайда: Препарат эффективный в очень малых дозах, которые подбирают индивидуально.
Препарат эффективный в очень малых дозах, которые подбирают индивидуально.
Лечение препаратом необходимо прекращать, постепенно уменьшая дозу (иначе может наступить гипертонический кризис – “симптом ликвидации”.
Во время лечения клофелином запрещается употребление спиртных напитков. Не рекомендуется принимать вместе с антидепрессантами (уменьшение гипотензивного действия) и с большими дозами нейролептиков (усиление седативного эффекта).
Внимание!
Отпускать все лекарственные формы клофелина только по рецепту врача и применять строго по медицинскому назначению.
№100 слайд


Содержание слайда: Получение
Получение
Морфолин смешивают с метиленхлоридом СН2Cl2, затем прибавляют 3-метил-1,2,4-триазолил-5-тиоацетатную кислоту (нерастворима в СН2Cl2) и смесь тщательно перемешивают. Полученный продукт также нерастворим в СН2Cl2. Поэтому осадок отфильтровывают, промывают на фильтре метиленхлоридом СН2Cl2 (экстрагируют возможную примесь морфолина).
№101 слайд


Содержание слайда: Свойства
Свойства
Описание. Белый кристаллический порошок.
Растворимость. Очень легко растворим в воде, растворим в спирте.
Идентификация
1. Реакция на остаток морфолина
Препарат смешивают с NаOH и нагревают на пламени горелки. При внесении к отверстию пробирки красной лакмусовой бумаги наблюдается его посинение (щелочная среда).
2. Реакция на производное тиоацетатной кислоты (получение стирильного производного -СН=СН-С6Н4-)
При прибавлении к препарату п-диметиламинобензальдегида в присутствии смеси ацетангидрида (СН3СО)2О и ледяной СН3СООН (1:4) и нагревании появляется оранжево-коричневое окрашивание.
Скачать все slide презентации Производные пирролидина, пиразолона и пиразолидиндиона: их свойства, анализ, хранение, применение одним архивом:
Похожие презентации
-
 Имидазол. Получение, свойства, анализ, применение, условия хранения лекарственных препаратов производных имидазола
Имидазол. Получение, свойства, анализ, применение, условия хранения лекарственных препаратов производных имидазола -
 Германий, его характеристика, способы получения органопроизводных, химические свойства. Практическое применение
Германий, его характеристика, способы получения органопроизводных, химические свойства. Практическое применение -
 Бор, его характеристика, способы получения органопроизводных, химические свойства. Практическое применение
Бор, его характеристика, способы получения органопроизводных, химические свойства. Практическое применение -
 Гормоны, как лекарственные вещества. Анализ, применение и хранение. (Тема 4)
Гормоны, как лекарственные вещества. Анализ, применение и хранение. (Тема 4) -
 Химические свойства бензола. Получение, применение. Учитель биологии-химии МОУ «СОШ р. п. Озинки» Хорова Людмила Владимировна
Химические свойства бензола. Получение, применение. Учитель биологии-химии МОУ «СОШ р. п. Озинки» Хорова Людмила Владимировна -
 По химии. Спирты, их свойства и применение.
По химии. Спирты, их свойства и применение. -
 Пресс - конференция «Карбоновые кислоты в природе, химические свойства, применение. »
Пресс - конференция «Карбоновые кислоты в природе, химические свойства, применение. » -
 По Химии "Аммиак: состав, строение, свойства, применение" - скачать смотреть
По Химии "Аммиак: состав, строение, свойства, применение" - скачать смотреть -
 По Химии "Альдегиды, свойства, получение, применение" - скачать смотреть
По Химии "Альдегиды, свойства, получение, применение" - скачать смотреть -
 Углерод и его соединения Лекция. (29 -30, с. 172 -178). Цель: Какие соединения образует углерод? Какие свойства, связанные со строением атома углерода, характерны для углерода и его соединений? Где находят применение соединения углерода?
Углерод и его соединения Лекция. (29 -30, с. 172 -178). Цель: Какие соединения образует углерод? Какие свойства, связанные со строением атома углерода, характерны для углерода и его соединений? Где находят применение соединения углерода?