Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
49 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
5.64 MB
Просмотров:
90
Скачиваний:
1
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Учитель химии МБОУ СОШ №79
г. о. Самара
Язрикова Любовь Михайловна
№2 слайд
№3 слайд
№4 слайд
Содержание слайда: Расстановка степеней окисления
Расстановка степеней окисления
Задавать себе главный вопрос: кто в этой реакции отдаёт электроны, а кто их принимает?
Определите, в какой среде (кислой, нейтральной или щелочной) протекает реакция. если в продуктах мы видим кислоту, кислотный оксид — значит, это точно не щелочная среда, а если выпадает гидроксид металла — точно не кислая.
Проверьте, чтобы в реакции был и окислитель, и восстановитель
Если оба вещества могут проявлять свойства и восстановителя, и окислителя — надо продумать, какое из них более активный окислитель. Тогда второй будет восстановителем.
№5 слайд
Содержание слайда: Сначала проставьте коэффициенты, полученные из электронного баланса
Сначала проставьте коэффициенты, полученные из электронного баланса
Если какое-либо вещество выступает и в роли среды, и в роли окислителя (восстановителя) — его надо будет уравнивать позднее, когда почти все коэффициенты расставлены
Предпоследним уравнивается водород
по кислороду мы только проверяем
№6 слайд
Содержание слайда: Расстановка степеней окисления:
Расстановка степеней окисления:
а) степени окисления в водородных соединениях неметаллов: фосфин РН3 — степень окисления у фосфора — отрицательная;
б) в органических веществах — проверьте ещё раз, всё ли окружение атома С учтено
в) аммиак и соли аммония — в них азот всегда имеет степень окисления −3
в) кислородные соли и кислоты хлора — в них хлор может иметь степень окисления +1, +3, +5, +7;
г) двойные оксиды: Fe3O4, Pb3O4 — в них металлы имеют две разные степени окисления, обычно только одна из них участвует в переносе электронов.
№7 слайд
Содержание слайда: 2. Выбор продуктов без учёта переноса электронов — то есть, например, в реакции есть только окислитель без восстановителя или наоборот
2. Выбор продуктов без учёта переноса электронов — то есть, например, в реакции есть только окислитель без восстановителя или наоборот
3. Неверные с химической точки зрения продукты: не может получиться такое вещество, которое вступает во взаимодействие со средой!
а) в кислой среде не может получиться оксид металла, основание, аммиак;
б) в щелочной среде не получится кислота или кислотный оксид;
в) оксид или тем более металл, бурно реагирующие с водой, не образуются в водном растворе.
№8 слайд
№9 слайд
Содержание слайда: Повышение степеней окисления марганца
№10 слайд
Содержание слайда: Дихромат и хромат как окислители.
№11 слайд
Содержание слайда: Повышение степеней окисления хрома
№12 слайд
Содержание слайда: Азотная кислота с металлами.
— не выделяется водород, образуются продукты восстановления азота
№13 слайд
Содержание слайда: Диспропорционирование
Реакции диспропорционирования — это реакции, в которых один и тот же элемент является и окислителем, и восстановителем, одновременно и повышая, и понижая свою степень окисления:
№14 слайд
Содержание слайда: Серная кислота с металлами
№15 слайд
Содержание слайда: Диспропорционирование оксида азота (IV) и солей.
№16 слайд
№17 слайд
Содержание слайда: Задание С2 предложено в двух форматах.
Задание С2 предложено в двух форматах.
В одних вариантах КИМ оно будет предложено в прежнем формате
а в других в новом, когда условие задания представляет собой описание конкретного химического эксперимента, ход которого экзаменуемый должен будет отразить посредством уравнений соответствующих реакций.
№18 слайд
Содержание слайда: С2.1. (ПРЕЖНИЙ ФОРМАТ) – 4 БАЛЛА.
ДАНЫ ВЕЩЕСТВА: ОКСИД АЗОТА (IV), МЕДЬ, РАСТВОР ГИДРОКСИДА КАЛИЯ И КОНЦЕНТРИРОВАННАЯ СЕРНАЯ КИСЛОТА. НАПИШИТЕ УРАВНЕНИЯ ЧЕТЫРЕХ ВОЗМОЖНЫХ РЕАКЦИЙ МЕЖДУ ВСЕМИ ПРЕДЛОЖЕННЫМИ ВЕЩЕСТВАМИ, НЕ ПОВТОРЯЯ ПАРЫ РЕАГЕНТОВ.
С2.2.(В НОВОМ ФОРМАТЕ) – 4 БАЛЛА. СОЛЬ, ПОЛУЧЕННУЮ ПРИ РАСТВОРЕНИИ ЖЕЛЕЗА В ГОРЯЧЕЙ КОНЦЕНТРИРОВАННОЙ СЕРНОЙ КИСЛОТЕ, ОБРАБОТАЛИ ИЗБЫТКОМ РАСТВОРА ГИДРОКСИДА НАТРИЯ. ВЫПАВШИЙ БУРЫЙ ОСАДОК ОТФИЛЬТРОВАЛИ И ПРОКАЛИЛИ. ПОЛУЧЕННОЕ ВЕЩЕСТВО СПЛАВИЛИ С ЖЕЛЕЗОМ. НАПИШИТЕ УРАВНЕНИЯ ОПИСАННЫХ РЕАКЦИЙ.
№19 слайд
Содержание слайда: 1 или 2 реакции обычно «лежат на поверхности», демонстрируя либо кислотные, либо основные свойства вещества
1 или 2 реакции обычно «лежат на поверхности», демонстрируя либо кислотные, либо основные свойства вещества
В наборе из четырех веществ, как правило, встречаются типичные окислители и восстановители. В этом случае как минимум одна представляют собой ОВР
Для написания реакций между окислителем и восстановителем необходимо:
1. предположить, до какого возможного значения повысится степень окисления атома-восстановителя и в каком продукте реакции он будет ее проявлять;
2. предположить, до какого возможного значения понизится степень окисления атома-окислителя и в каком продукте реакции он будет ее проявлять.
№20 слайд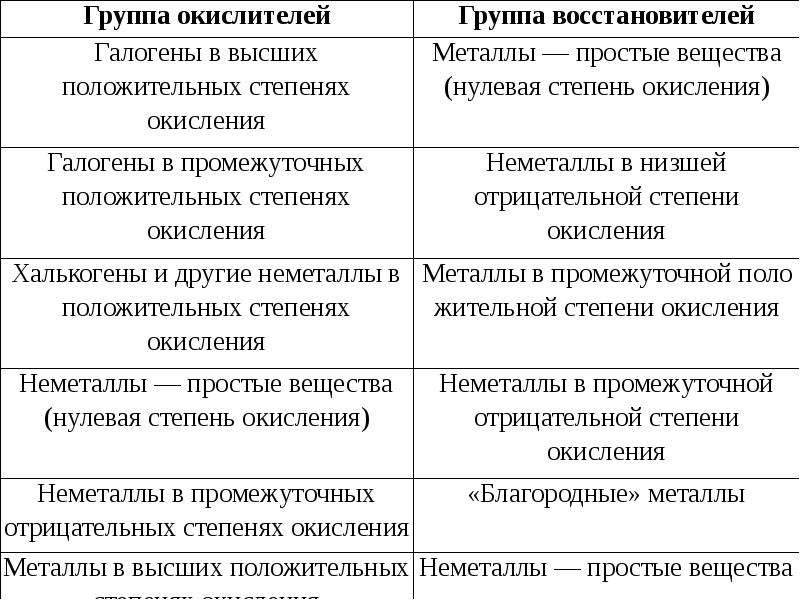
Содержание слайда: Типичные окислители и восстановители в порядке ослабления окислительных и восстановительных свойств
№21 слайд
Содержание слайда: Даны четыре вещества: оксид азота (IV), иодоводород, раствор гидроксида калия, кислород.
Даны четыре вещества: оксид азота (IV), иодоводород, раствор гидроксида калия, кислород.
№22 слайд
№23 слайд
Содержание слайда: Общие свойства классов органических веществ
Общие свойства классов органических веществ
Общие способы получения органических веществ
Специфические свойства некоторых конкретных веществ
№24 слайд
№25 слайд
Содержание слайда: Основные превращения бензола и его производных
№26 слайд
Содержание слайда: Получение азотсодержащих
органических веществ
№27 слайд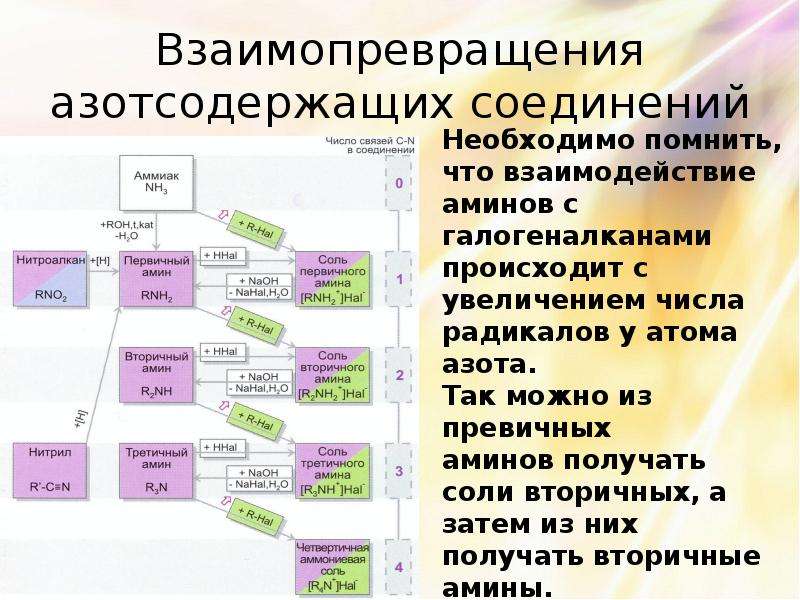
Содержание слайда: Взаимопревращения азотсодержащих соединений
№28 слайд
Содержание слайда: Окислительно-восстановительные свойства кислородсодержащих соединений
№29 слайд
Содержание слайда: Получение производных карбоновых кислот
№30 слайд
Содержание слайда: Генетическая связь
между производными карбоновых кислот
№31 слайд
№32 слайд
№33 слайд
Содержание слайда: Классификация задач
№34 слайд
№35 слайд
№36 слайд
№37 слайд
№38 слайд
№39 слайд
№40 слайд
№41 слайд
Содержание слайда: Вывод формул
№42 слайд
№43 слайд
№44 слайд
№45 слайд
№46 слайд
№47 слайд
№48 слайд
№49 слайд
Содержание слайда: Список использованной литературы и интернет – ресурсов.


























































