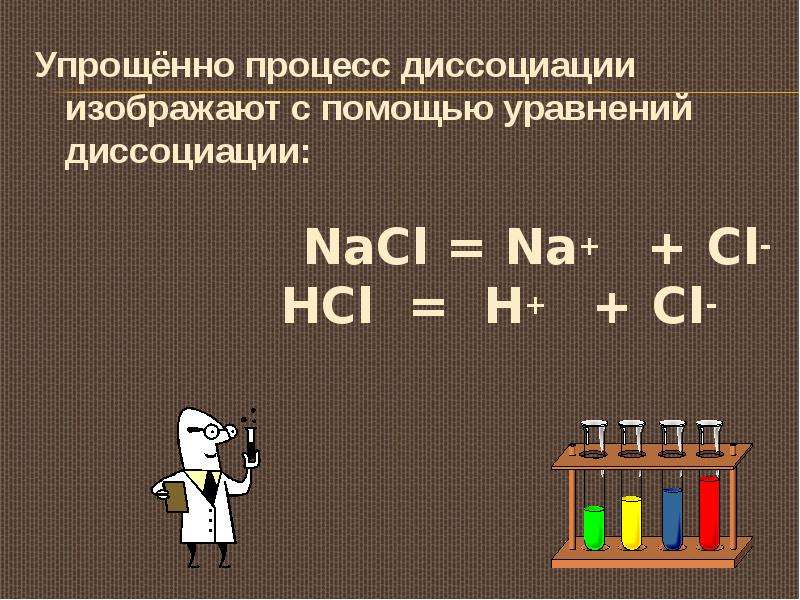Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
19 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
2.64 MB
Просмотров:
106
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Выполнила учитель химии и экологи МОУ «СОШ с. Усть-Курдюм» Филимонова И.В.
8 класс
№2 слайд
Содержание слайда: Все вещества по их способности проводить электрический ток в растворах делятся на электролиты и неэлектролиты
№3 слайд
Содержание слайда: Электролиты
Электролиты
(водные растворы
проводят эл.ток)
№4 слайд
Содержание слайда: Укажите вид связи и принадлежность данных веществ к электролитам и неэлектролитам: KCl, O2 , HNO3 ,CuO.
Укажите вид связи и принадлежность данных веществ к электролитам и неэлектролитам: KCl, O2 , HNO3 ,CuO.
Назовите из перечня веществ электролиты (не забудьте воспользоваться таблицей растворимости !): BaCl2 , CaO, H2 SO4 , NaOH, Cl2 , Zn(OH)2
№5 слайд
Содержание слайда: В РАСТВОРАХ ЭЛЕКТРОЛИТЫ ДИССОЦИИРУЮТ, Т.Е. РАСПАДАЮТСЯ НА ИОНЫ.
В РАСТВОРАХ ЭЛЕКТРОЛИТЫ ДИССОЦИИРУЮТ, Т.Е. РАСПАДАЮТСЯ НА ИОНЫ.
№6 слайд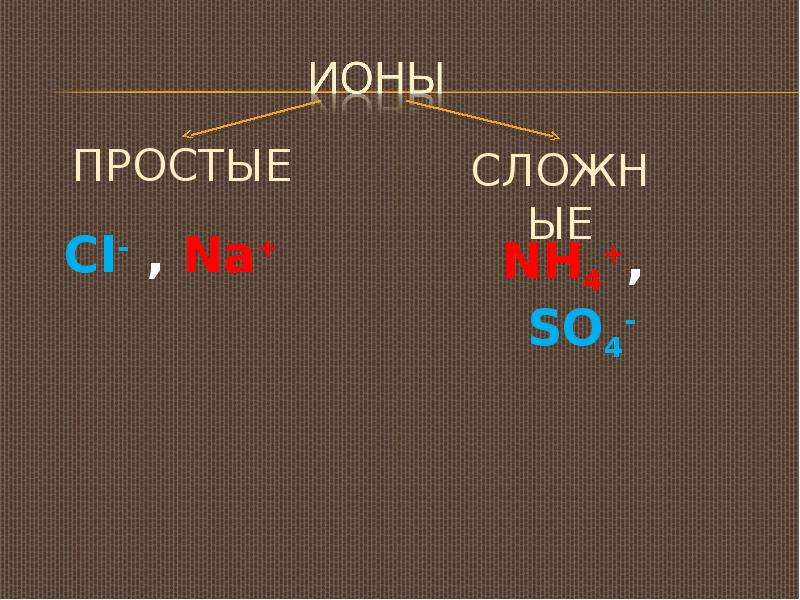
Содержание слайда: ПРОСТЫЕ
ПРОСТЫЕ
№7 слайд
Содержание слайда: Вещества с ионной связью:
Вещества с ионной связью:
Ориентация
диполей воды
гидратация
диссоциация.
№8 слайд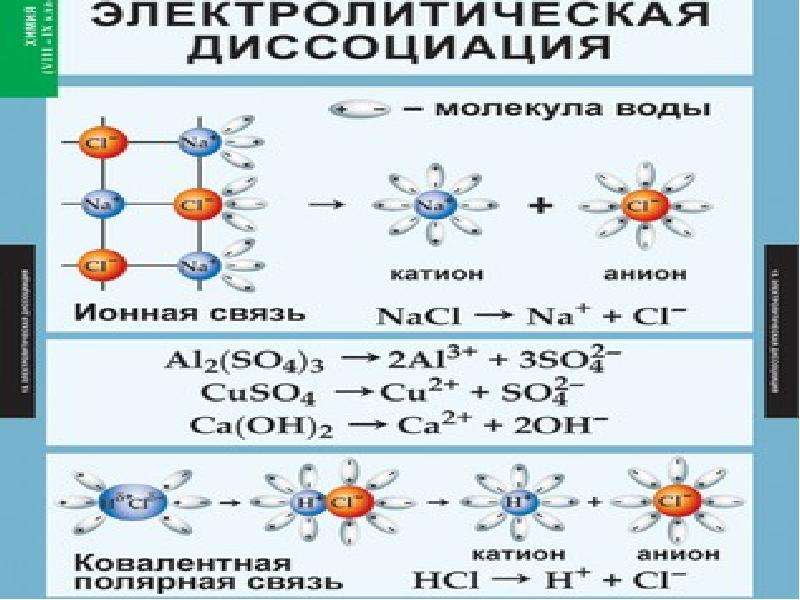
№9 слайд
Содержание слайда: Под действием электрического тока положительные ионы движутся к катоду и называются катионами, а отрицательные – к аноду и называются анионами.
Под действием электрического тока положительные ионы движутся к катоду и называются катионами, а отрицательные – к аноду и называются анионами.
№10 слайд
№11 слайд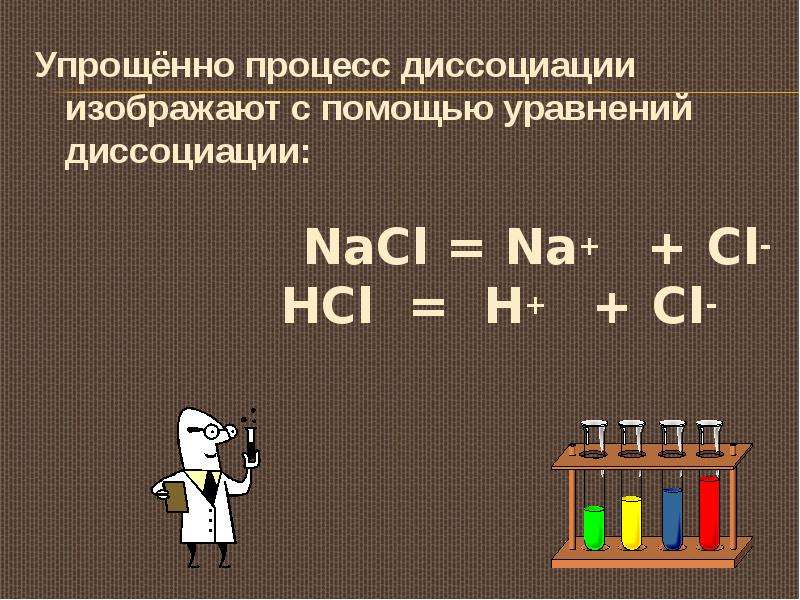
Содержание слайда: Упрощённо процесс диссоциации изображают с помощью уравнений диссоциации:
NaCl = Na+ + Cl-
HCl = H+ + Cl-
№12 слайд
Содержание слайда: Назовите частицы: а) H, H2 , H+ ; б) Cl2 , Cl, Cl- .
Назовите частицы: а) H, H2 , H+ ; б) Cl2 , Cl, Cl- .
Назовите катионы и анионы в соединениях, формулы которых: CuCl2 , AgNO3 , Ca(OH)2 , H3 PO4 .
№13 слайд
Содержание слайда: Разные электролиты по-разному диссоциируют на ионы и поэтому делятся на:
Разные электролиты по-разному диссоциируют на ионы и поэтому делятся на:
Сильные (соли, щелочи, некоторые кислоты –
HCl, HNO3, H2SO4, у которых ά → 1;
Слабые (гидрат аммиака NH4*H2O, некоторые кислоты – HNO2, H2SO3, H2S, H2CO3 , у которых ά → 0.
№14 слайд
Содержание слайда: Свойства растворов электролитов определяются свойствами тех ионов, которые они образуют при диссоциации.
Свойства растворов электролитов определяются свойствами тех ионов, которые они образуют при диссоциации.
По характеру образующихся ионов различают три типа электролитов:
Кислоты – это электролиты, которые диссоциируют на катионы водорода и анионы кислотного остатка.
№15 слайд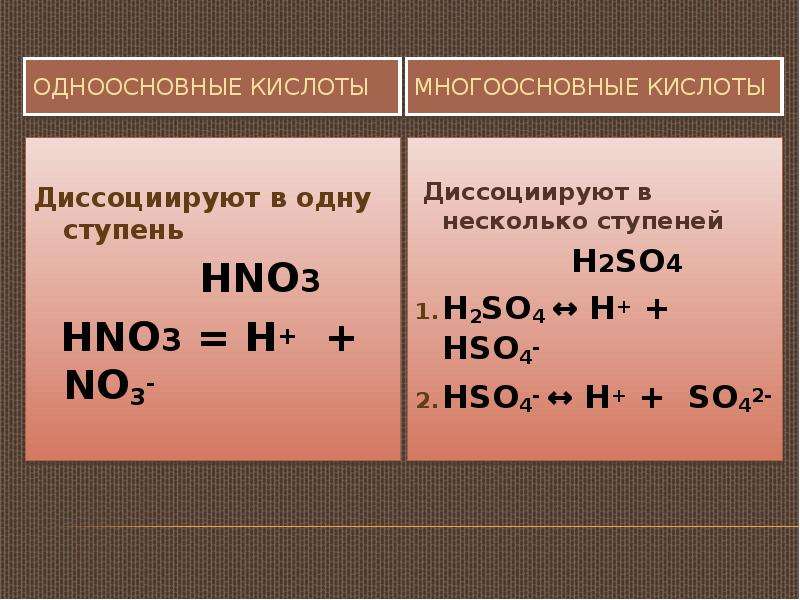
Содержание слайда: ОДНООСНОВНЫЕ КИСЛОТЫ
№16 слайд
Содержание слайда: ОДНОКИСЛОТНЫЕ ОСНОВАНИЯ
ОДНОКИСЛОТНЫЕ ОСНОВАНИЯ
№17 слайд
Содержание слайда: Независимо от числа катионов и анионов кислотного остатка средние соли диссоциируют в одну ступень:
Независимо от числа катионов и анионов кислотного остатка средние соли диссоциируют в одну ступень:
Al2(SO4) = 2Al3+ + 3SO42-
№18 слайд
Содержание слайда: Напишите уравнения диссоциации следующих веществ: HCl, H3PO4, KOH
Напишите уравнения диссоциации следующих веществ: HCl, H3PO4, KOH
№19 слайд
Содержание слайда: § 36, упр. № 1, 4, 5.
§ 36, упр. № 1, 4, 5.