Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
43 слайда
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
549.50 kB
Просмотров:
96
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
Внутренняя энергия. Работа и теплота.
Теплоемкость идеального газа
№2 слайд
Содержание слайда: Внутренняя энергия. Работа и теплота
Наряду с механической энергией любое тело (или система) обладает внутренней энергией. Внутренняя энергия – энергия покоя. Она складывается из теплового хаотического движения молекул, составляющих тело, потенциальной энергии
их взаимного расположения, кинетической и потенциальной энергии электронов в атомах, нуклонов в ядрах и так далее.
№3 слайд
Содержание слайда: В термодинамике важно знать не абсолютное значение внутренней энергии, а её изменение.
В термодинамических процессах изменяется только кинетическая энергия движущихся молекул. Следовательно, фактически под внутренней энергией в термодинамике подразумевают энергию теплового хаотического движения молекул.
№4 слайд
Содержание слайда: Внутренняя энергия U одного моля идеального газа равна:
или
Таким образом, внутренняя энергия зависит только от температуры. Внутренняя энергия U является функцией состояния системы независимо от предыстории.
№5 слайд
Содержание слайда: В общем случае термодинамическая система может обладать как внутренней, так и механической энергией и разные системы могут обмениваться этими видами энергии.
Обмен механической энергией характеризуется совершенной работой А, а обмен внутренней энергией – количеством переданного тепла Q.
№6 слайд
Содержание слайда: Количество теплоты, сообщаемой телу, идёт на увеличение внутренней энергии тела и на совершение телом работы:
– это и есть первое начало термодинамики или закон сохранения энергии в термодинамике.
№7 слайд
Содержание слайда: В дифференциальном виде первое начало термодинамики будем иметь :
U – функция состояния системы; dU – её полный дифференциал, а δQ и δА таковыми не являются.
№8 слайд
Содержание слайда: Особое значение в термодинамике имеют круговые или циклические процессы, при которых система, пройдя ряд состояний, возвращается в исходное.
№9 слайд
Содержание слайда: Для цикла из первого начала термодинамики
Следовательно, нельзя построить периодически действующий двигатель, который совершал бы бóльшую работу, чем количество сообщенной ему извне энергии.
Одна из формулировок первого начала термодинамики: невозможно создать вечный двигатель первого рода.
№10 слайд
Содержание слайда: Теплоёмкость идеального газа. Уравнение Майера
Теплоёмкость тела характеризуется количеством теплоты, необходимой для нагревания этого тела на один градус
№11 слайд
Содержание слайда: Для газов удобно пользоваться молярной теплоемкостью Сμ количество теплоты, необходимое для нагревания 1 моля газа на 1 градус.
№12 слайд
Содержание слайда: Теплоёмкость термодинамической системы зависит от того, как изменяется состояние системы при нагревании.
Если газ нагревать при постоянном объёме, то всё подводимое тепло идёт на нагревание газа, то есть изменение его внутренней энергии. Теплоёмкость при этом обозначается СV.
№13 слайд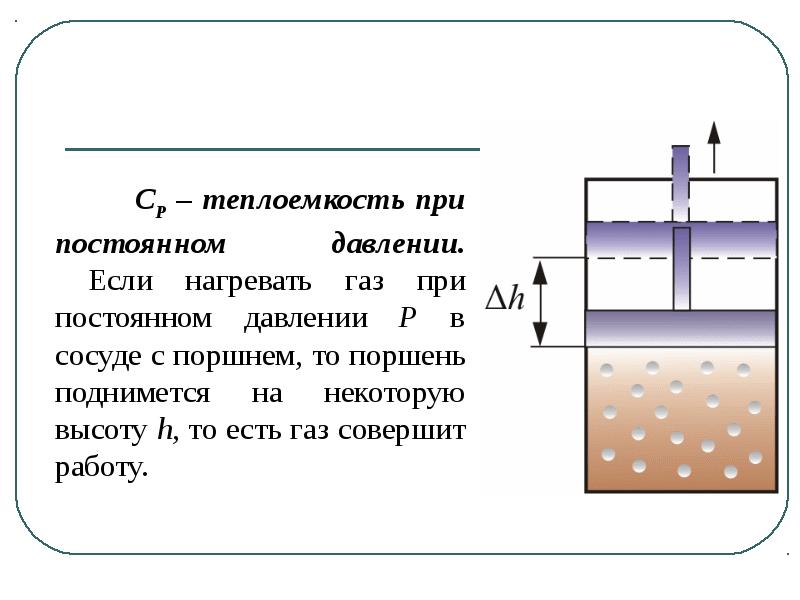
Содержание слайда: СР – теплоемкость при постоянном давлении.
Если нагревать газ при постоянном давлении Р в сосуде с поршнем, то поршень поднимется на некоторую высоту h, то есть газ совершит работу.
№14 слайд
Содержание слайда: Следовательно, подводимое тепло затрачивается и на нагревание и на совершение работы. Отсюда ясно, что
Величины СР и СV оказываются связанными простым соотношением.
№15 слайд
Содержание слайда: При нагревании одного моля идеального газа при постоянном объёме, первое начало термодинамики запишется в виде:
Теплоемкость при постоянном объёме будет равна:
№16 слайд
Содержание слайда: В общем случае
так как U может зависеть не только от температуры.
В случае идеального газа справедлива формула
Из этого следует, что
№17 слайд
Содержание слайда: Внутренняя энергия идеального газа является только функцией температуры (и не зависит от V, Р), поэтому формула
справедлива для любого процесса.
Для произвольной идеальной массы газа:
№18 слайд
Содержание слайда: При изобарическом процессе кроме увеличения внутренней энергии происходит совершение работы газом:
Из уравнения Клапейрона-Менделеева
Подставив полученный результат в уравнение, получим
№19 слайд
Содержание слайда: Это уравнение Майера для одного моля газа. Из него следует физический смысл универсальной газовой постоянной . R – численно равна работе, совершаемой одним молем газа при нагревании на один градус при изобарическом процессе.
№20 слайд
Содержание слайда: Теплоёмкости одноатомных и многоатомных газов
Внутренняя энергия одного моля идеального газа равна
№21 слайд
Содержание слайда: Теплоёмкости одноатомных газов
Теплоемкость при постоянном объеме СV – величина постоянная, от температуры не зависит.
№22 слайд
№23 слайд
Содержание слайда: Полезно знать отношение:
где γ коэффициент Пуассона
№24 слайд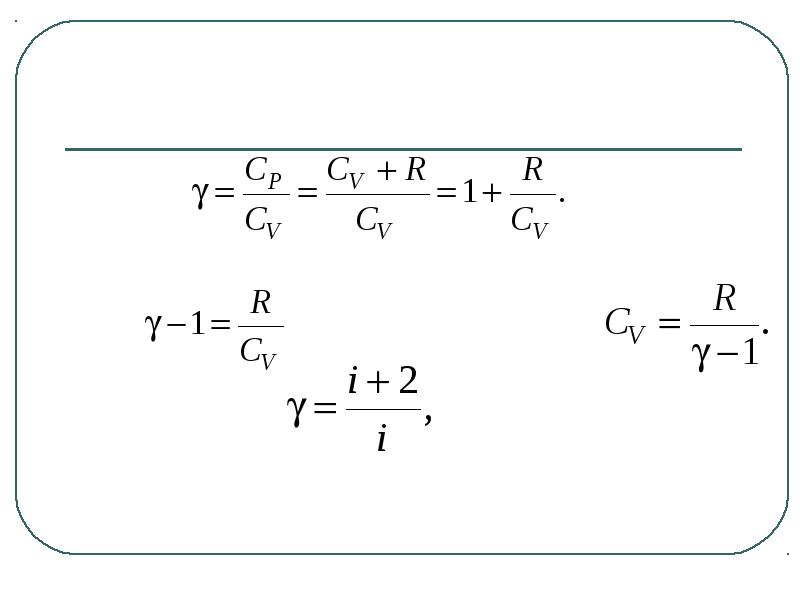
Содержание слайда: Так как
Тогда . Из этого следует, что
Кроме того
где i – число степеней свободы молекул.
№25 слайд
Содержание слайда: Подставив в выражение для внутренней энергии, получим:
а так как , то
внутреннюю энергию можно найти по формуле:
№26 слайд
Содержание слайда: Необходимо учитывать вращательное и колебательное движение молекул. Число степеней свободы таких молекул
№27 слайд
Содержание слайда: Числом степени свободы называется число независимых переменных, определяющих положение тела в пространстве и обозначается i
Как видно, положение материальной точки (одноатомной молекулы) задаётся тремя координатами, поэтому она имеет три степени свободы.
№28 слайд
Содержание слайда: Многоатомная молекула может ещё и вращаться. Например, у двухатомных молекул вращательное движение можно разложить на два независимых вращения. Любое вращение можно разложить на три вращательных движения вокруг взаимно перпендикулярных осей. Но для двухатомных молекул вращение вокруг оси z не изменит её положение в пространстве.
№29 слайд
№30 слайд
№31 слайд
Содержание слайда: У двухатомных жестких молекул пять степеней свободы (i = 5), а у трёхатомных шесть степеней свободы (i = 6).
Если молекула не жесткая, то она обладает еще колебательными степенями свободы. На каждую колебательную степень свободы приходится энергия, равная
приходится на кинетическую энергию и
на потенциальную .
№32 слайд
Содержание слайда: Больцман доказал, что, средняя энергия, приходящаяся на одну степень свободы равна
№33 слайд
Содержание слайда: На среднюю кинетическую энергию молекулы, имеющей i-степеней свободы приходится
Это и есть закон Больцмана о равномерном распределении средней кинетической энергии по степеням свободы.
№34 слайд
Содержание слайда: В общем случае, для молярной массы газа
№35 слайд
Содержание слайда: Для произвольного количества газов:
,
№36 слайд
Содержание слайда: Применение первого начала термодинамики к изопроцессам
Используем I начало термодинамики или закон сохранения энергии в термодинамике
№37 слайд
Содержание слайда: Изотермический процесс
Изотермический процесс
Изохорический процесс
№38 слайд
Содержание слайда: Изобарический процесс
Изобарический процесс
Адиабатный процесс
№39 слайд
Содержание слайда: Рассмотрим политропный процесс – такой процесс, при котором изменяются все основные параметры системы, кроме теплоемкости, т.е. С = const.
Уравнение политропы
№40 слайд
Содержание слайда: С помощью показателя n можно легко описать любой изопроцесс:
1. Изобарный процесс Р = const, n = 0
2. Изотермический процесс Т = const, n = 1,
№41 слайд
Содержание слайда: Изохорный процесс
Изохорный процесс
Адиабатический процесс Q = 0, n = γ,
Сад = 0.
№42 слайд
Содержание слайда: Во всех этих процессах работу можно вычислить по одной формуле:
№43 слайд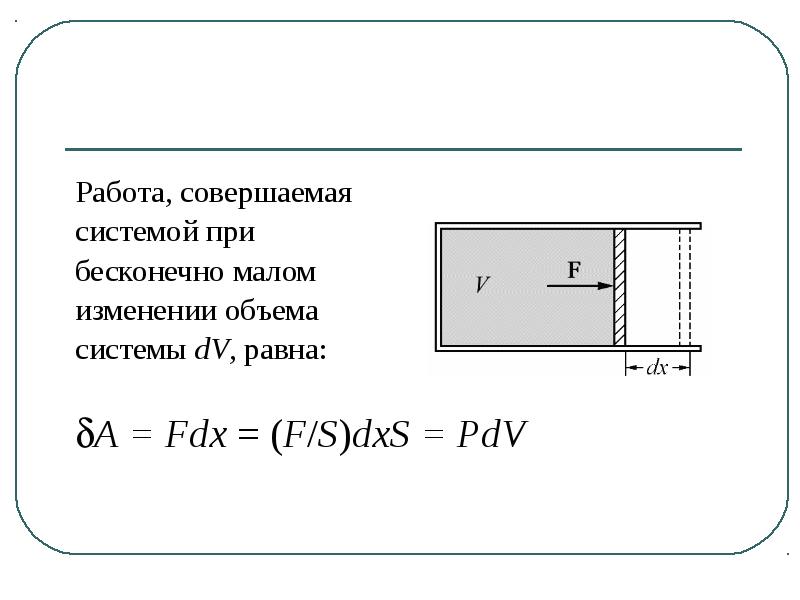
Содержание слайда: Работа, совершаемая
Работа, совершаемая
системой при
бесконечно малом
изменении объема
системы dV, равна:
A = Fdx = (F/S)dxS = PdV




















































