Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
15 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
3.02 MB
Просмотров:
63
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: АЛЮМИНИЙ
Овчинникова Ольга Анатольевна
Учитель химии
МБОУ Российская гимназия № 59 г.Улан-Удэ
№2 слайд
Содержание слайда: АЛЮМИНИЙ.
нахождение в природе
Алюмосиликаты:
Глина – Al2O3*nSiO2*mH2O
Бокситы – Al2O3*nH2O
№3 слайд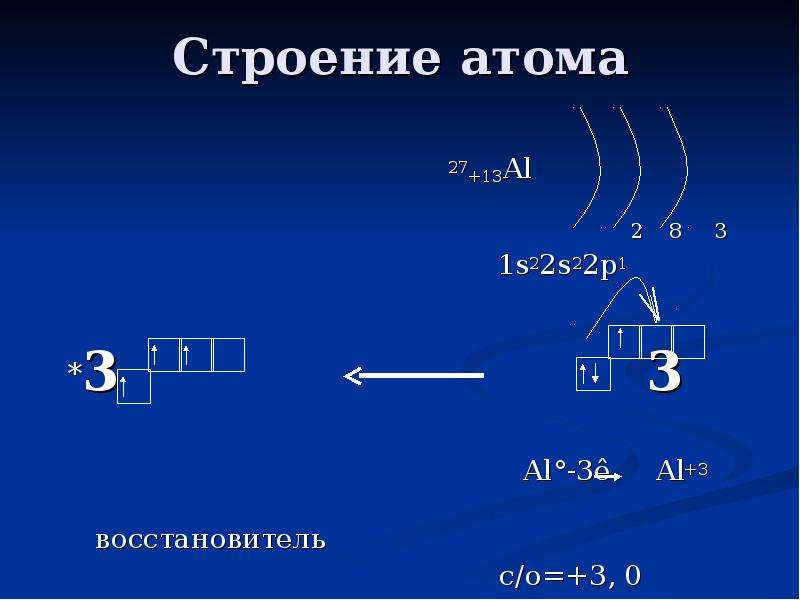
Содержание слайда: Строение атома
27+13Al
2 8 3
1s22s22p1
*3 3
Al°-3ê Al+3
восстановитель
с/о=+3, 0
№4 слайд
Содержание слайда: ФИЗИЧЕСКИЕ СВОЙСТВА
Al-серебристо-белый металл
Мягкий, пластичный (легко вытягивается в проволоку и раскатывается в листы), легкий (плотность 2,7г/см3)
Хорошо проводит тепло и электрический ток
Температура плавления - 660°С
Особо чистый Аl хорошо отражает солнечные лучи
№5 слайд
Содержание слайда: ХИМИЧЕСКИЕ СВОЙСТВА
Al – активный металл. На воздухе всегда покрыт пленкой Al2O3. Поэтому при обычных условиях не вступает во взаимодействие с другими веществами.
№6 слайд
Содержание слайда: ВЗАИМОДЕЙСТВИЕ С ПРОСТЫМИ ВЕЩЕСТВАМИ
При нагревании
Взаимодействие с углеродом:
4Al+3C=Al4C3 (1500-1700°C)
Взаимодействие с серой:
2Al+3S= Al2S3 (150-170°C)
№7 слайд
Содержание слайда: Взаимодействие со сложными веществами
Взаимодействие с водой (очищенный от оксидной пленки)
Al +H2O=Al(OH)3 +H2
Подберите коэффициенты
№8 слайд
Содержание слайда: Взаимодействие со сложными веществами
Взаимодействие с водой (очищенный от оксидной пленки)
2 Al +6H2O=2Al(OH)3 +3H2
Взаимодействует с растворами кислот
Al +HCl= AlCl3 + H2
Подберите коэффициенты
№9 слайд
Содержание слайда: Взаимодействие со сложными веществами
Взаимодействие с водой (очищенный от оксидной пленки)
2 Al +6H2O=2Al(OH)3 +3H2
Взаимодействует с растворами кислот
2Al +6HCl= 2AlCl3 + 3H2
Взаимодействует с растворами щелочей
Al+ NaOH + H2O=Na[Al(OH)4]+H2
тетрагидроксоалюминат
натрия
Подберите коэффициенты
№10 слайд
Содержание слайда: Взаимодействие со сложными веществами
Взаимодействие с водой (очищенный от оксидной пленки)
2 Al +6H2O=2Al(OH)3 +3H2
Взаимодействует с растворами кислот
2Al +6HCl= 2AlCl3 + 3H2
Взаимодействует с растворами щелочей
2Al+ 2NaOH + 6H2O=2Na[Al(OH)4]+3H2
тетрагидроксоалюминат
натрия
№11 слайд
Содержание слайда: Алюминий при обычных условиях не взаимодействует с концентрированными H2SO4 и
HNO3
№12 слайд
Содержание слайда: ПРИМЕНЕНИЕ АЛЮМИНИЯ
№13 слайд
Содержание слайда: ПРИМЕНЕНИЕ АЛЮМИНИЯ
№14 слайд
Содержание слайда: Домашнее задание
§ 13 (до соединений алюминия)
Работа с текстом конспекта
Подберите коэффициенты методом электронного баланса:
Al + H2SO4= Al2(SO4)3 + SO2 + H2O
Al + HNO3 = Al(NO3)3 + NO2 + H2O
№15 слайд
Содержание слайда: Ссылки на источники используемого материала:
http://s019.radikal.ru/i606/1204/27/74062dfcc275.jpg
[URL=http://www.radikal.ru][IMG]http://s019.radikal.ru/i606/1204/27/74062dfcc275.jpg[/IMG][/URL]
[URL=http://radikal.ru/F/s019.radikal.ru/i606/1204/27/74062dfcc275.jpg.html][IMG]http://s019.radikal.ru/i606/1204/27/74062dfcc275t.jpg[/IMG][/URL]
























