Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
30 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
3.75 MB
Просмотров:
47
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Учитель химии
МБОУ СОШ № 9 МО ЩР
станица Новощербиновская
Степучева Ольга Викторовна
№2 слайд
Содержание слайда: Повторить свойства металлов и неметаллов
Повторить свойства металлов и неметаллов
Изучить строениеатомов, свойства галогенов на основании их сравнительной характеристики.
№3 слайд
№4 слайд
Содержание слайда: 1 вариант – неметаллы
1 вариант – неметаллы
2, 4, 5, 7, 10, 11, 13, 15
2 вариант – металлы
1, 2, 3, 6, 8, 9, 12, 14
№5 слайд
№6 слайд
№7 слайд
№8 слайд
№9 слайд
Содержание слайда: «рождающие соли»
«рождающие соли»
№10 слайд
№11 слайд
№12 слайд
№13 слайд
№14 слайд
Содержание слайда: F2
F2
Ядовитый
газ
светло-
зелёного
цвета
№15 слайд
Содержание слайда: CI2 -
CI2 -
Ядовитый
газ
жёлто-зеленого цвета
№16 слайд
Содержание слайда: Br2
Br2
Токсичная
тяжёлая
жидкость
красно- бурого цвета
№17 слайд
№18 слайд
Содержание слайда: Число электронов на внешнем энергетическом уровне атома;
Число электронов на внешнем энергетическом уровне атома;
Изменение радиуса атомов и окислительно-восстановительных свойств галогенов в подгруппе;
Возможные степени окисления.
Тип химической связи
Тип кристаллической решетки
№19 слайд
Содержание слайда: На внешнем энергетическом уровне галогены содержат 7 электронов.
На внешнем энергетическом уровне галогены содержат 7 электронов.
В главной подгруппе с увеличением зарядов ядер, увеличиваются радиусы атомов, нарастают восстановительные свойства.
Возможные степени окисления: -1, +7.
Ковалентная неполярная связь
Молекулярная кристаллическая решетка.
№20 слайд
№21 слайд
№22 слайд
Содержание слайда: 2KI + Br2 = 2 KBr + I2 ,
но KBr + I2
№23 слайд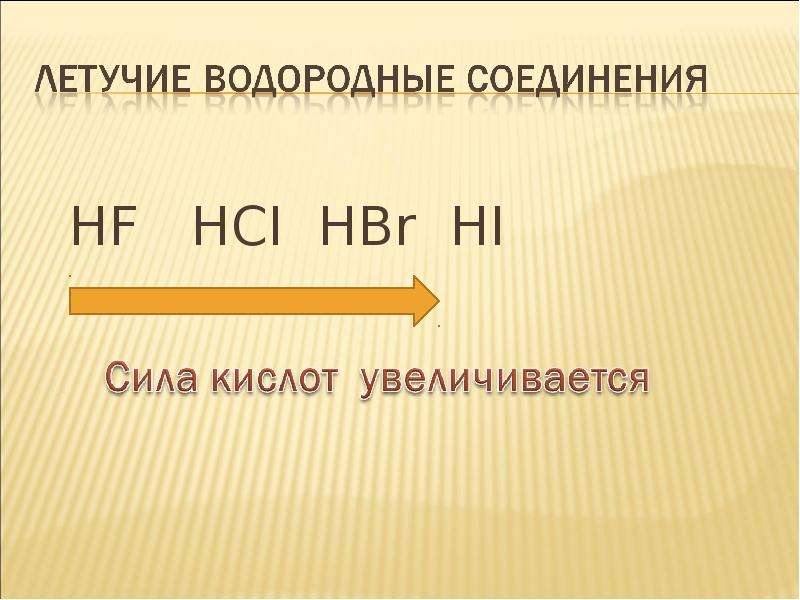
Содержание слайда: HF HCI HBr HI
№24 слайд
№25 слайд
№26 слайд
Содержание слайда: Перечислите галогены.
Перечислите галогены.
Фтор, хлор, бром, йод, астат.
Где в ПСХЭ располагаются галогены?
в VII группе, главной подгруппе.
Чему равно число валентных электронов в атомах галогенов ?
Число валентных электронов равно семи.
№27 слайд
Содержание слайда: Сопоставьте :
Сопоставьте :
Хлор красно – бурая жидкость
Бром светло – зеленый газ
Йод жёлто – зелёный газ
Фтор твёрдый с металлическим
блеском пары фиолетового цвета
№28 слайд
Содержание слайда: Дополните:
Дополните:
Самый сильный неметалл –
фтор.
Самая сильная бескислородная кислота –
HI.
Как изменяются окислительные свойства галогенов?
Уменьшаются в ряду F CI Br I
№29 слайд
Содержание слайда: Домашнее задание
Домашнее задание
№30 слайд
Содержание слайда: Изображение хлора и брома:
Изображение хлора и брома:
http://ru.wikipedia.org/wiki/
Изображение периодической системы д.И. Менделеева:
http://steelbros.ru/threads/%D…
Изображение морского прибоя:
http://misterforex.ru/gdefon/w…
Изображение флюорита:
http://geo.web.ru/







































