Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
53 слайда
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
3.69 MB
Просмотров:
75
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Лекция 2. Электронная природа химической связи. Кристаллические и аморфные вещества
№2 слайд
№3 слайд
№4 слайд
Содержание слайда: Ковалентная связь –
это связь за счет общих
электронных пар
№5 слайд
Содержание слайда: Метод валентных схем
№6 слайд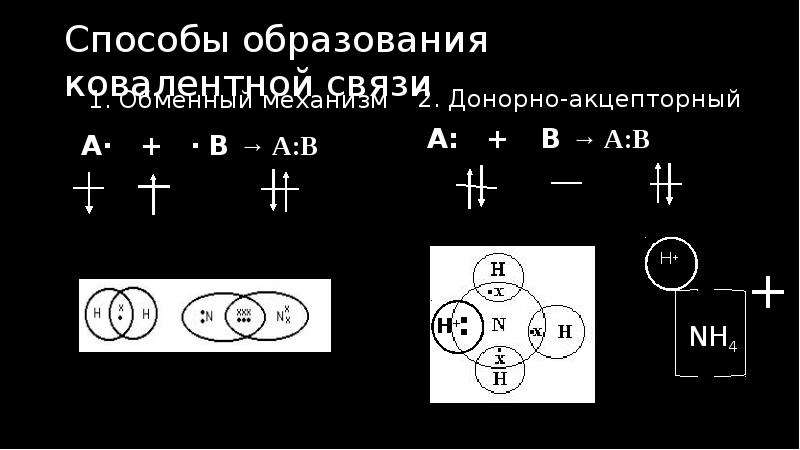
Содержание слайда: Способы образования ковалентной связи
№7 слайд
Содержание слайда: Способы перекрывания атомных орбиталей
№8 слайд
Содержание слайда: Свойства ковалентной связи:
1. Кратность связи
2. Длина связи
3. Энергия связи
4. Направленность связи
5. Полярность связи
6. Насыщаемость связи
№9 слайд
Содержание слайда: Кратность ковалентной связи
– это число общих электронных пар
№10 слайд
Содержание слайда: Длина связи - расстояние между ядрами связанных атомов
№11 слайд
№12 слайд
№13 слайд
№14 слайд
Содержание слайда: Направленность ковалентной связи – это
№15 слайд
Содержание слайда: Гибридизация атомных орбиталей при образовании ковалентных связей
Гибридизацией называется гипотетический процесс смешения различного типа, но близких по энергии орбиталей данного атома (АО) с возникновением того же числа новых (гибридных) орбиталей, одинаковых
по энергии и форме.
Форма гибридной АО отличается от формы исходных АО.
Чаще всего встречаются гибридизации sp, sp2, sp3. Каждому типу гибридизации соответствует определенное пространственное строение молекул вещества.
№16 слайд
№17 слайд
№18 слайд
№19 слайд
№20 слайд
Содержание слайда: Важно!
Число гибридных орбиталей равно числу исходных;
Гибридные орбитали ориентируются в пространстве таким образом, чтобы обеспечить максимальное удаление друг от друга;
Гибридные орбитали принимают участие в образовании только -связей;
Каждая гибридная орбиталь имеет долю s-составляющей и долю р-составляющей. Чем больше доля р-составляющей, тем более вытянута орбиталь;
Чем больше доля s-составляющей, тем меньше размер орбитали и тем больше электроотрицательность атома (ЭО (С sр) ЭО (С sр2 ) ЭО (С sр3).
№21 слайд
Содержание слайда: Задание: определите геометрию следующих молекул BeCl2, BH3 SiCl4
№22 слайд
Содержание слайда: Полярность ковалентной связи
№23 слайд
Содержание слайда: Полярность связи
№24 слайд
Содержание слайда: Полярность молекулы
№25 слайд
№26 слайд
Содержание слайда: Задание: Определите, полярны ли молекулы воды и углекислого газа
№27 слайд
№28 слайд
Содержание слайда: Валентные возможности атомов
№29 слайд
№30 слайд
№31 слайд
№32 слайд
№33 слайд
Содержание слайда: Строение веществ с ковалентными связями
№34 слайд
Содержание слайда: Характеристики веществ с атомной кристаллической решеткой
№35 слайд
№36 слайд
Содержание слайда: Характеристики веществ с молекулярной кристаллической решеткой
№37 слайд
Содержание слайда: Ионная связь – это связь между разноименно заряженными ионами-анионом и катионом
№38 слайд
№39 слайд
№40 слайд
№41 слайд
Содержание слайда: Свойства веществ с ионными связями
№42 слайд
Содержание слайда: Задание: Установите соответствие формулы вещества типу химической связи, который реализуется в данном соединении.
№43 слайд
№44 слайд
№45 слайд
Содержание слайда: Металлическая связь
№46 слайд
№47 слайд
Содержание слайда: Кристаллические решетки металлов
№48 слайд
Содержание слайда: Аморфные вещества
№49 слайд
Содержание слайда: Взаимодействие между молекулами
Строение и свойства веществ определяются не только химическими связями, но и межмолекулярными взаимодействиями.
№50 слайд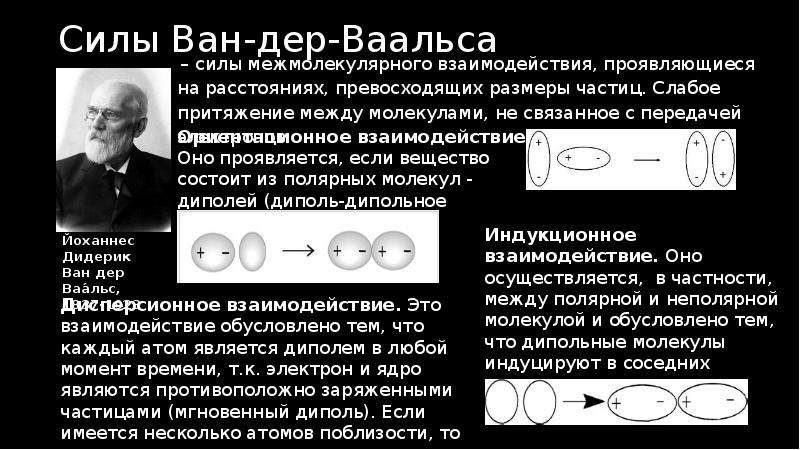
Содержание слайда: Силы Ван-дер-Ваальса
№51 слайд
Содержание слайда: Водородная связь
№52 слайд
№53 слайд






























































