Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
23 слайда
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
517.75 kB
Просмотров:
65
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
№2 слайд
Содержание слайда: Разделите вещества на группы
AlCl3, O2, Al, SO3, Na, HCl, Cl2, Na2S
№3 слайд
Содержание слайда: Классификация веществ в зависимости от типа химической связи
Ионная AlCl3, Na2S
Ковалентная полярная SO3, HCl
Ковалентная неполярная O2, Cl2
Металлическая Al, Na
№4 слайд
Содержание слайда: Ионная Al3+Cl-3, Na+12S2-
Ионная Al3+Cl-3, Na+12S2-
Ковалентная полярная
Sδ+O δ-3, H δ+Cl δ-
S+6O -23, H +1Cl -1
№5 слайд
Содержание слайда: Степень окисления
это заряд,
№6 слайд
Содержание слайда: Правила определения
cтепени окисления
№7 слайд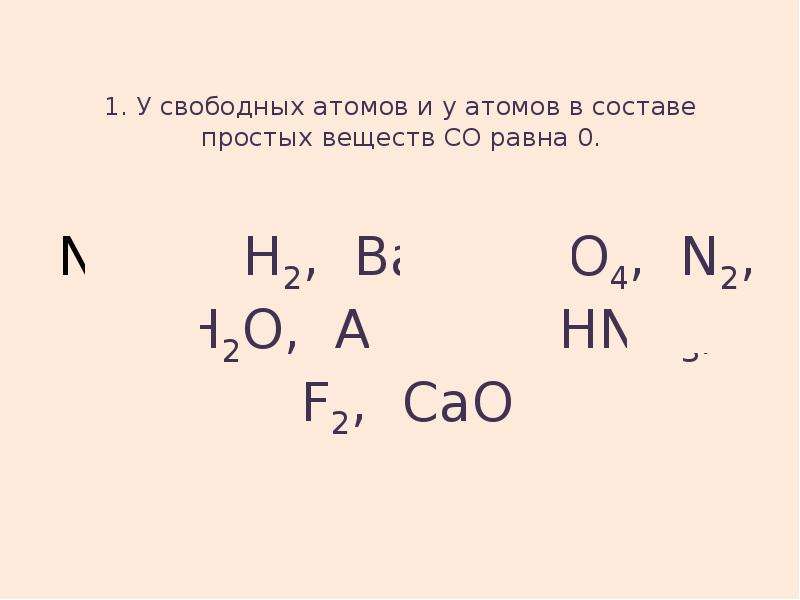
Содержание слайда: 1. У свободных атомов и у атомов в составе простых веществ СО равна 0.
Na2O, H2, Ba, H2SO4, N2, S, H2O, Al, Cu, HNO3, F2, CaO
№8 слайд
Содержание слайда: 2. Металлы во всех соединениях имеют положительную СО, её максимальное значение равно номеру группы:
А) у металлов главной подгруппы I группы +1
Б) у металлов главной подгруппы II группы +2
В) у металлов главной подгруппы III группы +3
Na, K2O, Fe, CaCO3, CrO3, AlCl3, Li3N, BaSO4, Zn, Mg(NO3)2, Mn2O7
№9 слайд
№10 слайд
Содержание слайда: 3. Неметаллы в соединениях имеют положительную и отрицательную степень окисления.
Её максимальное значение равно номеру группы, а минимальное можно рассчитать по формуле
СО = № группы - 8
SO3, H2S, NH3, N2O5, HCl, Cl2O7
№11 слайд
Содержание слайда: 4. В соединениях кислород
имеет СО -2
(исключения OF2 и пероксиды Н2О2, К2О2)
H2CO3, O3, OF2, CuSO4, NaOH, O2, SO3
№12 слайд
Содержание слайда: 5. У водорода в соединениях
с неметаллами СО +1,
с металлами -1
HCl, KH, H2, KOH, BaH2, H2O, H2SO4, NH3
№13 слайд
Содержание слайда: 6. В соединениях
сумма степеней окисления
всех атомов равна 0.
№14 слайд
Содержание слайда: Группа 1
Группа 1
N2+1O-2, N-3 H3+1,
N2+5O5-2, Fe2+3O3-2,
Al2+3S3-2
№15 слайд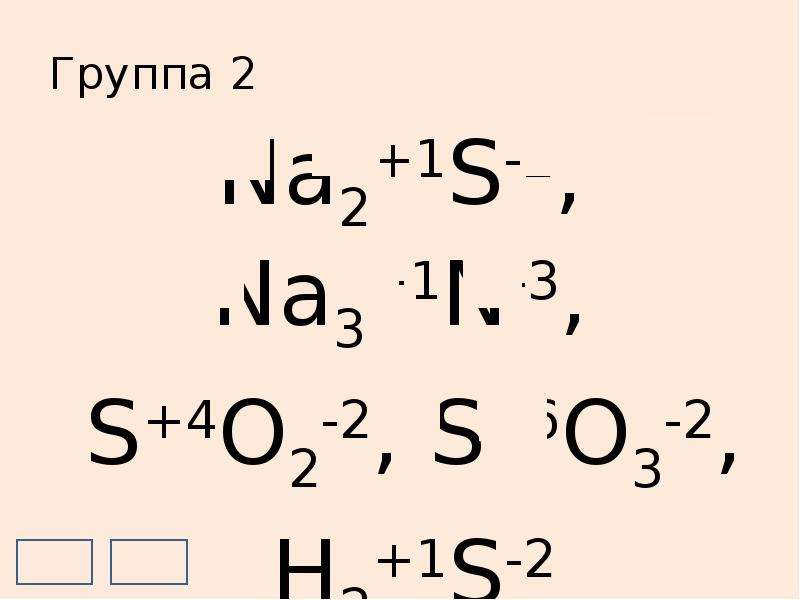
Содержание слайда: Группа 2
Na2+1S-2, Na3+1N-3,
S+4O2-2, S+6O3-2,
H2+1S-2
№16 слайд
Содержание слайда: Группа 3
Mg+2S-2, Mg3+2N2-3,
P2+5O5-2, P-3H3+1,
P2+3O3-2
№17 слайд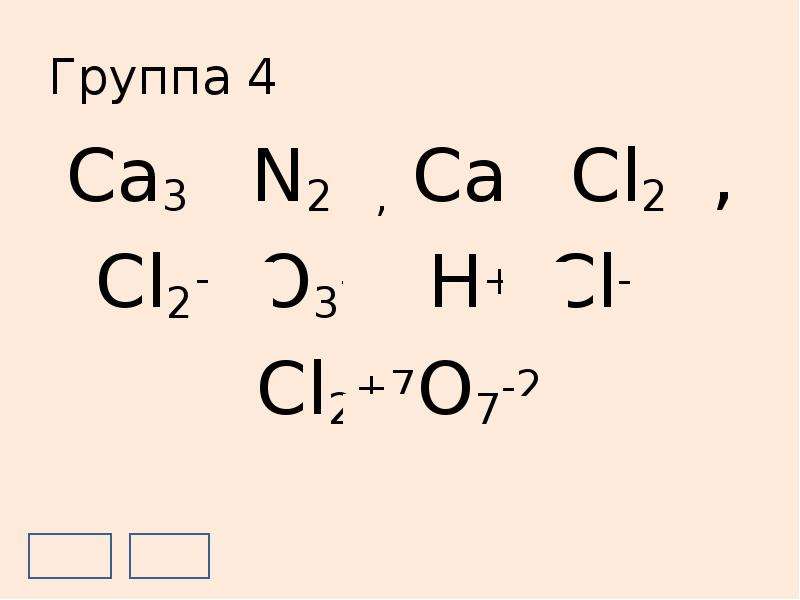
Содержание слайда: Группа 4
Ca3+2N2-3, Ca+2Cl2-1,
Cl2+3O3-2, H+1Cl-1,
Cl2+7O7-2
№18 слайд
Содержание слайда: Алгоритм определения
cтепени окисления
Запишем значение постоянной степени окисления.
Умножим значение постоянной степени окисления на число атомов элемента.
Полученное число разделим на число атомов второго элемента.
Полученное число – значение степени окисления второго элемента.
Необходимо помнить, что сумма степеней окисления элементов в соединении равна 0.
№19 слайд
Содержание слайда: Алгоритм определения
cтепени окисления
Составим уравнение. Для этого
определим значение постоянной степени окисления и умножим его на число атомов элемента;
неизвестную степень окисления обозначим Х и умножим на число атомов элемента;
сложим полученные произведения;
их сумма равна 0, так как сумма степеней окисления элементов в соединении равна 0.
№20 слайд
Содержание слайда: Группа 6
K3P, K3PO4, KF, С+4S2-2, SiH4
№21 слайд
Содержание слайда: На уроке я узнал ….
На уроке я узнал ….
На уроке я научился …
Сегодня мне удалось…
При подготовке домашнего задания мне надо обратить внимание на ….
Я хочу узнать …
№22 слайд
Содержание слайда: Степень окисления. Определение степени окисления по формуле вещества.
№23 слайд
Содержание слайда: Домашнее задание
1. Прочитайте текст §18 с. 100 – 104
2. Выучите определение и правила.
3. Выполните задания 5, 7 на с. 106
































