Презентация Физическая химия дисперсных систем. Коллоидные растворы онлайн
На нашем сайте вы можете скачать и просмотреть онлайн доклад-презентацию на тему Физическая химия дисперсных систем. Коллоидные растворы абсолютно бесплатно. Урок-презентация на эту тему содержит всего 31 слайд. Все материалы созданы в программе PowerPoint и имеют формат ppt или же pptx. Материалы и темы для презентаций взяты из открытых источников и загружены их авторами, за качество и достоверность информации в них администрация сайта не отвечает, все права принадлежат их создателям. Если вы нашли то, что искали, отблагодарите авторов - поделитесь ссылкой в социальных сетях, а наш сайт добавьте в закладки.
Презентации » Химия » Физическая химия дисперсных систем. Коллоидные растворы
Оцените!
Оцените презентацию от 1 до 5 баллов!
- Тип файла:ppt / pptx (powerpoint)
- Всего слайдов:31 слайд
- Для класса:1,2,3,4,5,6,7,8,9,10,11
- Размер файла:415.00 kB
- Просмотров:82
- Скачиваний:0
- Автор:неизвестен
Слайды и текст к этой презентации:
№4 слайд


Содержание слайда: Немного истории…
До начала XX века наука о коллоидах содержала описание свойств отдельных высокодисперсных систем и способы их приготовления
М.В. Ломоносов, Ловиц, Рейсс, Ф.Сельми, М.Фарадей – внесли неоценимый вклад в развитие коллоидной химии
Томас Грэм (1861) – «отец» коллоидной химии; ввел термин и определил понятие «коллоиды»
№5 слайд


Содержание слайда: По Т. Грэму
Кристаллоиды – вещества быстро диффундирующие и проходящие через растительные и животные мембраны, легко кристаллизующиеся
Растворы кристаллоидов – истинные растворы
Коллоиды – вещества, обладающие очень малой диффузией, не проходящие через мембраны и не кристаллизующиеся, а образующие аморфные осадки
Растворы коллоидов – золи
№6 слайд


Содержание слайда: По И.Г. Борщеву
В зависимости от условий одно и то же вещество может проявлять свойства кристаллической и коллоидной форм
Р-р NaCl в воде – истинный раствор,
Р-р NaCl в бензоле – коллодный
Мыло в воде – коллоид
Мыло в спирте – кристаллоид
Можно говорить лишь о коллоидном и кристаллоидном состоянии того или иного вещества
№11 слайд


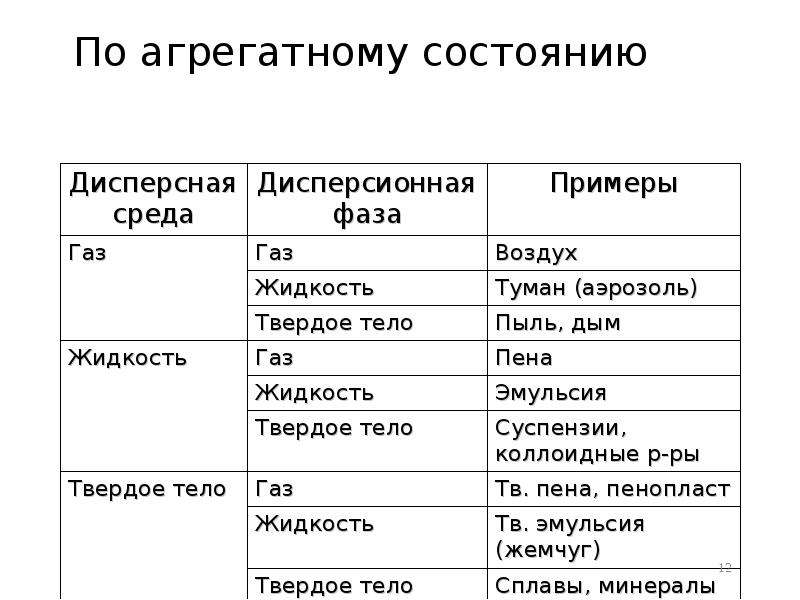
Содержание слайда: Классификация дисперсных систем
По величине частиц дисперсной фазы
Грубодисперсные (больше 10-7м). Быстро оседают, видимы в микроскоп, остаются на бумажном фильтре, неустойчивы (суспензии, эмульсии, взвеси)
Коллоидно-дисперсные (10-7-10-9м). Относительно устойчивы
Молекулярно- и ионно-дисперсные. Гомогенны, устойчивы (истинные растворы)
№13 слайд


Содержание слайда: Классификация коллоидных растворов
По интенсивности взаимодействия частиц на поверхности раздела фаз:
Лиофильные – сильное взаимодействие; устойчивы, обратимы (взаимодействие полярных групп веществ с полярными жидкостями или неполярных групп с неполярными жидкостями)
Лиофобные – взаимодействие частиц только при добавлении стабилизаторов; необратимы (металлы в коллоидном состоянии, эмульсии)
№15 слайд


Содержание слайда: Условия получения коллоидов
Дисперсная фаза должна обладать плохой растворимостью
Размеры диспергируемого вещества должны быть доведены до размеров коллоидных частиц (10-7-10-9м)
Необходимы стабилизаторы, которые на поверхности раздела фаз образуют ионный или молекулярный слой и гидратную оболочку
№18 слайд
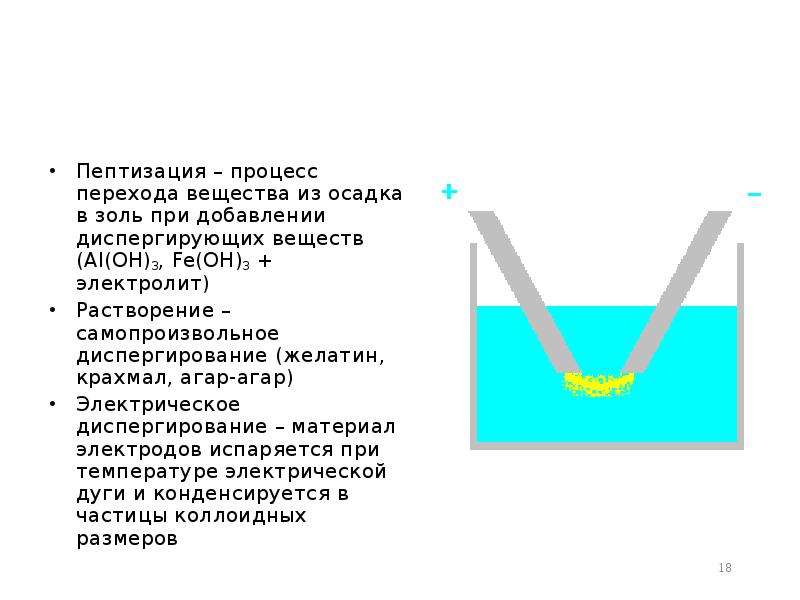

Содержание слайда: Пептизация – процесс перехода вещества из осадка в золь при добавлении диспергирующих веществ (Al(OH)3, Fe(OH)3 + электролит)
Пептизация – процесс перехода вещества из осадка в золь при добавлении диспергирующих веществ (Al(OH)3, Fe(OH)3 + электролит)
Растворение – самопроизвольное диспергирование (желатин, крахмал, агар-агар)
Электрическое диспергирование – материал электродов испаряется при температуре электрической дуги и конденсируется в частицы коллоидных размеров
№20 слайд


Содержание слайда: Нейтрализация
Нейтрализация
Ca(OH)2 + H2SO4 CaSO4 + 2H2O
Замена растворителя
При вливании спиртовых растворов серы, канифоли, в воду, в которой эти вещества плохо растворимы, они начинают конденсироваться в частицы коллоидных размеров и могут находиться во взвешенном состоянии
№25 слайд


Содержание слайда: Применение седиментационного анализа
Определение размера и фракционного состава частиц (число частиц разного размера)
Определение молекулярного веса полимерных материалов, белков, нуклеиновых кислот
Качественная оценка функционального состояния эритроцитов. СОЭ значительно меняется при различных заболеваниях
№30 слайд


Содержание слайда: осм (1% золь золота) = 0,00045 атм
осм (1% золь золота) = 0,00045 атм
осм (1% раствор сахарозы) = 0,725 атм
Осмотическое давление коллоидных растворов со временем уменьшается (частицы самоукрупняются или оседают, и их в растворе становится меньше)
Часть измеряемого осмотического давления в коллоидных растворах обусловлена примесью электролитов
№31 слайд


Содержание слайда: Роль коллоидов
Кровь, лимфа, плазма, спинномозговая жидкость, протоплазма – коллоидные системы, в которых ряд веществ (белки, гликоген, липиды) находятся в коллоидном состоянии
Могут связывать большие количества воды (соединительная ткань, стекловидное тело)
Коллоиды различных тканей живых организмов обуславливают многообразие их свойств: эластичность, набухание, коагуляция, сохранение той или иной формы
Многие основные операции в фармацевтической промышленности – коллоидные процессы (изготовление эмульсий, порошков, кремов, мазей)
Введение лекарств в коллоидной форме локализует их действие и увеличивает срок их действия
Скачать все slide презентации Физическая химия дисперсных систем. Коллоидные растворы одним архивом:
Похожие презентации
-
 Физико-химия дисперсных систем. Коллоидные растворы
Физико-химия дисперсных систем. Коллоидные растворы -
 Дисперсные (коллоидные) системы и растворы
Дисперсные (коллоидные) системы и растворы -
 Химия. Дисперсные системы. Растворы
Химия. Дисперсные системы. Растворы -
 Дисперсные системы. Свойства коллоидных растворов
Дисперсные системы. Свойства коллоидных растворов -
 Поверхностные явления и дисперсные системы (коллоидная химия)
Поверхностные явления и дисперсные системы (коллоидная химия) -
 Физическая химия дисперсных систем
Физическая химия дисперсных систем -
 Физическая химия тугоплавких неметаллических и силикатных материалов. Дисперсные системы. (Лекции 1-3)
Физическая химия тугоплавких неметаллических и силикатных материалов. Дисперсные системы. (Лекции 1-3) -
 Классификация дисперсных систем. Электрокинетические свойства и устойчивость коллоидных растворов. (Лекция 8)
Классификация дисперсных систем. Электрокинетические свойства и устойчивость коллоидных растворов. (Лекция 8) -
 Скачать презентацию Дисперсные системы и растворы
Скачать презентацию Дисперсные системы и растворы -
 Растворы (дисперсные системы)
Растворы (дисперсные системы)