Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
39 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
893.88 kB
Просмотров:
75
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
№2 слайд
Содержание слайда: Классификация дисперсных систем. Электрокинетические свойства и устойчивость коллоидных растворов
Лекция №8
№3 слайд
Содержание слайда: Коллоидная химия ‒ …
… наука о поверхностных явлениях и дисперсных системах.
… наука о коллоидном состоянии вещества.
… физика и химия реальных тел.
№4 слайд
Содержание слайда: Основные понятия:
Дисперсность ‒ мерой её служит удельная поверхность (Sуд). Sуд ‒ площадь раздела фаз, приходящаяся на единицу массы или объёма дисперсной фазы.
Sуд = 6 · а-1
Гетерогенность ‒ мерой её служит поверхностное натяжение (σ ‒ величина энергии единицы поверхности).
№5 слайд
№6 слайд
№7 слайд
№8 слайд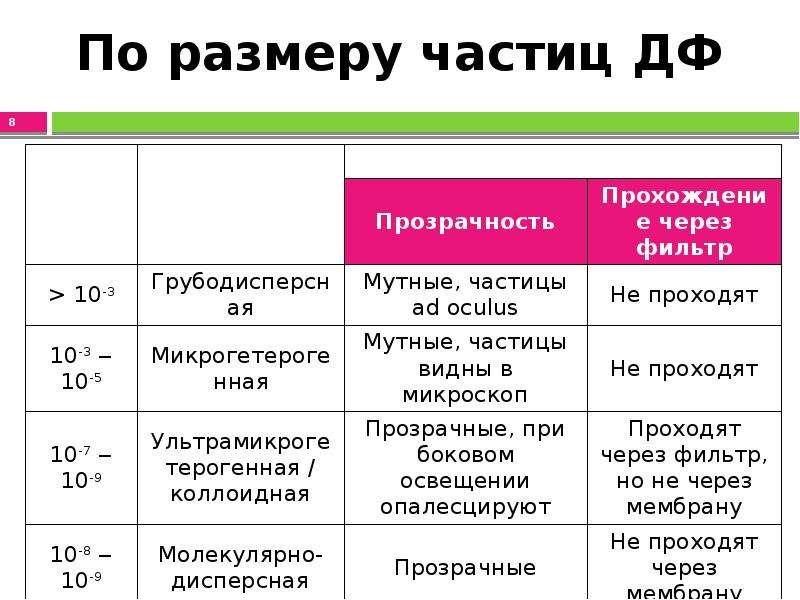
Содержание слайда: По размеру частиц ДФ
№9 слайд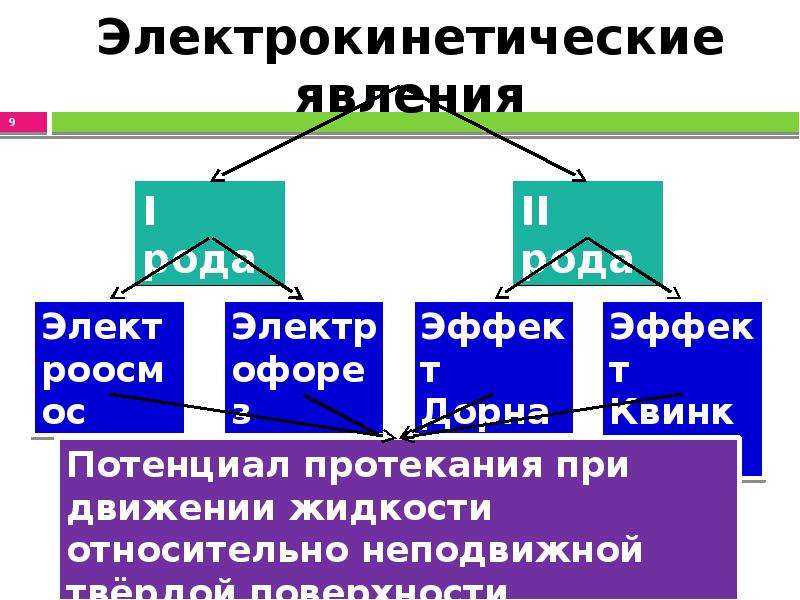
Содержание слайда: Электрокинетические явления
№10 слайд
Содержание слайда: Мицеллярная теория лиофобных золей
Мицелла ‒ гетерогенная микросистема, состоящая из микрокристалла ДФ, окружённого сольватированными ионами стабилизатора.
В мицелле выделяют следующие части:
‒ микрокристаллы ДФ; их число определяют «m».
№11 слайд
Содержание слайда: Мицеллярная теория лиофобных золей
– агрегат с адсорбированными на нём потенциалопределяющими ионами (ПОИ).
– ионы, сообщающие заряд коллоидной частице; находят по правилу Панета – Фаянса – Гана. Их число определяют «n».
– ионы, заряд которых противоположен заряду ПОИ.
№12 слайд
Содержание слайда: Мицеллярная теория лиофобных золей
– ядро с адсорбционным слоем противоионов, являющаяся гигантским многозарядным ионом.
Источником ПОИ и противоионов являются стабилизаторы – электролиты (один из реагентов, продукт реакции, постороннее вещество).
№13 слайд
Содержание слайда: Получение золя конденсационным методом по реакции обмена
№14 слайд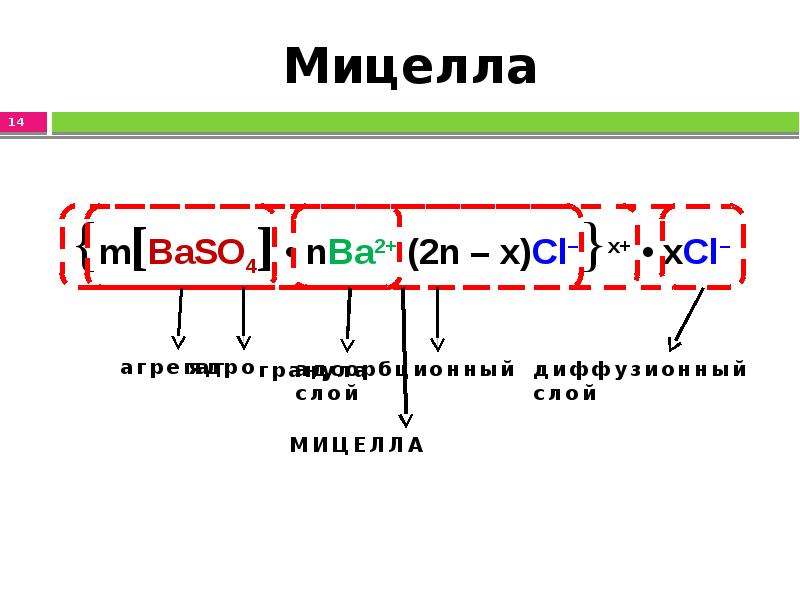
Содержание слайда: Мицелла
№15 слайд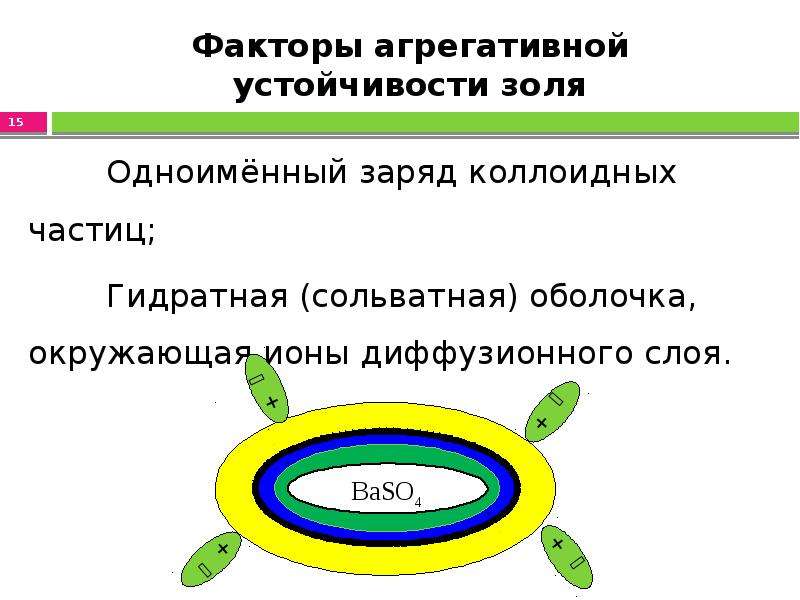
Содержание слайда: Факторы агрегативной устойчивости золя
Одноимённый заряд коллоидных частиц;
Гидратная (сольватная) оболочка, окружающая ионы диффузионного слоя.
№16 слайд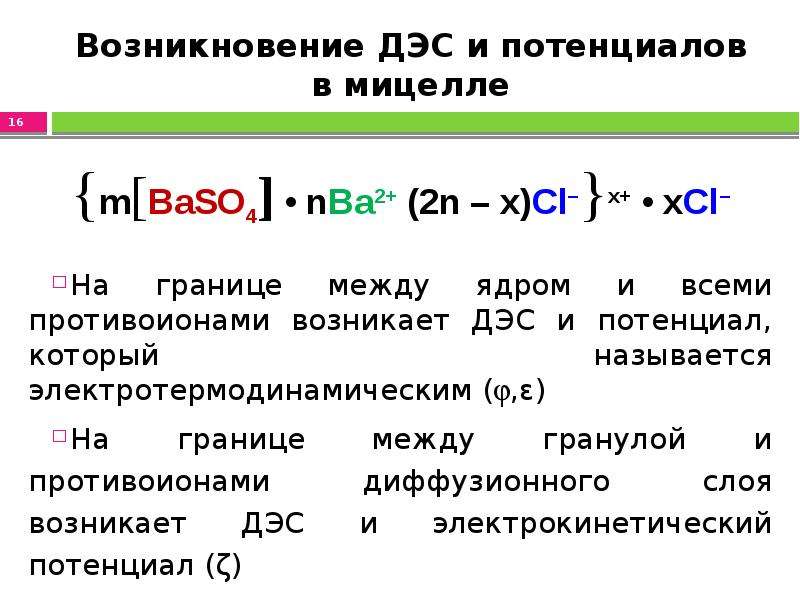
Содержание слайда: Возникновение ДЭС и потенциалов в мицелле
На границе между ядром и всеми противоионами возникает ДЭС и потенциал, который называется электротермодинамическим (,ε)
На границе между гранулой и противоионами диффузионного слоя возникает ДЭС и электрокинетический потенциал (ζ)
№17 слайд
Содержание слайда: Возникновение ДЭС и потенциалов в мицелле
По величине 0 ≤ ζ < . При ζ = 0 имеет место изоэлектрическая точка золя (ИЭТ), в которой происходит полное разрушение золя.
ζкрит. = ±30 мВ. При этом значении золь начинает разрушаться.
Т.о., по величине ζ можно судить об устойчивости золя: чем больше ζ, тем устойчивее золь.
№18 слайд
Содержание слайда: Факторы, влияющие на ζ
Концентрация стабилизатора.
Состояние ИЭТ золя, ζ = 0. Золь разрушается.
Концентрация посторонних электролитов.
При введении посторонних электролитов, ионы которых обладают более высокой адсорбционной способностью, чем ионы стабилизатора, возможна перезарядка частиц золя.
№19 слайд
№20 слайд
Содержание слайда: Расчёт ζ
Поскольку ζ обнаруживает себя при попадании мицеллы в электрическое поле, для его расчёта используются данные электрофореза и электроосмоса.
№21 слайд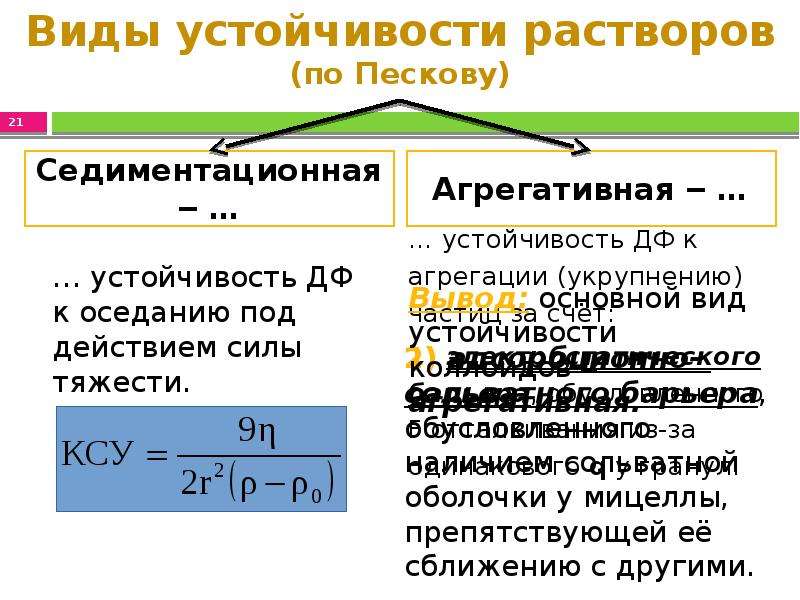
Содержание слайда: Виды устойчивости растворов (по Пескову)
… устойчивость ДФ к агрегации (укрупнению) частиц за счёт:
1) электростатического барьера, обусловленного F отталкивания из-за одинакового q у гранул.
№22 слайд
Содержание слайда: Коагуляция ‒ …
… процесс слипания частиц, образование крупных агрегатов с потерей седиментационной и фазовой устойчивости и последующим разделением фаз.
… процесс уменьшения степени дисперсности ДФ под действием тех или иных факторов.
Стадии коагуляции
Вывод: для золей переход скрытой в явную происходит практически мгновенно!!!
№23 слайд
Содержание слайда: Факторы, вызывающие коагуляцию
Увеличение концентрации золя приводит к уменьшению расстояния между частицами, на котором начинают действовать силы притяжения.
Добавление неэлектролитов из-за способности разрушения гидратной (сольватной) оболочки. Отсутствие оболочки позволяет частицам приблизиться на расстояние, на котором действуют силы притяжения.
№24 слайд
Содержание слайда: Факторы, вызывающие коагуляцию
Добавление электролитов наиболее сильное по 2-м причинам:
из-за адсорбции ионов электролита на грануле и агрегате, снижении заряда гранулы и ζ-потенциала;
из-за уменьшения толщины диффузионного слоя, что приводит к уменьшению расстояния между частицами и возникновению сил притяжения.
№25 слайд
№26 слайд
№27 слайд
Содержание слайда: Правило Дерягина ‒ Ландау …
№28 слайд
Содержание слайда: Факторы, вызывающие коагуляцию
Способность ионов одного заряда к гидратации (лиотропные ряды)
№29 слайд
Содержание слайда: Факторы, вызывающие коагуляцию
«Ионы-партнёры», идущие в паре с коагулирующими ионами, уменьшают их γ в случае адсорбции на поверхности коллоидной частицы.
№30 слайд
Содержание слайда: Особые случаи коагуляции
Смесями электролитов;
Многозарядными ионами‒коагуляторами (чередование зон коагуляции);
При смешивании коллоидов с гранулами разного по знаку заряда (взаимная коагуляция / гетерокоагуляция);
Добавлением очень малых количеств ВМС (сенсибилизация).
№31 слайд
№32 слайд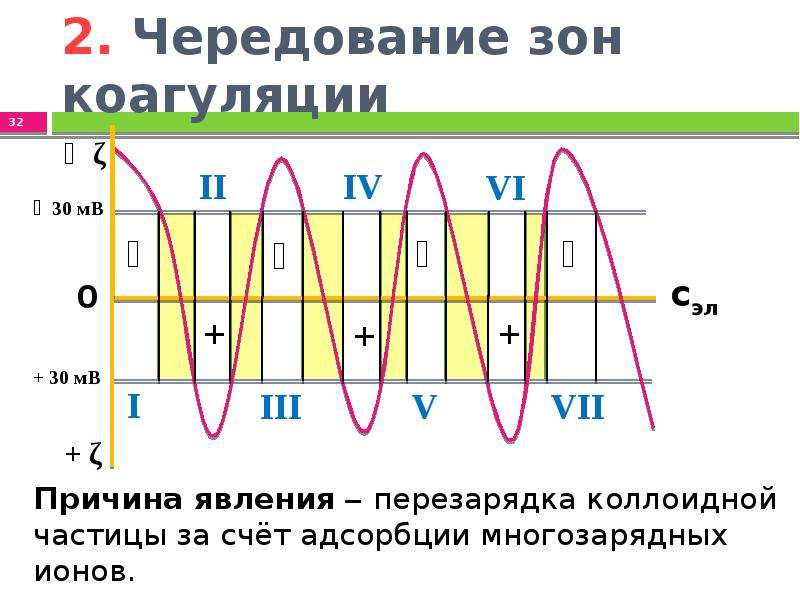
Содержание слайда: 2. Чередование зон коагуляции
№33 слайд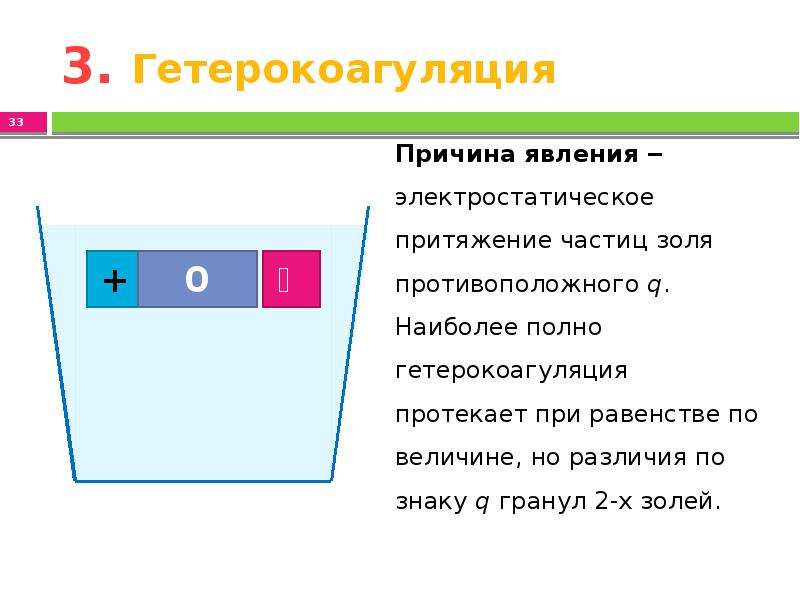
Содержание слайда: 3. Гетерокоагуляция
№34 слайд
Содержание слайда: 4. Сенсибилизация …
… вызвана добавлением очень малых количеств ВМС и понижает устойчивость коллоидов.
… связана с особенностями ВМС:
1. образование макроионов с большой адсорбционной способностью;
2. одновременная адсорбция макроионов на нескольких коллоидных частицах с образованием флокул (мостиковый механизм).
№35 слайд
Содержание слайда: Вывод: адсорбционный слой является механическим препятствием для иона ‒ коагулянта.
…повышение устойчивости коллоидов добавлением ВМС в концентрациях, достаточных для полного адсорбционного насыщения поверхности мицелл защищаемого золя.
№36 слайд
Содержание слайда: Защитное число …
… min масса ВМС (мг), достаточная для предотвращения 10 см3 гидрозоля от коагулирующего действия 1 см3 раствора NaCl с ω=10% (массовая концентрация 100 г/л).
№37 слайд
№38 слайд
Содержание слайда: Теории коагуляции
№39 слайд
















































