Презентация I закон термодинамики, его применение для расчёта тепловых эффектов онлайн
На нашем сайте вы можете скачать и просмотреть онлайн доклад-презентацию на тему I закон термодинамики, его применение для расчёта тепловых эффектов абсолютно бесплатно. Урок-презентация на эту тему содержит всего 70 слайдов. Все материалы созданы в программе PowerPoint и имеют формат ppt или же pptx. Материалы и темы для презентаций взяты из открытых источников и загружены их авторами, за качество и достоверность информации в них администрация сайта не отвечает, все права принадлежат их создателям. Если вы нашли то, что искали, отблагодарите авторов - поделитесь ссылкой в социальных сетях, а наш сайт добавьте в закладки.
Презентации » Химия » I закон термодинамики, его применение для расчёта тепловых эффектов
Оцените!
Оцените презентацию от 1 до 5 баллов!
- Тип файла:ppt / pptx (powerpoint)
- Всего слайдов:70 слайдов
- Для класса:1,2,3,4,5,6,7,8,9,10,11
- Размер файла:1.97 MB
- Просмотров:301
- Скачиваний:5
- Автор:неизвестен
Слайды и текст к этой презентации:
№3 слайд


Содержание слайда: Библиографический список
Стромберг А. Г. Физическая химия / А. Г. Стромберг, Д. П. Семченко – М.: Высш. шк., 2001. – 527 с.
Эткинс П. Физическая химия. В 3-х ч. Ч. 1.: Равновесная термодинамика / П. Эткинс, Дж. де Паула. – М.: Мир, 2007. – 494 с.
Евстратова К. И. Физическая и коллоидная химия / К. И. Евстратова, Н. Н. Купина, Е. Е. Малахова. – М.: Высш. шк., 1990. – 487 с.
Краткий справочник физико-химических величин / Под ред. А. А. Равделя, А. М. Пономаревой. – СПб., 2003. – 238 с.
Химия – Википедия. [Электронный ресурс] – Режим доступа: https://ru.wikipedia.org/wiki/Химия.
Презентации по химии. [Электронный ресурс] – Режим доступа: https:// 900igr.net/prezentacii-po-khimii.html
№5 слайд


Содержание слайда: Предмет термодинамики
Термодинамика изучает положения и законы, описывающие обмен энергией между изучаемой системой и внешней средой, превращения одних форм энергии в другие.
Химическая термодинамика применяет законы и положения общей термодинамики к изучению химических и физико-химических процессов, например, определению теплового эффекта, направления протекания процесса и др.
Термодинамика (Т/Д) базируется на трёх началах или законах термодинамики (постулатах), установленных на основе анализа множества экспериментальных данных.
№6 слайд


Содержание слайда: Основные понятия термодинамики
Система (С.) − тело или группа тел, находящихся во взаимосвязи и мысленно обособленных от окружающей среды.
Окружающая среда (обычно большого размера) − всё, что находится в прямом или косвенном контакте с системой.
С. изолированная − не обменивается веществом и энергией с окружающей средой.
С. открытая − обменивается веществом и энергией с окружающей средой.
С. закрытая − не обменивается веществом, но обменивается энергией с окружающей средой.
С. гомогенная − состоит из одной фазы.
С. гетерогенная − состоит из двух и более фаз.
№7 слайд


Содержание слайда: Основные понятия термодинамики
Фаза − часть системы, одинаковая по составу, физическим и химическим свойствам и отделённая от других частей системы видимой поверхностью раздела.
Компоненты − вещества, из которых состоит система.
Состояние системы − совокупность физических и химических свойств, характеризующих систему.
Термодинамические (Т/Д ) параметры:
T – температура;
P – давление;
V – объём;
C – состав (концентрация).
№8 слайд


Содержание слайда: Основные понятия термодинамики
Т/Д параметры − характеризуют состояние системы.
Различают экстенсивные параметры (аддитивны):
m – масса; V – объём; U – внутренняя энергия и др.,
и интенсивные параметры (не обладают свойством аддитивности, при контакте систем выравниваются):
T – температура; P – давление; C – концентрация и др.
Термодинамический (Т/Д) процесс − всякое изменение в системе, связанное с изменением хотя бы одного параметра.
Различают круговой, изобарный (Р = const), изохорный (V = const), изотермический (T = const), адиабатический (Q(теплота) = const) и др. процессы.
№9 слайд


Содержание слайда: Основные понятия термодинамики
Функции состояния (U, H, S, G, A) − Т/Д функции, значения которых зависят только от начального и конечного состояний системы и не зависят от пути процесса.
Стандартное состояние − при Р = 101325 Па и любой Т.
Стандартные условия − при Р = 101325 Па и Т = 298 К.
Обратимый Т/Д процесс − равновесный, протекает бесконечно медленно, без изменений в окружающей среде.
Необратимый Т/Д процесс − неравновесный, в результате его протекания происходят энергетические изменения в окружающей среде.
№10 слайд


Содержание слайда: I закон (начало) термодинамики
(закон сохранения энергии)
- В любой изолированной системе общий запас энергии постоянен.
- Разные формы энергии переходят друг в друга в строго эквивалентных количествах.
- Вечный двигатель первого рода невозможен, т. е. невозможно построить машину, которая давала бы механическую работу без подвода энергии извне.
Теплота Q, полученная системой извне, расходуется на изменение внутренней энергии U и работу W.
Математическая формулировка I
закона термодинамики
Для физико-химических процессов:
dW = PdV или W = РV – работа расширения
№11 слайд


Содержание слайда: I закон термодинамики
Внутренняя энергия U – общий запас энергии системы, которая складывается из кинетической и потенциальной энергии всех частиц системы и энергии их взаимодействий – функция состояния (U определить невозможно, определяют U).
U = U2 – U1
Теплота Q и работа W не являются функциями состояния.
№12 слайд


Содержание слайда: Применение I закона термодинамики
Термохимия – раздел, посвящённый изучению тепловых эффектов химических и физико-химических процессов.
Тепловой эффект – теплота, выделяемая или поглощаемая в результате протекания процесса.
Q = U + РV (I закон Т/Д для физико-химических процессов)
Изохорные процессы (V = const): V= 0; Q = U;
U (изменение внутренней энергии) – изохорный тепловой эффект.
Изобарные процессы (Р = const): H = U + PV; Q = H;
H (изменение энтальпии) – изобарный тепловой эффект.
Энтальпия Н – функция состояния, как и внутренняя энергия характеризует общий запас энергии системы (включает энергию, которая тратится на работу расширения).
№14 слайд


Содержание слайда: Применение I закона термодинамики
Связь между изобарным и изохорным тепловыми эффектами:
H = U + РV или H = U + nRT
(следует из уравнения Менделеева-Клапейрона РV = nRT)
n – изменение числа моль газообразных веществ в результате протекания реакции (процесса); R = 8,314 Дж/(моль· К).
Пример 1: Определить n в реакциях:
а) 2NO2(г) + O3(г) = O2(г) + N2O5(г);
б) CH4(г) + 2H2S(г) = CS2(ж) + 4H2(г);
в) 2CrCl3(к) + 3H2(г) =2Cr(к) + 6HCl(г).
Решение. а) n = (1 + 1) – (2 + 1) = – 1; б) n = 4 – (1 + 2) = 1;
в) n = 6 – 3 = 3.
При расчёте n число моль жидких и твёрдых веществ
не учитывают!
№16 слайд


Содержание слайда: Применение I закона термодинамики
Расчёты любого процесса основаны на свойстве энтальпии являться функцией состояния!
1) Расчёт тепловых эффектов химических реакций r0
или процессов, например, фазовых переходов trs0: плавления, испарения и др.
Для расчёта необходимы стандартные энтальпии (теплоты) образования веществ f0(298) – справочные величины.
f0(298), кДж/моль – это тепловой эффект образования 1 моль вещества из простых веществ, устойчивых при стандартных условиях (Т = 298 К; Р = 101325 Па).
f0 для устойчивых простых веществ принимают равной нулю.
Например, для углерода устойчивой формой считают графит.
f0(С(графит)) = 0, но f0(С(алмаз)) = 1,83 кДж/моль.
r0 – стандартная энтальпия химической реакции (тепловой эффект химической реакции при стандартном давлении и данной температуре).
№17 слайд


Содержание слайда: Применение I закона термодинамики
trs0 – стандартная энтальпия фазового перехода (тепловой эффект фазового перехода при стандартном давлении и данной температуре).
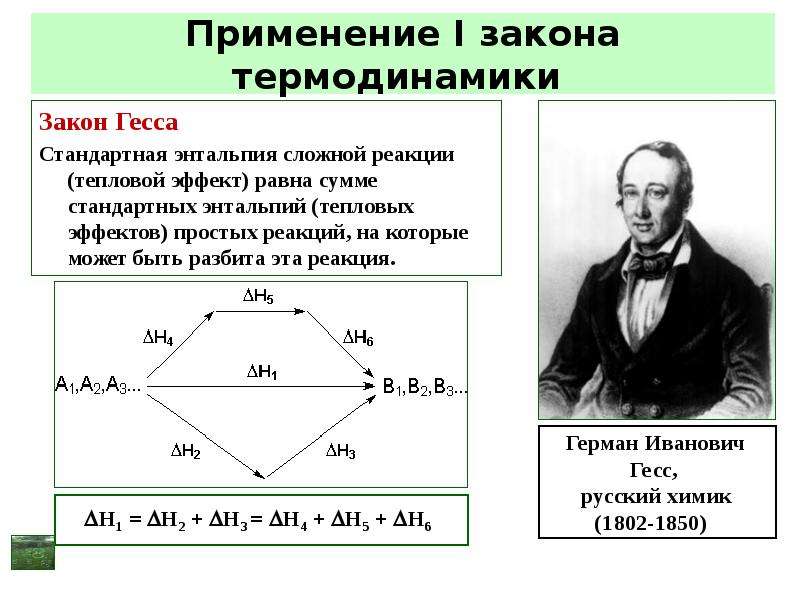
Следствия из закона Гесса:
1) Тепловой эффект реакции (процесса) равен разности суммы энтальпий (теплот) образования продуктов реакции (процесса) и суммы энтальпий (теплот) образования исходных веществ с учётом стехиометрических коэффициентов в уравнении реакции (процесса).
r0 = i f0(прод) – i f0(исх) или
trs0 = i f0(кон) – i f0(исх),
прод (кон) – продукты реакции (конечные вещества);
исх – исходные вещества;
i – стехиометрические коэффициенты в уравнении реакции (процесса).
r0 рассчитывают, по уравнению, записанному в особой термодинамической (термохимической) форме.
№18 слайд


Содержание слайда: Применение I закона термодинамики
Особенности термодинамического уравнения:
Указываются агрегатные состояния веществ.
Допускаются дробные коэффициенты.
С термодинамическими уравнениями можно выполнять такие же действия, как с любыми математическими уравнениями.
Для реакций, протекающих в водных растворах электролитов с участием ионов, тепловые эффекты рассчитывают таким же способом, используя стандартные энтальпии образования ионов в водных растворах (справочные величины).
2) Тепловой эффект прямой реакции (процесса) равен тепловому эффекту обратной реакции (процесса) с противоположным знаком
r(прямой) = –r(обратной),
trs(испарения) = – trs(конденсации),
trs(плавления) = – trs(кристаллизации).
№19 слайд


Содержание слайда: Применение I закона термодинамики
Пример 2.
Определить при Т = 298 К тепловой эффект реакции разложения
воды по уравнению
2H2О(г) = 2Н2(г) + О2(г),
если известно, что для реакции
Н2(г) + 0,5О2(г) = H2О(г), r = –241,81 кДж.
Решение.
Если удвоить коэффициенты второго уравнения, то полученное уравнение реакции
2Н2(г) + О2(г) = 2H2О(г)
отражает реакцию получения 2-х моль воды. Она является обратной для реакции разложения 2-х моль воды. Откуда,
r(прямой) = – 2r(обратной) = – 2· (–241,81) = 483,62 кДж.
Так как r > 0, реакция разложения воды является эндотермической, т. е. протекает с поглощением теплоты.
№20 слайд


Содержание слайда: Применение I закона термодинамики
Для реакций с участием органических веществ тепловой эффект можно рассчитывать по стандартным энтальпиям (теплотам) сгорания с0 (справочные величины) – это тепловые эффекты полного окисления 1 моль органических соединений с образованием определённых продуктов: СО2(г), Н2О(ж), N2(г), HCl(г), HBr(г), НI(г).
Например, с0(C6H5О2N(ж)) представляет собой тепловой эффект реакции
C6H5О2N(ж) + 6,25О2(г) = 6СО2(г) + 2,5Н2О(ж) + 0,5N2(г).
Из справочной таблицы с0(C6H5О2N(ж)) = –3091,2 кДж/моль.
Расчёт тепловых реакций по теплотам сгорания проводят по формуле
r0 = i с0(исх) – i с0(прод),
исх – исходные вещества; прод – продукты реакции;
i – стехиометрические коэффициенты в уравнении реакции.
№21 слайд


Содержание слайда: Применение I закона термодинамики
2) Тепловые эффекты процессов растворения
Интегральная энтальпия (теплота) растворения s0 зависит от моляльной концентрации вещества в растворе.
s0 (m), кДж/моль – теплота, которая выделяется или поглощается при растворении 1 моль вещества в таком количестве растворителя, чтобы образовался раствор определённой моляльной концентрации (справочная величина).
3) Расчёт тепловых эффектов процессов разбавления или концентрирования
Для расчёта необходимы величины интегральных энтальпий (теплот) растворения исходных и конечных растворов.
Тепловым эффектом разбавления (концентрирования) называют теплоту , которая выделяется или поглощается при разбавлении (концентрировании) раствора, содержащего 1 моль растворённого вещества, от концентрации Сm(1) до концентрации Сm(2).
Раствор 1(Сm(1)) → Раствор 2(Сm(2))
= s0(2) – s0(1) или = m(2) – m(1).
№22 слайд


Содержание слайда: Влияние температуры на тепловой эффект (уравнение Кирхгофа)
Характер влияния температуры на тепловой эффект в соответствии с уравнением Кирхгофа определяется знаком
изменения молярной теплоёмкости
СР (изобарной) или СV (изохорной)
в результате протекания соответствующего процесса.
Уравнение Кирхгофа
в дифференциальной
форме
№23 слайд


Содержание слайда: Анализ уравнения Кирхгофа
если СР > 0, то d/dТ > 0, т. е. с увеличением температуры тепловой эффект увеличивается;
если СР < 0, то d/dТ < 0, т. е. с увеличением температуры тепловой эффект уменьшается;
если СР = 0, то d/dТ = 0, = const, тепловой эффект не зависит от температуры.
№24 слайд


Содержание слайда: Расчёт теплового эффекта при любой температуре
Уравнение Кирхгофа
в интегральной форме
r298 = i f0(прод) – i f0(исх),
СР = i СР(прод) – i СР(исх),
i – стехиометрические коэффициенты в уравнении реакции;
СР = a + bT + c'/T2 – изобарная молярная теплоёмкость для неорганических веществ, уравнение зависимости СР от температуры;
СР = a + bT + cT2 – изобарная молярная теплоёмкость для органических веществ, уравнение зависимости СР от температуры;
а, b, c', c – эмпирические коэффициенты веществ (справочные величины в указанном интервале температур).
№25 слайд


Содержание слайда: Расчёт теплового эффекта при любой температуре
Расчёт rТ с различными приближениями
Первое приближение: СР = С0Р,298;
С0Р,298 – стандартная изобарная молярная теплоёмкость (справочная величина).
С0Р,298 = i С0Р,298(прод) – i С0Р,298(исх).
Второе приближение: СР = a + bT;
Третье приближение: СР = a + bT + c'/T2 + cT2 – наиболее точный расчёт.
а = iаi(прод) – iаi(исх).
Расчёт b, c', c – аналогичен.
i – стехиометрические коэффициенты в уравнении реакции.
№26 слайд


Содержание слайда: Влияние температуры на тепловой эффект
Пример 3.
Определить тепловой эффект реакции
С2Н5ОН(г) + 3О2(г) = 2СО2(г) + 3Н2О(г)
при температурах 298 и 800 К.
Решение.
Для расчета r при 298 К находим справочные значения стандартных энтальпий образования (кДж/моль) веществ-участников реакции:
f0(С2Н5ОН(г)) = – 234,80; f0(СО2(г)) = – 393,51;
f0(Н2О(г)) = –241,81; для простого вещества О2 f0(О2(г)) = 0.
r298 = i f0(прод) - i f0(исх) =
(2fH0(СО2) + 3fH0(Н2О)) – (fH0(С2Н5ОН) + 3fH0(О2)) =
(2·(–393,51) + 3·(–241,81)) – ((–234,80) + 3·0) = –1277,62 кДж.
Т. к. r298 < 0, реакция экзотермическая, протекает с выделением теплоты.
Для расчета r при 800 К используем уравнение Кирхгофа и первое приближение при определении СР:
СР = С0Р,298 = iС0Р,298(прод) – iС0Р,298(исх) = const.
№27 слайд


Содержание слайда: Влияние температуры на тепловой эффект (уравнение Кирхгофа)
rТ = r298 + = r298 + СР,298· (Т – 298).
Для расчета СР,298 выпишем справочные значения стандартных изобарных молярных теплоёмкостей (Дж/(моль·К)) веществ-участников реакции:
СР,298 (С2Н5ОН(г)) = 65,75; СР,298 (СО2(г)) = 37,11; СР,298 (О2(г)) = 29,37; СР,298(Н2О(г)) = 33,61.
СР,298 = (2СР,298(СО2) + 3СР,298(Н2О)) – (СР,298(С2Н5ОН) + 3СР,298(О2)) =
= (2·37,11 + 3·33,61) – (65,75 + 3·29,37) = 21,19Дж/К = 0,02119 кДж/К.
Рассчитаем rТ при Т = 800 К.
r800 = –1277,62 + 0,02119 · (800 – 298) = –1266,98 кДж.
При 800 К реакция по-прежнему – экзотермическая, но теплоты выделится несколько меньше, чем при 298 К.
№28 слайд


Содержание слайда: Качественная оценка тепловых эффектов различных процессов
С выделением теплоты (rH < 0, trs < 0, s < 0) протекают:
– реакции горения (взаимодействие веществ с кислородом), например,
C2H4(г) + 3O2(г) = 2CO2(г) + 2H2O(г);
– реакции соединения (образование сложных веществ из более простых), например,
2C(графит) + 3H2(г) = C2H6(г);
– процессы растворения кислот и щелочей в воде, например,
Н2SO4 + nН2O = 2Н+ ·aq + SO42− ·aq (aq - молекулы Н2O);
– процессы конденсации и кристаллизации, например,
H2O(г) = H2O(ж).
С поглощением теплоты (rH > 0, trs > 0) протекают:
– реакции разложения (образование простых или менее сложных веществ из более сложных), например,
CaCO3(к) = CaO(к) + СО2(г);
– процессы испарения и плавления, например,
H2O(к) = H2O(ж).
№30 слайд


Содержание слайда: II закон (начало) термодинамики
I закон термодинамики позволяет определять теплоту и работу, но не даёт ответа на вопрос: в каком направлении и до какого предела будет протекать самопроизвольный процесс. Ответ на этот вопрос даёт II закон термодинамики.
Формулировка Клаузиуса (1850 г.)
- Теплота не может самопроизвольно переходить от более холодного тела к горячему.
Формулировка Томпсона
Никакая совокупность процессов не может сводиться только к превращению теплоты в работу, тогда как превращение работы в теплоту может быть единственным результатом процесса.
№31 слайд


Содержание слайда: II закон (начало) термодинамики
Формулировка Оствальда
Невозможно создание вечного двигателя второго рода, т. е. невозможно построить машину, которая превращала бы всю теплоту в работу без передачи части её холодильнику.
Формулировка Кельвина
- Не существует циклического процесса, единственным результатом которого было бы получение теплоты от нагревателя и полное превращение её в работу.
№32 слайд


Содержание слайда: II закон (начало) термодинамики
II закон термодинамики также был установлен как постулат, но в отличие от I закона имеет более ограниченную область применения, носит статистический характер, поэтому применим только к системам, состоящим из большого числа частиц.
Самопроизвольными называют процессы, протекающие без вмешательства извне (без затраты энергии)
№33 слайд


Содержание слайда: II закон (начало) термодинамики
Накопленный человечеством опыт показывает, что самопроизвольное протекание процессов в системе возможно только в направлении выравнивания фактора интенсивности (температуры, давления, концентрации и т. д.). Пределом самопроизвольного протекания процесса является достижение одинакового значения фактора интенсивности во всех частях системы.
Но это утверждение не применимо к однородным системам, в частности, к химическим реакциям.
Это требует введения новой функции состояния – энтропии.
Её ввёл Р. Клаузиус (1865 г.), обозначил S.
№34 слайд


Содержание слайда: II закон (начало) термодинамики
II закон (начало) термодинамики особенно наглядно проявляется в работе тепловых машин, для которых и был сформулирован.
В настоящее время этот закон вводят в рассмотрение путём анализа работы тепловых машин (цикл Карно).
Второй закон термодинамики можно сформулировать
без анализа работы тепловых машин
(принцип Каратеодори).
II закон термодинамики – всеобщий закон природы, по своей фундаментальности уступающий место только I закону термодинамики – закону сохранения энергии!
№35 слайд


Содержание слайда: II закон (начало) термодинамики
Пусть система переходит из состояния 1 в
состояние 2 с поглощением теплоты.
Предположим, что система может вернуться из
состояния 2 в состояние 1 без теплообмена
(адиабатически). В соответствии с I законом
термодинамики:
Q = U + W(1) (для прямого процесса);
0 = – U + W(2) (для обратного процесса).
В результате кругового процесса: Q = W(1) + W(2), т. е. вся теплота должна превратиться в работу, а это невозможно согласно I закону термодинамики.
Принцип Каратеодори: в непосредственной близости от любого состояния имеются такие состояния, которые недостижимы адиабатическим путём, т. е. без передачи теплоты.
№36 слайд


Содержание слайда: II закон (начало) термодинамики
Из принципа Каратеодори следует утверждение о существовании новой функции, которая связана с теплотой процесса!
II закон термодинамики – это закон о существовании и сохранении энтропии S.
Математическое выражение
II закона термодинамики
Знак = – для обратимых Т/Д процессов;
знак > – для необратимых Т/Д процессов.
Математическое выражение
объединённого уравнения I и II
законов термодинамики
№37 слайд


Содержание слайда: Энтропия как критерий самопроизвольного протекания процесса
Для изолированных систем (U = const; V = const)
теплообмен и массообмен отсутствует: Q = 0.
Для обратимых процессов: dS = 0; S = 0.
Для необратимых процессов: dS > 0; S > 0.
В изолированной системе всякий самопроизвольный процесс протекает в направлении возрастания энтропии:
dS > 0; S > 0; S → Smax;
при dS = 0; S = 0; S = Smax в системе – равновесие.
№38 слайд


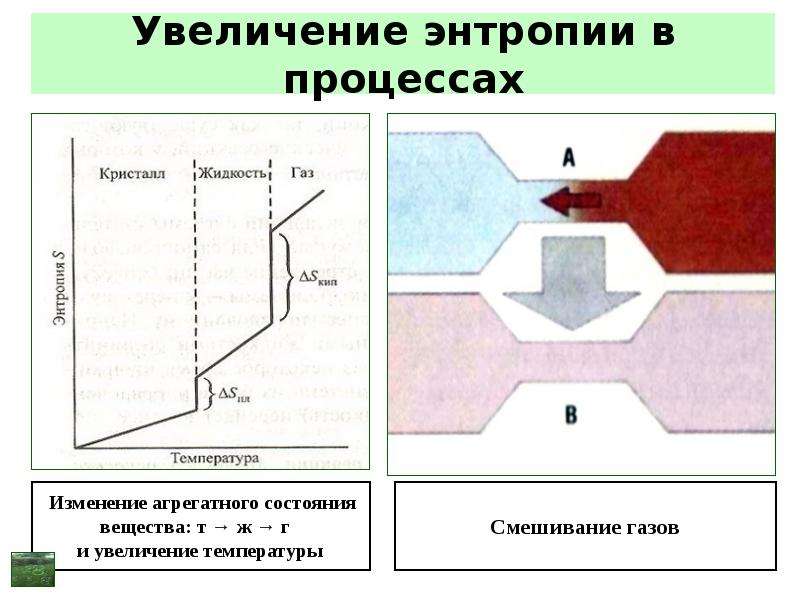
Содержание слайда: Изменение энтропии в процессах
Энтропия S – мера беспорядка (хаоса) или степень неупорядоченности системы – функция состояния.
ТS – мера связанной энергии (не может превратиться в полезную работу).
Всякий процесс, приводящий к увеличению беспорядка приводит к увеличению энтропии:
- изменение агрегатного состояния т → ж → г;
- повышение температуры;
- усложнение состава вещества;
- растворение твёрдых и жидких веществ;
- в химических реакциях – увеличение числа газообразных молекул и т. п.
№40 слайд


Содержание слайда: Статистическое обоснование II закона термодинамики
Всякая изолированная система стремится перейти из состояния менее вероятного в состояние более вероятное: W → Wmax.
W – термодинамическая вероятность (число микросостояний, характеризующих данное макросостояние).
Л. Больцман показал, что при
W → Wmax; S → Smax.
Уравнение Больцмана
k – постоянная Больцмана (1,38· 10−23 Дж/К)
№41 слайд


Содержание слайда: Расчёт изменения энтропии
в различных процессах
1. При фазовом превращении 1 моль вещества (Т = const; Р = const):
Н(ф.п.) – теплота (энтальпия) фазового превращения;
Т(ф.п.) – температура фазового превращения.
2. При изменении температуры 1 моль вещества (Р = const):
3. При взаимной диффузии двух идеальных газов:
S = – R(x1lnx1 + x2lnx2)
x1, x2 – молярная доля 1-го и 2-го газа.
№42 слайд


Содержание слайда: Расчёт изменения энтропии в различных процессах
4. В химических реакциях:
При Т = 298 К rS 0298 = i S0(прод) – i S0(исх),
S2980, Дж/(моль·К) – абсолютная стандартная энтропия 1 моль вещества (справочная величина).
При любой Т
СР = i СР(прод) – i СР(исх).
Первое приближение: СР = С0Р,298;
Второе приближение: СР = a + bT;
Третье приближение: СР = a + bT + c'/T2 + cT2 – точный расчёт.
С0Р,298 (а, b, с', c) – стандартная изобарная молярная теплоёмкость 1 моль вещества (эмпирические коэффициенты в уравнении для расчёта изобарной молярной теплоёмкости вещества) – справочные величины.
№43 слайд


Содержание слайда: Расчёт изменения энтропии вещества
при изменении температуры
Пример 4.
Определить изменение энтропии при охлаждении 320 г моноклинной серы от 360 0С до 25 0С.
Решение. Выпишем из справочных таблиц температуру плавления моноклинной серы: Тпл = 119,3 0С.
При 25 0С сера находится в твёрдом (кристаллическом) состоянии, следовательно, в интервал температур 360-25 0С попадает фазовый переход: кристаллизация серы. При 360 0С сера находится в жидком состоянии.
Запишем схему процессов, происходящих с серой S в интервале температур Т1 − Т2:
№44 слайд


Содержание слайда: Расчёт изменения энтропии вещества при изменении температуры
Таким образом, общее изменение энтропии S при охлаждении серы в интервале температур Т1 − Т2 складывается из изменения энтропии S1 − при охлаждение жидкой серы; S2 − при кристаллизации серы; S3 − при охлаждение твёрдой серы.
Для расчёта S выпишем из справочных таблиц теплоту плавления Нпл, изобарные молярные теплоёмкости в твёрдом СР(т) и жидком СР(ж) состояниях для моноклинной серы: Нпл = 1,446 кДж/моль; СР(т) = 23,64 Дж/(моль∙К), СР(ж) = 35,73 Дж/(моль∙К).
Переведём массу серы в количество:
n = 10 моль.
Определим теплоту кристаллизации Нкр:
Нкр = −Нпл = −1446 Дж/моль,
т. к. кристаллизация − процесс, обратный плавлению.
Переведём величины температур из 0С в К:
Т1 = 573 К; Т2 = 298 К; Тпл = Ткр= 392,3 К.
№45 слайд


Содержание слайда: Расчёт изменения энтропии вещества при изменении температуры
Рассчитаем изменение энтропии в процессе охлаждения жидкой серы:
S1 = = СР(ж) ln = 35,73 ln = −13,54 Дж/(моль∙К).
Рассчитаем изменение энтропии в процессе кристаллизации:
S1 = = = −3,69 Дж/(моль∙К).
Рассчитаем изменение энтропии в процессе охлаждения твёрдой серы:
S1 = = СР(т) ln = 23,64 ln = −6,56 Дж/(моль∙К).
Все расчёты сделаны на 1 моль серы.
Рассчитаем изменение энтропии при охлаждении 320 г (10 моль) серы в интервале температур Т1 − Т2:
S = n(S1 + S2 + S3) = 10(− 13,54 − 3,69 − 6,56) = −237,9 Дж/К.
При охлаждении любого вещества энтропия системы уменьшается, при нагревании − увеличивается!
№46 слайд


Содержание слайда: Расчёт изменения энтропии в
химической реакции
Пример 5. Определить изменение энтропии при температурах 298 К и 800 К в химической реакции
С2Н5ОН(г) + 3О2(г) = 2СО2(г) + 3Н2О(г).
Решение. Выпишем из справочной таблицы S0298 и С0Р,298 всех веществ-участников химической реакции
Рассчитаем изменение энтропии при 298 К
rS298 = i S0(прод) – i S0(исх) = (2S0(СО2) + 3S0(Н2О)) – (1S0(С2Н5ОН) + 3S0(О2)) = (2·213,66 + 3·188,72) – (1·281,38 + 3·205,01) = 96,95 Дж/К.
№47 слайд


Содержание слайда: Расчёт изменения энтропии в
химической реакции
rS298 > 0, беспорядок в системе увеличился, т. к. из 4 молекул газа образовалось 5 молекул газа.
Рассчитаем изменение энтропии при 800 К,
примем СР = С0Р,298.
С0Р,298 = i С0Р,298(прод) – i С0Р,298(исх) = (2С0Р,298(СО2) + 3С0Р,298(Н2О)) – (1С0Р,298(С2Н5ОН) + 3С0Р,298(О2)) = (2·37,11 + 3·33,61) – (1·65,75 + 3·29,37) = 21,19 Дж/К.
= 96,95 + 21,19∙ln = 117,88 Дж/К.
С увеличением температуры в системе энтропия в результате протекания данной реакции увеличилась.
№49 слайд


Содержание слайда: Энергия Гиббса,
энергия Гельмгольца,
их практическое значение
Энергия Гиббса и энергия Гельмгольца, их физический смысл.
Энергия Гиббса и энергия Гельмгольца как критерий самопроизвольного протекания процесса.
Расчёт энергии Гиббса в химических реакциях.
Химический потенциал.
Нулевой закон термодинамики.
№51 слайд


Содержание слайда: Энергия Гельмгольца
Энергия Гельмгольца (изохорно-изотермический потенциал) – A
Из объединённого уравнения I и II законов термодинамики следует, при T = const; V = const:
WM – максимальная полезная работа в изохорно-изотермическом процессе.
Связь энергии Гиббса и энергии Гельмгольца
G = A + РV или G = A + nRT
n – изменение числа моль газообразных веществ в результате протекания реакции (процесса).
№52 слайд
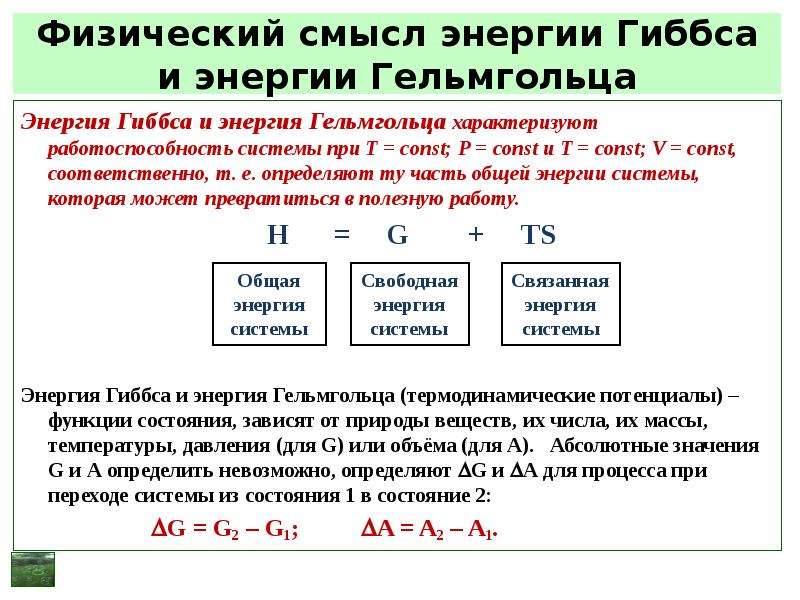

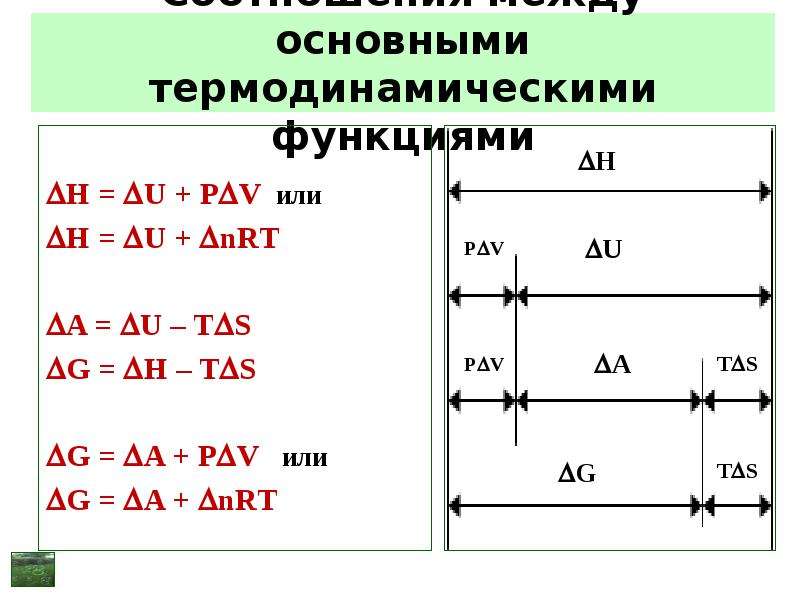
Содержание слайда: Физический смысл энергии Гиббса и энергии Гельмгольца
Энергия Гиббса и энергия Гельмгольца характеризуют работоспособность системы при T = const; Р = const и T = const; V = const, соответственно, т. е. определяют ту часть общей энергии системы, которая может превратиться в полезную работу.
H = G + TS
Энергия Гиббса и энергия Гельмгольца (термодинамические потенциалы) – функции состояния, зависят от природы веществ, их числа, их массы, температуры, давления (для G) или объёма (для А). Абсолютные значения G и А определить невозможно, определяют G и А для процесса при переходе системы из состояния 1 в состояние 2:
G = G2 – G1; A = A2 – A1.
№53 слайд


Содержание слайда: Полные дифференциалы термодинамических потенциалов A и G
После дифференцирования выражений А = U – TS и G = H – TS и использования объединённого уравнения I и II законов термодинамики получают выражения для полных дифференциалов термодинамических потенциалов A и G.
При T = const; V = const
При T = const; Р = const
Знак = – для обратимых Т/Д процессов;
знак < – для необратимых Т/Д процессов.
№54 слайд


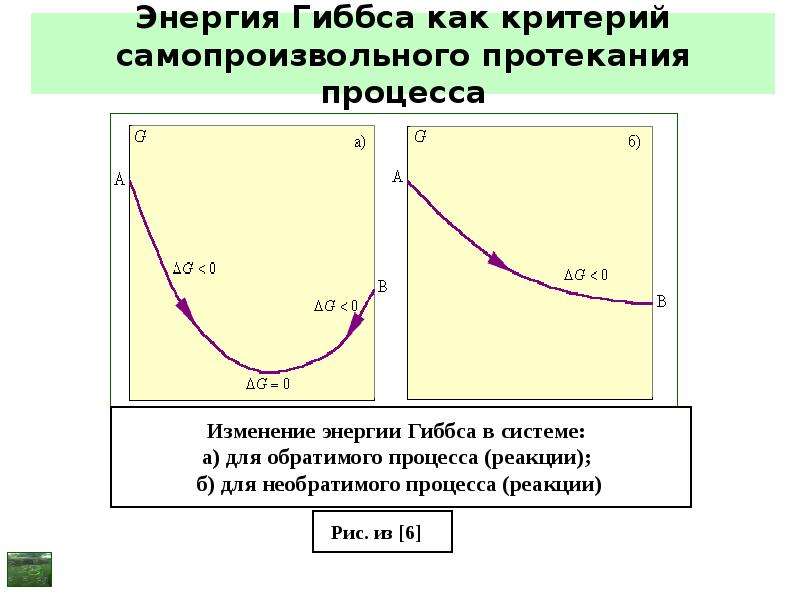
Содержание слайда: Энергии Гельмгольца и Гиббса как критерий самопроизвольного протекания процесса
В закрытой системе всякий самопроизвольный процесс протекает в направлении уменьшения энергии Гельмгольца (изохорно-изотермический процесс) или уменьшения энергии Гиббса (изобарно-изотермический процесс)
T = const; V = const: dА < 0 или A < 0; A → Amin;
T = const; P = const: dG < 0 или G < 0; G → Gmin;
при dА = 0 или А = 0; А = Аmin в системе – равновесие;
при dG = 0 или G = 0; G = Gmin в системе – равновесие.
Самопроизвольными называют процессы, протекающие без вмешательства извне (без затраты энергии).
№57 слайд


Содержание слайда: Характеристические функции. Уравнения Гиббса-Гельмгольца
Характеристическими называют термодинамические функции, посредством которых или их производных могут быть выражены в явном виде термодинамические свойства системы (P, V, T, S).
G и A – характеристические функции, т. к. с учётом зависимости G = f(T, P) и A= f(T, V) выведены соотношения для частных производных G, A и, соответственно, G, А, позволяющие выразить P, V, S (S).
Подставляя в выражения G = H – TS; A = U – TS
частные производные от G и А получают
Уравнение Гиббса
Уравнение Гельмгольца
№58 слайд


Содержание слайда: Стандартная энергия Гиббса
образования вещества
fG0298, кДж/моль – стандартная энергия Гиббса образования 1 моль вещества из простых веществ, устойчивых при стандартных условиях
(Т = 298 К; Р = 101325 Па) – справочная величина.
fG0298 для устойчивых простых веществ принимают равной нулю.
fG0298 – мера прочности (устойчивости) сложных веществ:
чем меньше значение fG0 298 вещества, тем более прочным
(устойчивым) оно является.
На практике величины fG0298 используют для сравнительной характеристики устойчивости однотипных соединений (оксидов, солей и др.)
№59 слайд


Содержание слайда: Стандартная энергия Гиббса
образования вещества
Пример 6.
Определить наиболее устойчивое вещество в ряду карбонатов:
Na2CO3(К), BaCO3(К), MgCO3(К), FeCO3(K).
Решение. Из справочных таблиц выпишем значения fG0298 для карбонатов металлов:
fG0298, кДж/моль
1. Na2CO3(К) −1048,20
2. BaCO3(К) −1132,77
3. MgCO3(К) −1012,15
4. FeCO3(K) −665,09.
И анализа приведённых величин следует, что наиболее устойчивым является карбонат бария BaCO3, т. к. имеет наименьшее значение fG0298.
№60 слайд


Содержание слайда: Расчёт изменения энергии Гиббса в химических реакциях
При Т = 298 К 1) rG0298 = i fG0(прод) – i fG0(исх),
2) rG0298 = rH0298 – 298·rS0298.
При любой Т rG0Т = rH0Т – ТrS0Т;
rG0Т можно рассчитать с различной степенью точности, используя различные приближения для определения СР!
№61 слайд


Содержание слайда: Расчёт изменения энергии Гиббса в химических реакциях
Пример 7.
Определить при температурах 298 и 800 К изменение энергии Гиббса и направление протекания химической реакции
С2Н5ОН(г) + 3О2(г) = 2СО2(г) + 3Н2О(г).
Решение. Для расчета rG298 при 298 К 1 способом необходимы справочные значения стандартных энергий Гиббса образования (кДж/моль) веществ-участников реакции:
fG0(С2Н5ОН(г)) = –167,96; f0G(СО2(г)) = –394,37;
fG0(Н2О(г)) = –228,61; для простого вещества О2 fG0(О2(г)) = 0.
rG298 = i fG0(прод) – i fG0(исх) = (2fG0(СО2) + 3fG0(Н2О)) – (G0(С2Н5ОН) + 3fG0(О2)) = (2·(–394,37) + 3(–228,61)) – (1·(–167,96) + 3·0) = –1306,61 кДж.
№62 слайд


Содержание слайда: Расчёт изменения энергии Гиббса в химических реакциях
Расчет rG при 298 К 2 способом по уравнению
rG0298 = rH0298 – 298·rS0298.
rH0298 = –1277,62 кДж (см. пример 3);
rS0298 = 96,95 Дж/К = 0,09695 кДж/К (см. пример 5).
rG0298 = –1277,62 – 298( –0,09695) = –1306,51 кДж.
Величины rG0(298), рассчитанные двумя способами, практически совпадают.
При 298 К реакция протекает в прямом направлении, т. к. rG0 < 0.
Расчет rG при 800 К по уравнению
rG0Т = rH0Т – Т·rS0Т.
rH0800 = –1266,98 кДж (см. пример 3); rS0800 = 117,88Дж/К = 0,118 кДж/К (см. пример 5).
rG0800 = –1266,98 – 800 · 0,118 = –1361,3 кДж.
При 800 К реакция по-прежнему протекает в прямом направлении, т. к. rG0 < 0.
№63 слайд


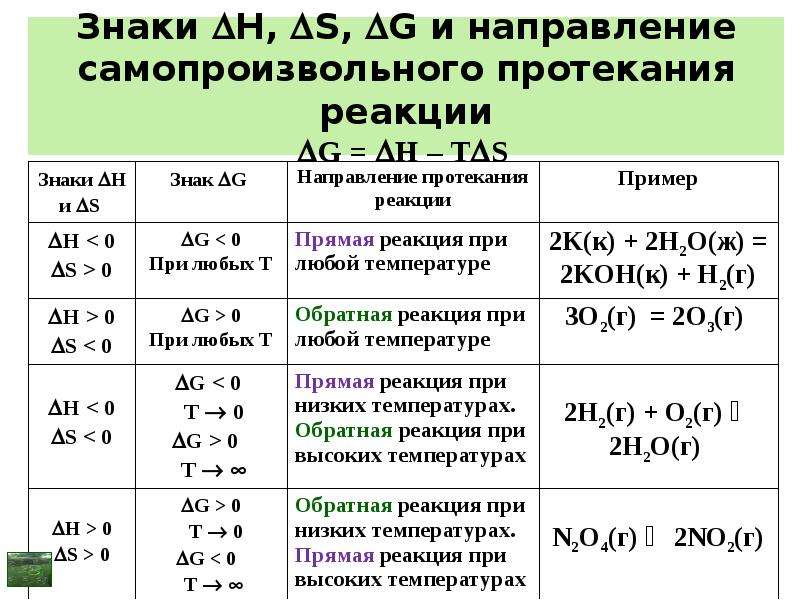
Содержание слайда: Качественная оценка направления протекания процесса
Оценку производят по знакам rH и rS и по знаку rG из анализа уравнения
rG0Т = rH0Т – Т·rS0Т.
Т. к. для процесса (пример 7) rH < 0; rS > 0, следовательно,
при Т→ 0 (низкие температуры) rGТ rH;
rG0 < 0 – прямая реакция (→);
при Т→ ∞ (высокие температуры) rGТ – Т·rS0Т;
rG0 < 0 – прямая реакция(→).
Данная реакция при любых температурах протекает в прямом направлении и поэтому является практически необратимой!
№65 слайд


Содержание слайда: Химический потенциал
При протекании химических реакций в открытых системах состав и масса каждого компонента изменяются, что влияет на энергетическое состояние каждого участника и всей системы в целом. Поэтому термодинамические потенциалы А и G зависят не только от внешних параметров, но и от количества каждого участника реакции ni.
G = f(T, P, n1, n2, … ni).
Для определения энергии Гиббса в открытых системах необходимо введение функции, характеризующей энергетическое состояние каждого компонента.
№67 слайд


Содержание слайда: Химический потенциал
Для многокомпонентной системы при T = const и Р = const
Критерий самопроизвольного
протекания процесса
в открытых системах
Равновесие в системе
Химический потенциал характеризует энергетическое состояние вещества в многокомпонентной открытой системе, в то время как термодинамические потенциалы A и G характеризуют энергетическое состояние индивидуального вещества.
№68 слайд


Содержание слайда: Химический потенциал
µ = f(T, P, C, природы вещества).
При Т = const химический потенциал i-того компонента µi в системе зависит от его давления (фугитивности).
Для идеальных газов µi = µ0i + RTlnPi;
Для реальных газов µi = µ0i + RТlnfi; fi = γ · Pi;
µ0i − стандартный химический потенциал (Р = 1013251 Па);
Pi − парциальное давление идеального газа, Па;
fi − фугитивность (парциальное давление реального газа);
γ − коэффициент фугитивности.
№69 слайд


Содержание слайда: Химический потенциал
При Т = const химический потенциал i-того компонента µi в системе зависит от его концентрации (активности).
Для идеальных растворов µi = µ0i + RTlnСi;
Для реальных растворов µi = µ0i + RTlnаi; аi = γ · Сi
µ0i − стандартный химический потенциал (С = 1 моль/м3 или С = 1 моль/кг растворителя);
Сi − концентрация идеального раствора, моль/м3 или моль/кг растворителя;
аi − активность (концентрация реального раствора);
γ − коэффициент активности.
№70 слайд
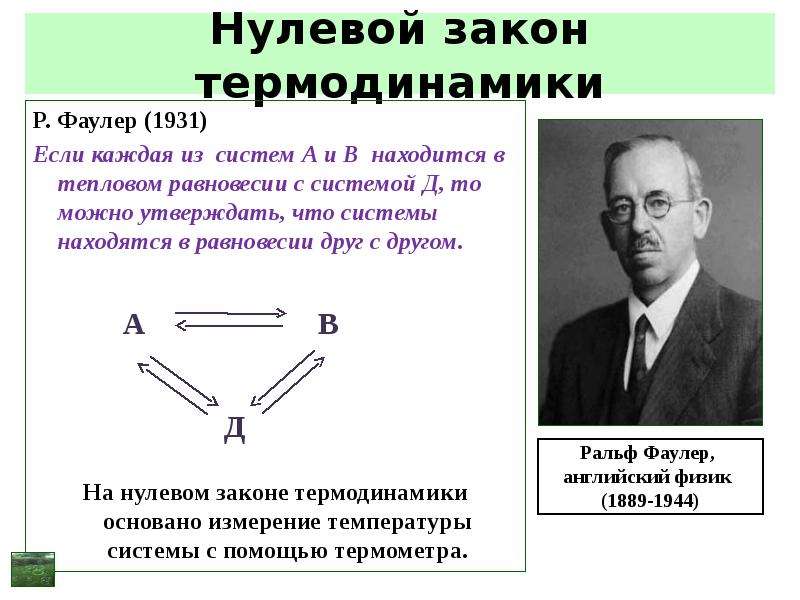

Содержание слайда: Нулевой закон термодинамики
Р. Фаулер (1931)
Если каждая из систем А и В находится в тепловом равновесии с системой Д, то можно утверждать, что системы находятся в равновесии друг с другом.
На нулевом законе термодинамики основано измерение температуры системы с помощью термометра.
Скачать все slide презентации I закон термодинамики, его применение для расчёта тепловых эффектов одним архивом:
Похожие презентации
-
 Углерод и его соединения Лекция. (29 -30, с. 172 -178). Цель: Какие соединения образует углерод? Какие свойства, связанные со строением атома углерода, характерны для углерода и его соединений? Где находят применение соединения углерода?
Углерод и его соединения Лекция. (29 -30, с. 172 -178). Цель: Какие соединения образует углерод? Какие свойства, связанные со строением атома углерода, характерны для углерода и его соединений? Где находят применение соединения углерода? -
 Источники сырья для производства полимера полиуретана, области применения, его свойства, объемы его производства
Источники сырья для производства полимера полиуретана, области применения, его свойства, объемы его производства -
 Закон действующих масс и его использование в расчетах. (Лекциии 4-6)
Закон действующих масс и его использование в расчетах. (Лекциии 4-6) -
 Термохимия. Расчет тепловых эффектов химических реакций
Термохимия. Расчет тепловых эффектов химических реакций -
 Основные понятия химической термодинамики. Первый закон термодинамики Физическая и коллоидная химия и ее значение для фармации
Основные понятия химической термодинамики. Первый закон термодинамики Физическая и коллоидная химия и ее значение для фармации -
 Закон действующих масс и его применение к различным типам равновесий
Закон действующих масс и его применение к различным типам равновесий -
 Теория сильных электролитов. Закон действующих масс и его применение к гетерогенным равновесиям
Теория сильных электролитов. Закон действующих масс и его применение к гетерогенным равновесиям -
 Интеллектуальная игра по теме: «Периодический закон и система химических элементов Д. И. Менделеева». «Химический дом и его обитат
Интеллектуальная игра по теме: «Периодический закон и система химических элементов Д. И. Менделеева». «Химический дом и его обитат -
 Значение периодического закона для современной науки и техники (связь химии с экономикой и экологией) Учитель химии МОУ лицея
Значение периодического закона для современной науки и техники (связь химии с экономикой и экологией) Учитель химии МОУ лицея -
 Применение арт-технологии на уроках химии Обобщение опыта педагогической деятельности МОУ СОШ 14 город Мончегорск Мурманск
Применение арт-технологии на уроках химии Обобщение опыта педагогической деятельности МОУ СОШ 14 город Мончегорск Мурманск