Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
25 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
108.00 kB
Просмотров:
44
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Карбоновые кислоты
Учитель химии МОУ лицея № 6
Дробот Светлана Сергеевна
№2 слайд
Содержание слайда: Содержание
Определение
Классификация кислот
Номенклатура
Изомерия
Получение
Химические свойства (как минеральные
кислоты; специфические свойства )
Применение
Источники информации
№3 слайд
Содержание слайда: Определение
Карбоновыми кислотами называются
производные углеводородов, в молекуле
которых содержится одна или несколько
карбоксильных групп –COOH.
Общая формула карбоновых кислот:
R – C = O
|
OH
№4 слайд
Содержание слайда: Классификация кислот
В зависимости от природы радикала, связанного с карбоксильной группой, кислоты подразделяются на предельные, непредельные и ароматические.
По числу карбоксильных групп делятся на одноосновные и многоосновные кислоты.
Общая формула предельных одноосновных кислот: СnH2n+1COOH (или СnH2nO2).
№5 слайд
Содержание слайда: Дайте классификацию следующим кислотам:
Дайте классификацию следующим кислотам:
COOH
O O O
|| || ||
HO – C – (CH2)2 – C – OH CH2 = CH – C – OH
бензойная янтарная акриловая
O COOH O O
|| || ||
CH3 – C – OH HO – C – CH = CH – C – OH
HOOC
уксусная терефталевая малеиновая
C17H35COOH C17H33COOH
стеариновая олеиновая
№6 слайд
Содержание слайда: HCOOH Муравьиная (метановая) - формиат
HCOOH Муравьиная (метановая) - формиат
CH3COOH Уксусная (этановая) - ацетат
CH3CH2COOH Пропионовая (пропановая) - пропионат
CH3(CH2)2COOH Масляная (бутановая) - бутират
CH3(CH2)3COOH Валериановая (пентановая)-валерат
CH3(CH2)4COOH Капроновая (гексановая) - гексанат
CH3(CH2)6COOH Каприловая (октановая) - октаноат
CH3(CH2)8COOH Каприновая (декановая) - деканоат
CH2=CH–COOH Акриловая (пропеновая) - акрилат
C6H5COOH Бензойная (бензойная) - бензоат
HOOC–COOH Щавелевая (этандиовая) - оксалат
CH3(CH2)14COOH Пальмитиновая (гексадекановая)
- пальмиат
CH3(CH2)16COOH Стеариновая (октадекановая)
- стеарат
№7 слайд
Содержание слайда: Номенклатура
В систематической номенклатуре кислот действуют
следующие правила:
1. Главная цепь должна начинаться и нумероваться с
карбоксильной группы.
2. В префиксе указываются положение и названия
заместителей.
3. После корня указывающего число атомов в цепи
идет суффикс, показывающий наличие или отсутствие
двойных, тройных связей, их положение.
4. После этого добавляется «– овая кислота». Если
карбоксильных групп несколько, то перед – овая
ставится числительное (ди –, три –… ).
№8 слайд
Содержание слайда: 4 3 2 1
4 3 2 1
CH3 – CH2 – CH – COOH 2 – метилбутановая кислота
|
OH
5 4 3 2 1
H2C = C – C = CH – COOH 3,4-диметилпентадиен-2,4-
| | овая кислота
CH3 CH3
CH3 CH3
| |
HOOC – C = C – COOH 2,3-диметилбутен-2-диовая
1 2 3 4 кислота
№9 слайд
Содержание слайда: Изомерия
1)углеродного скелета
CH3 – CH2 – CH2 – COOH CH3 – CH – COOH
|
CH3
бутановая кислота 2-метилпропановая кислота
2)межклассовая (сложные эфиры)
H – C = O CH3 – C = O
| |
O – C3H7 O – C2H5
пропиловый эфир этиловый эфир
муравьиной кислоты уксусной кислоты (этилэтанат)
(пропилформиат)
№10 слайд
Содержание слайда: Получение:
1.Вытеснение кислот из солей более
сильной кислотой (лаб. способ):
2CH3COONa + H2SO4 → Na2SO4 + 2CH3COOH
конц. t
2.Окисление первичных спиртов:
C2H5OH + O2 → CH3COOH + H2O
t,Cu
№11 слайд
Содержание слайда: 3.Окисление альдегидов (в лаб.- Ag2O;
Cu(OH)2; в пром.- O2, kat)
kat
2R-CH = O + O2 → 2R-COOH
4.Окисление алканов (kat – соединения
марганца)
2CH3-CH2-CH2-CH3 + 5O2 → 4CH3COOH + 2H2O
t,p,kat
№12 слайд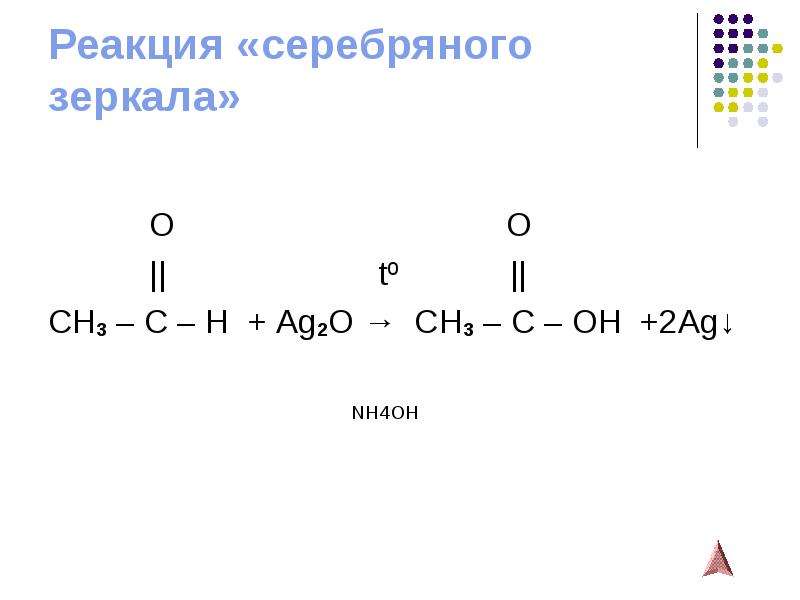
Содержание слайда: Реакция «серебряного зеркала»
O O
|| tº ||
CH3 – C – H + Ag2O → CH3 – C – OH +2Ag↓
NH4OH
№13 слайд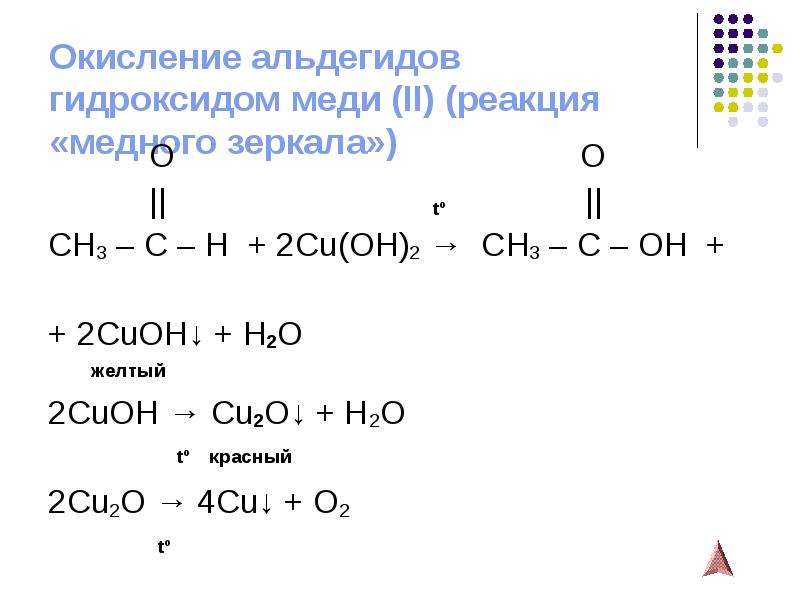
Содержание слайда: Окисление альдегидов
гидроксидом меди (II) (реакция «медного зеркала»)
O O
|| tº ||
CH3 – C – H + 2Cu(OH)2 → CH3 – C – OH +
+ 2CuOH↓ + H2O
желтый
2CuOH → Cu2O↓ + H2O
tº красный
2Cu2O → 4Cu↓ + O2
tº
№14 слайд
Содержание слайда: Химические свойства
I.Карбоновые кислоты обладают
свойствами, характерными для минеральных
кислот.
1.Из-за смещения электронной плотности от
гидроксильной группы O–H к сильно
поляризованной карбонильной группе C=O
молекулы карбоновых кислот способны к
электролитической диссоциации:
R–COOH → R–COO- + H+
№15 слайд
Содержание слайда: 2. Они реагируют с активными металлами.
2СH3COOH + Mg → (CH3COO)2Mg + H2↑
3. Реагируют с основными оксидами.
2СH3COOH + СaO → (CH3COO)2Ca + H2O
4. Реагируют с основаниями.
H–COOH + NaOH → H–COONa + H2O
3CH3COOH + Fe(OH)3 → (CH3COO)3Fe + 3H2O
№16 слайд
Содержание слайда: 5. Реагируют с солями слабых кислот.
5. Реагируют с солями слабых кислот.
2СH3CH2COOH + Na2CO3 →
→ 2CH3CH2COONa + H2O + CO2↑
СH3CH2COOH + NaHCO3 → CH3CH2COONa +
+ H2O + CO2↑
6. Реагируют с аммиаком (как основанием)
СH3COOH + NH3 → СH3COONH4
ацетат аммония
Карбоновые кислоты слабее многих
сильных минеральных кислот (HCl, H2SO4 и
т.д.) и поэтому вытесняются ими из солей:
СH3COONa + H2SO4 → CH3COOH + NaHSO4
конц. tº
№17 слайд
Содержание слайда: II.Специфические свойства карбоновых
кислот.
7. Реакция этерификации.
H2SO4 конц.
CH3–COOH + HO–CH3 ↔ CH3–COOCH3 + H2O
t уксуснометиловый
эфир
№18 слайд
Содержание слайда: Внимание!
Реакция образования сложного эфира
из кислоты и спирта называется
реакцией этерификации.
№19 слайд
Содержание слайда: 8. При воздействии водоотнимающих
реагентов в результате межмолекулярной
дегидратации образуются ангидриды.
CH3–С–OH + H–O–С–CH3 → CH3–С–O–С–CH3+
|| || P2O5 || ||
O O O O
+ H2O ангидрид уксусной
кислоты
№20 слайд
Содержание слайда: 9. Галогенирование. У карбоновых кислот
9. Галогенирование. У карбоновых кислот
под влиянием карбоксильной группы
Увеличивается подвижность атомов
водорода, стоящих при атоме углерода,
соседним с карбоксильной группой. Поэтому
они могут быть легко замещены на атомы
хлора или брома:
СH3COOH+ Cl2 → СH2ClCOOH + HCl
2-хлорэтановая кислота
(хлоруксусная кислота)
α-Галогензамещённые кислоты – более
сильные кислоты, чем карбоновые.
Хлоруксусная кислота в 100 раз сильнее
уксусной.
№21 слайд
Содержание слайда: 10. Восстановление и каталитическое
гидрирование (с большим трудом).
СH3COOH+ H2 → СH3CH=O+ H2O
kat,tº этаналь
СH3CH=O + H2 → СH3CH2OH
kat,tº этанол
№22 слайд
Содержание слайда: Применение
Муравьиная кислота – в медицине, в
пчеловодстве, в органическом синтезе, при
получении растворителей и консервантов; в
качестве сильного восстановителя.
Уксусная кислота – в пищевой и химической
промышленности (производство
ацетилцеллюлозы, из которой получают
ацетатное волокно, органическое стекло,
киноплёнку; для синтеза красителей,
медикаментов и сложных эфиров).
№23 слайд
Содержание слайда: Масляная кислота – для получения
Масляная кислота – для получения
ароматизирующих добавок, пластификато-
ров и флотореагентов.
Щавелевая кислота – в металлургической
промышленности (удаление окалины).
Стеариновая C17H35COOH и
пальмитиновая кислота C15H31COOH – в
качестве поверхностно-активных веществ,
смазочных материалов в металлообработке.
Олеиновая кислота C17H33COOH –
флотореагент и собиратель при обогащении
руд цветных металлов.
№24 слайд
Содержание слайда: Источники информации
1. Петров А.А., Бальян Х.В., Трощенко А.Т.
Органическая химия. Учебник для вузов./
Под ред. Петрова А.А. – М.: Высшая школа,
1981.
2. Хомченко Г.П. Пособие по химии для
поступающих в вузы. – М.: ООO «Издательство
Новая Волна», 2002.
3. Потапов В.М., Чертков И.Н. Строение и
свойства органических веществ. Пособие для
учащихся 10 кл. – М.: Просвещение, 1980.
№25 слайд
Содержание слайда: 4. Оганесян Э.Т. Руководство по химии
4. Оганесян Э.Т. Руководство по химии
поступающим в вузы. Справочное пособие. М.:
Высшая школа,1991.
5. Иванова Р.Г., Осокина Г.Н. Изучение
химии в 9-10 классах. Книга для учителя. – М.:
Просвещение, 1983.
6. Денисов В.Г. Химия. 10 класс. Поурочные
планы. – Волгоград: Учитель, 2004.


































