Презентация Строение атома. Периодическая таблица Менделеева. Химическая связь онлайн
На нашем сайте вы можете скачать и просмотреть онлайн доклад-презентацию на тему Строение атома. Периодическая таблица Менделеева. Химическая связь абсолютно бесплатно. Урок-презентация на эту тему содержит всего 43 слайда. Все материалы созданы в программе PowerPoint и имеют формат ppt или же pptx. Материалы и темы для презентаций взяты из открытых источников и загружены их авторами, за качество и достоверность информации в них администрация сайта не отвечает, все права принадлежат их создателям. Если вы нашли то, что искали, отблагодарите авторов - поделитесь ссылкой в социальных сетях, а наш сайт добавьте в закладки.
Презентации » Химия » Строение атома. Периодическая таблица Менделеева. Химическая связь
Оцените!
Оцените презентацию от 1 до 5 баллов!
- Тип файла:ppt / pptx (powerpoint)
- Всего слайдов:43 слайда
- Для класса:1,2,3,4,5,6,7,8,9,10,11
- Размер файла:519.75 kB
- Просмотров:94
- Скачиваний:1
- Автор:неизвестен
Слайды и текст к этой презентации:
№2 слайд


Содержание слайда: Атом
Атом состоит из двух частей – атомного ядра и электронной оболочки.
В атомном ядре сосредоточена почти вся масса атома. Частицы, образующие ядро атома называются «нуклонами». Это протоны и нейтроны.
В электронной оболочке находятся электроны – частицы с крайне малой массой и отрицательным зарядом.
№3 слайд


Содержание слайда: Атомное ядро
Атомное ядро, состоящее из частиц с одинаковым(положительным) зарядом существует благодаря так называемому «дефекту масс» Если высчитать массу атомного ядра как массу всех нуклонов, то окажется, что расчетная масса больше реальной массы атома. «Недостаток» массы конвертируется в энергию ядерных сил, удерживающих компоненты ядра вместе по формуле: E = mc2
№4 слайд


Содержание слайда: Атомное ядро
Атом в нормальном состоянии электронейтрален. Число протонов равно числу электронов. Поскольку именно электронная конфигурация определяет химические свойства, то изменение количества протонов в ядре меняет и принадлежность атома к химическому элементу.
Количество нейтронов в ядре атома на его химические свойства не влияет.
№5 слайд


Содержание слайда: Комбинации строения атомных ядер
Если у двух атомов одинаковое количество протонов, но различное количество нейтронов, то такие атомы называются «изотопами». Химические свойства изотопов одинаковы.
Если у двух атомных ядер одинаковое количество нейтронов, но разное количество протонов, то такие атомы называются «изотонами». Изотоны принадлежат к различным химическим элементам.
Если у двух атомных ядер равна сумма протонов и нейтронов, то они называются «изобарами». Как и изотоны, они принадлежат к разным химическим элементам.
№6 слайд


Содержание слайда: Электрон. Корпускулярно-волновой дуализм.
Электроны обладают двойственными свойствами, с одной стороны они демонстрируют свойства, характерные для потока частиц – имеют массу покоя, заряд, могут оказывать давление, с другой стороны движение электронов подчиняется законам распространения радиоволн – можно определить такие характеристики как длина волны и частота, присутствуют такие явления как дифракция и интерференция. Такое явление получило название «корпускулярно-волновой дуализм».
№8 слайд


Содержание слайда: Электрон. Уравнение Шрёдингера.
Важным физическим смыслом обладает квадрат волновой функции. Ψ2 для определенного объема v (математическое выражение - Ψ2/dv) определяет вероятность нахождения электрона в точке пространстве объема v.
Решение уравнения Шрёдингера на данный момент существует только для частиц с одним электроном – атом водорода, катион гелия и т.д.
№9 слайд


Содержание слайда: Электрон. Постулаты Бора.
Атом и атомные системы могут длительно пребывать только в особенных стационарных или квантовых состояниях, каждому из которых отвечает определенная энергия. В стационарном состоянии атом не излучает электромагнитных волн.
Излучение света происходит при переходе электрона из стационарного состояния с большей энергией в стационарное состояние с меньшей энергией. Энергия излученного фотона равна разности энергий стационарных состояний.
№12 слайд


Содержание слайда: Электрон. Электронное облако.
Пространство вокруг атома, в котором вероятность обнаружения электрона не менее 90% называется «электронным облаком» (или «атомной орбиталью»).
Электронное облако – всего – лишь модель движения электрона в стационарном состоянии. Со временем эта модель может быть заменена.
№14 слайд


Содержание слайда: Электрон. Главное квантовое число.
Главное квантовое число определяет энергию электрона на и размер атомной орбитали. Чем выше значение n, тем больше энергии у электрона и тем больше размер электронного облака.
Состояние электрона, характеризующееся определенным значением n называется энергетическим уровнем.
Электронные облака с одинаковым n имеют схожие размеры.
n может принимать значение целых положительных чисел. Значение n совпадает с номером периода в периодической таблице.
№15 слайд


Содержание слайда: Электрон. Орбитальное квантовое число.
Орбитальное квантовое число характеризует форму электронного облака и энергию электрона на подуровне. Максимальное значение l определяется по формуле:
l = n – 1
Каждому значению l соответствует своя форма электронного облака.
Энергетические подуровни обозначают буквами:
№19 слайд


Содержание слайда: Электрон. Спиновое квантовое число.
Спиновое квантовое число ms характеризует собственный момент количества движения электрона, обусловленный его движением вокруг своей оси; ms =± 1/2.
Знаки “+” и “–“ соответствуют различным направлениям вращения электрона – по или против часовой стрелки.
№20 слайд


Содержание слайда: Электрон.
Каждый электрон в атоме характеризуется четыремя квантовыми числами:
Главным - характеризует энергию уровня.
Орбитальным – характеризует энергию подуровня и форму электронного облака.
Магнитным – характеризует положение электронного облака в пространстве.
Спиновое – характеризует вращение электрона вокруг собственной оси.
В одном атоме не может быть двух электронов с одинаковыми квантовыми числами.
№22 слайд


Содержание слайда: Электронная конфигурация
Электронная конфигурация – совокупность всех электронов в атоме, с учетом их расположения на различных уровнях и подуровнях.
При записи электронной конфигурации:
Электронное облако условно обозначается ячейкой - □, над или под ячейкой указывается номер уровня и обозначение подуровня.
Электрон обозначается стрелкой в ячейке. Направление стрелки соответствует направлению спина.
№25 слайд


Содержание слайда: Принцип наименьшей энергии.
Любая система стремится занять самое устойчивое состояние. Как правило такому состоянию соответствует минимум энергии в системе. Соответственно электроны будут выбирать атомную орбиталь с минимальным уровнем энергии. Уровень энергии определяется правилом Клечковского.
№26 слайд


Содержание слайда: Правило Клечковского.
Правило Клечковского: при увеличении заряда ядра атома заполнение орбиталей происходит в порядке возрастания суммы главного и орбитального квантовых чисел (n+l), а при равных значениях суммы (n+l) – в порядке возрастания n.
Порядок заполнения:
1s<2s<2p<3s<3p<4s≈3d<4p<5s≈4d<5p<6s≈4f≈ 5d<6p<7s≈5f≈6d.
№30 слайд


Содержание слайда: Электронные семейства атомов
В химических реакциях участвую электроны с последнего энергетического уровня. Такие электроны называются «валентными». В зависимости от того, на каком подуровне находятся последние валентные электроны выделяют следующие семейства химических элементов:
s – элементы, валентные электроны находятся на последнем s - подуровне
p – элементы, валентные электроны находятся на последнем s- и p- подуровнях
d – элементы, валентные электроны находятся на последнем s- и предпоследнем d - подуровнях
f – элементы, заполняется f - подуровни
№31 слайд


Содержание слайда: Электронные аналоги
Электронные конфигурации валентных электронов по мере роста заряда ядра атома(то есть роста количества электронов) повторяются. На каждом энергетическом уровне есть место на s – орбиталях, начиная со второго на p – орбиталях, с третьего – на d – орбиталях. Элементы с одинаковой конфигурацией валентных уровней называются «электронными аналогами».
№32 слайд


Содержание слайда: Периодический закон
Формулировка Менделеева: свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса.
Современная формулировка: свойства химических элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины заряда атомных ядер.
№34 слайд


Содержание слайда: Периодическая таблица.
У каждого элемента в периодической таблице есть порядковый номер. Он соответствует количеству протонов в ядре атома.
Периоды – горизонтальные ряды элементов, в которых происходит последовательное заполнение одного энергетического уровня. Главное квантовое число равно номеру периода.
Группы – вертикальные ряды элементов, которые являются электронными аналогами. Номер группы равен числу валентных электронов.
№36 слайд


Содержание слайда: Стабильные электронные конфигурации
d5 и d10, - иметь заполненный наполовину или полностью d подуровень выгоднее, чем заполненный s подуровень. Именно поэтому существует явление «электронного провала» у хрома(достигается половинная емкость d подуровня), меди(достигается максимальная емкость d подуровня), и их электронных аналогов. Палладий для достижения максимальной емкости перемещает два электрона на d подуровень.
№38 слайд


Содержание слайда: Атомный радиус
Атомы и ионы не имеют строго определенных границ вследствие волновой природы электронов. Поэтому введены два условных понятия атомных радиусов:
Эффективный атомный радиус определяется экспериментально (из спектрографических данных) как ½ расстояния между центрами ядер двух соседних атомов в молекуле или кристалле.
Орбитальный атомный радиус – это расстояние от ядра атома до наиболее удаленного максимума электронной плотности.
№39 слайд


Содержание слайда: Атомный радиус
В периоде атомные радиусы с ростом порядкового номера уменьшаются (от щелочного металла к инертному газу).
В пределах каждой подгруппы элементов радиусы, как правило, увеличиваются при увеличении номера периода, так как возрастает число энергетических уровней.
При движении по диагонали эти два эффекта компенсируют друг - друга, в результате похожи по свойствам элементы, находящиеся по диагонали относительно друг - друга.
№40 слайд


Содержание слайда: Энергия ионизации
Энергия, необходимая для отрыва электрона от невозбужденного атома, называется «первой энергией ионизации». В результате ионизации атомы превращаются в положительно заряженные ионы. Энергию ионизации выражают либо в кДж/моль, либо в эВ/атом (1эВ = 1,6∙10-19 Дж).
Энергия ионизации характеризует восстановительную способность элемента или его металлические свойства. Чем меньше значение энергии ионизации тем проще атому отдать свой электрон.
№41 слайд


Содержание слайда: Энергия ионизации
Первая энергия ионизации в периоде возрастает слева направо.
В главных подгруппах с увеличением порядкового номера энергия ионизации уменьшается, что обусловлено увеличением размеров атомов.
В подгруппах d – элементов при переходе от 3d – к 5d – элементу энергии ионизации увеличиваются, это связано с усилением эффекта экранирования.
№42 слайд


Содержание слайда: Энергия сродства к электрону
Энергетический эффект присоединения электрона к нейтральному атому называется «сродством к электрону». Сродство к электрону характеризует окислительные или неметаллические свойства атома элемента. Принимая электроны, атом превращается в отрицательно заряженный ион. Эта величина так – же выражается в кДж/моль, либо в эВ/атом.
В периодах слева направо сродство к электрону и окислительные свойства элементов возрастают.
В группах сверху вниз сродство к электрону, как правило, уменьшается.
№43 слайд


Содержание слайда: Электроотрицательность
Электроотрицательность - способность атома химического элемента к оттягиванию на себя электронной плотности по сравнению с другими элементами соединения. Эта способность зависит от энергии ионизации атома и его сродства к электрону.
Существует множество способов оценки электроотрицательности, но относительное положение элементов в этих шкалах не меняется.
В периодах наблюдается общая тенденция роста величины электроотрицательности, а в подгруппах - ее падения.
Скачать все slide презентации Строение атома. Периодическая таблица Менделеева. Химическая связь одним архивом:
Похожие презентации
-
 Периодический закон Д. И. Менделеева. Строение атома. Химическая связь
Периодический закон Д. И. Менделеева. Строение атома. Химическая связь -
 Обобщающий урок по теме: «Периодический закон и периодическая система химических элементов Д. И. Менделеева. Строение атома»
Обобщающий урок по теме: «Периодический закон и периодическая система химических элементов Д. И. Менделеева. Строение атома» -
 Периодическая система химических элементов Д. И. Менделеева. Строение атома
Периодическая система химических элементов Д. И. Менделеева. Строение атома -
 Периодическая система химических элементов Д. И. Менделеева и строение атома
Периодическая система химических элементов Д. И. Менделеева и строение атома -
 Железо в периодической таблице химических элементов и строение его атома
Железо в периодической таблице химических элементов и строение его атома -
 Периодический закон и периодическая система химических элементов д. и. менделеева в свете учения о строении атома
Периодический закон и периодическая система химических элементов д. и. менделеева в свете учения о строении атома -
 Тема урока: Обобщение и систематизация знаний по теме: «Строение атома, химическая связь»
Тема урока: Обобщение и систематизация знаний по теме: «Строение атома, химическая связь» -
 Строение атома. Периодический закон Д. И. Менделеева в свете теории строения атома. Цели урока: Обобщение и углубление знания о стро
Строение атома. Периодический закон Д. И. Менделеева в свете теории строения атома. Цели урока: Обобщение и углубление знания о стро -
 «Строение атома и периодическая система» Химический диктант в 8 классе
«Строение атома и периодическая система» Химический диктант в 8 классе -
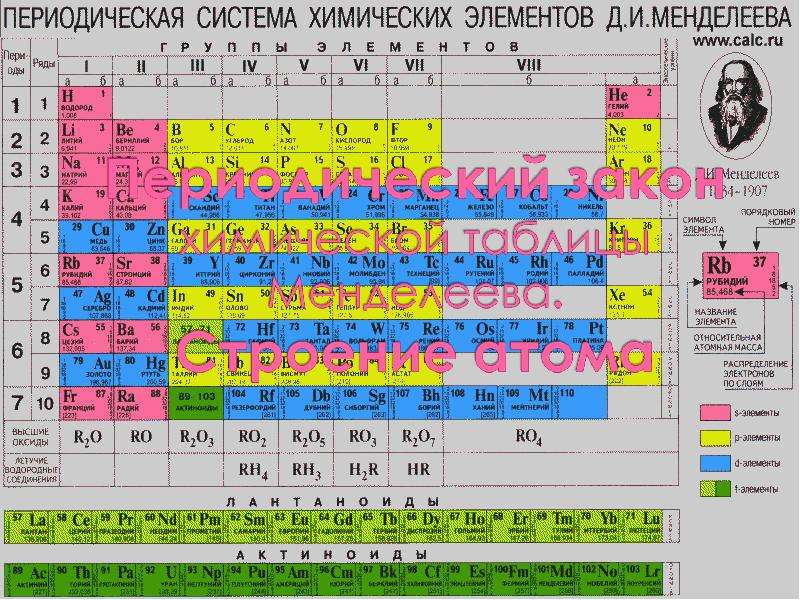 По Химии "Периодический закон химической таблицы Менделеева" - скачать смотреть
По Химии "Периодический закон химической таблицы Менделеева" - скачать смотреть
















