Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
24 слайда
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
3.60 MB
Просмотров:
90
Скачиваний:
1
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Урок по химии в 10 классе:
«Кислород и сера»
подготовил
учитель химии и биологии
ГУО СШ №163 г.Минска
Костюкевич Юрий Михайлович
№2 слайд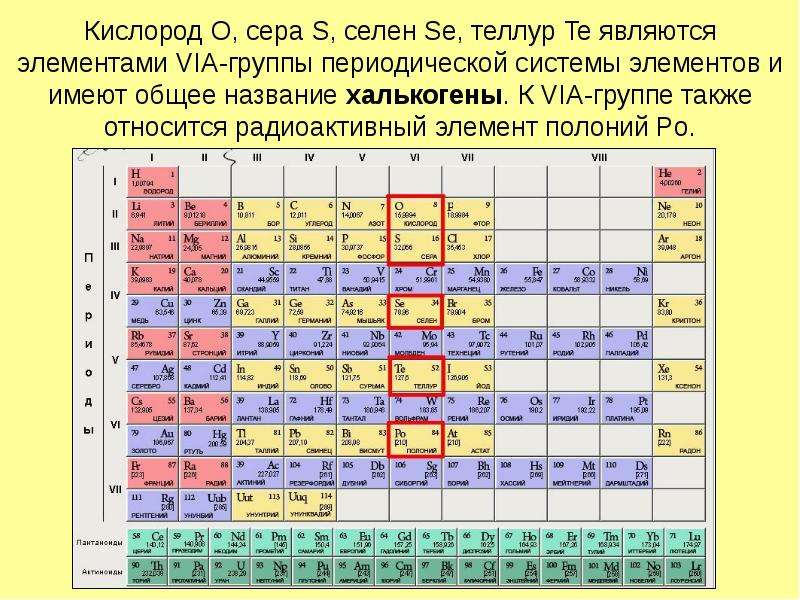
Содержание слайда: Кислород O, сера S, селен Se, теллур Te являются элементами VIА-группы периодической системы элементов и имеют общее название халькогены. К VIA-группе также относится радиоактивный элемент полоний Po.
№3 слайд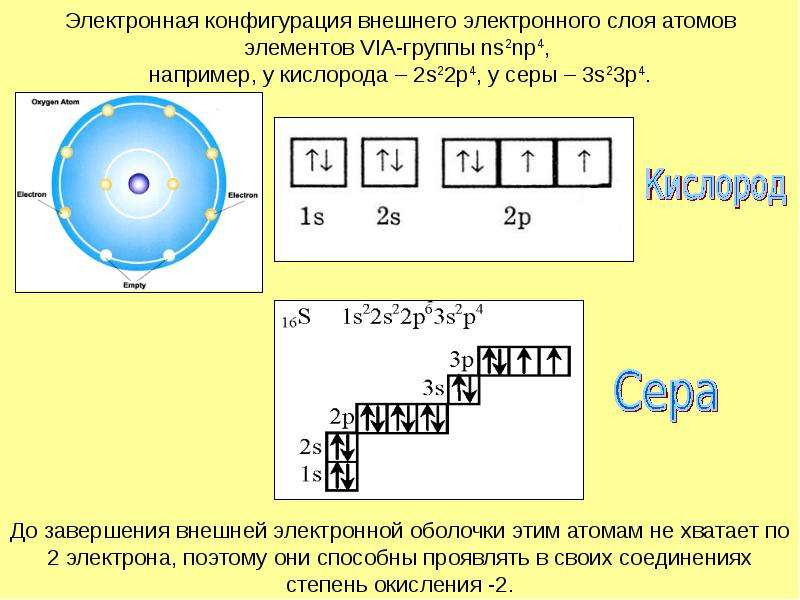
Содержание слайда: Электронная конфигурация внешнего электронного слоя атомов элементов VIA-группы ns2np4,
например, у кислорода – 2s22p4, у серы – 3s23p4.
№4 слайд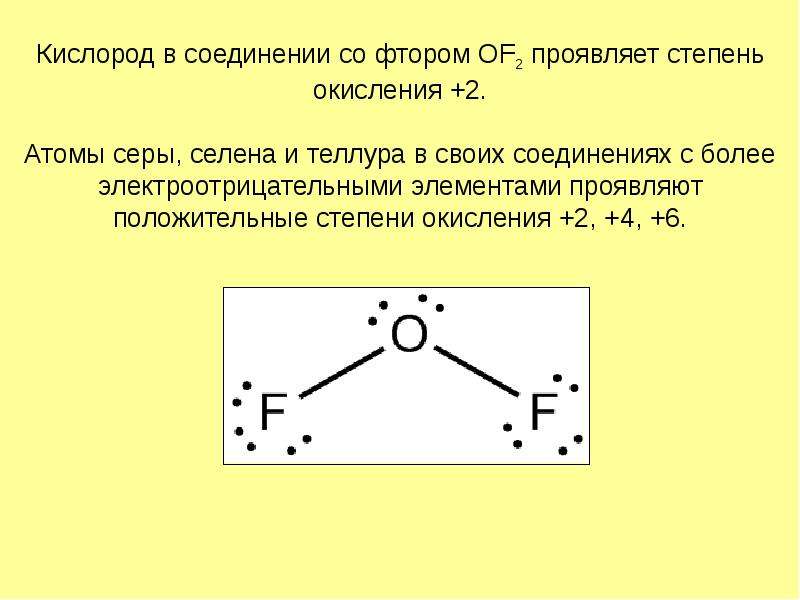
Содержание слайда: Кислород в соединении со фтором OF2 проявляет степень окисления +2.
Атомы серы, селена и теллура в своих соединениях с более электроотрицательными элементами проявляют положительные степени окисления +2, +4, +6.
№5 слайд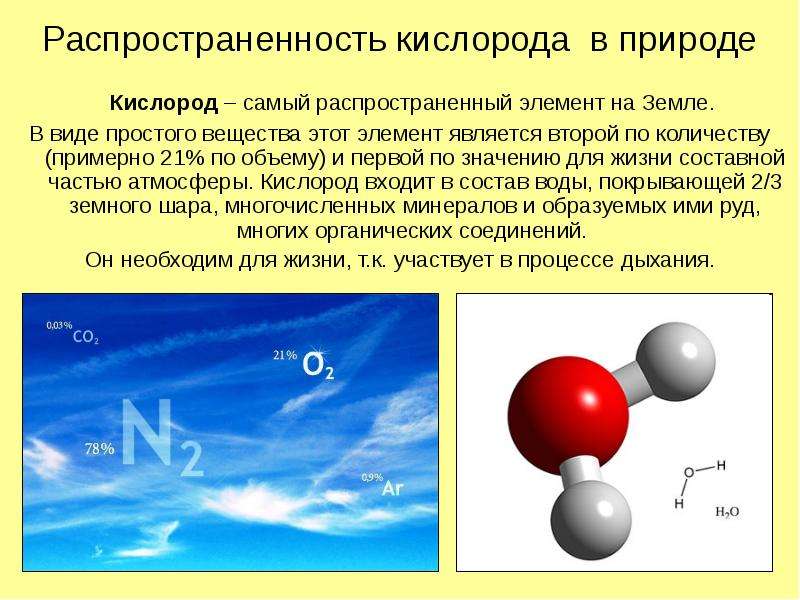
Содержание слайда: Распространенность кислорода в природе
Кислород – самый распространенный элемент на Земле.
В виде простого вещества этот элемент является второй по количеству (примерно 21% по объему) и первой по значению для жизни составной частью атмосферы. Кислород входит в состав воды, покрывающей 2/3 земного шара, многочисленных минералов и образуемых ими руд, многих органических соединений.
Он необходим для жизни, т.к. участвует в процессе дыхания.
№6 слайд
Содержание слайда: Распространенность серы в природе
Сера в природе встречается в самородном состоянии, в виде соединений с металлами – сульфидов и сульфатов. Сера относится к жизненно важным химическим элементам, она входит в состав биологических тканей всех растений и животных.
№7 слайд
Содержание слайда: Кислород
№8 слайд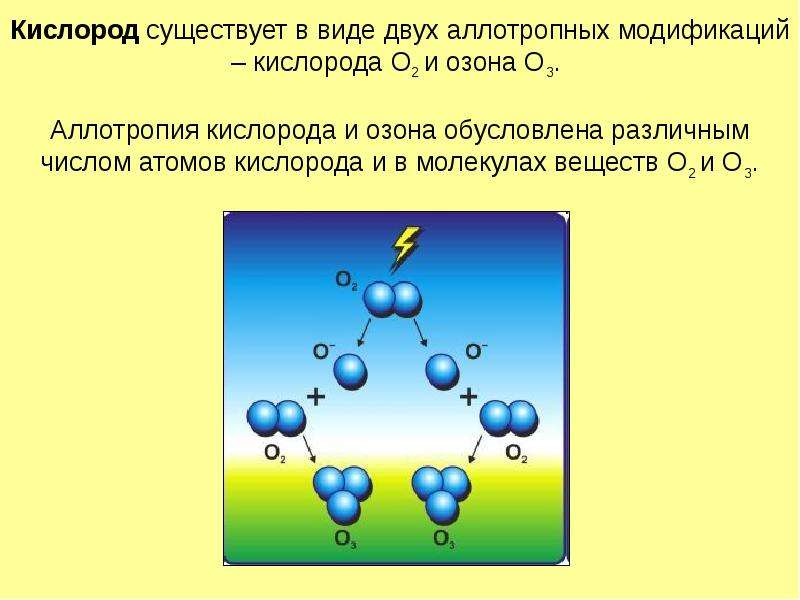
Содержание слайда: Кислород существует в виде двух аллотропных модификаций – кислорода О2 и озона О3.
Аллотропия кислорода и озона обусловлена различным числом атомов кислорода и в молекулах веществ О2 и О3.
№9 слайд
Содержание слайда: Простые вещества кислород и озон различаются по своим химическим свойствам. Кислород непосредственно взаимодействует со всеми простыми веществами,
кроме золота, платины и галогенов.
Например, кислород способен окислять металлы:
№10 слайд
Содержание слайда: Озон является более сильным окислителем, чем кислород. Многие малоактивные металлы, например серебро, ртуть, он окисляет уже при обычных условиях:
№11 слайд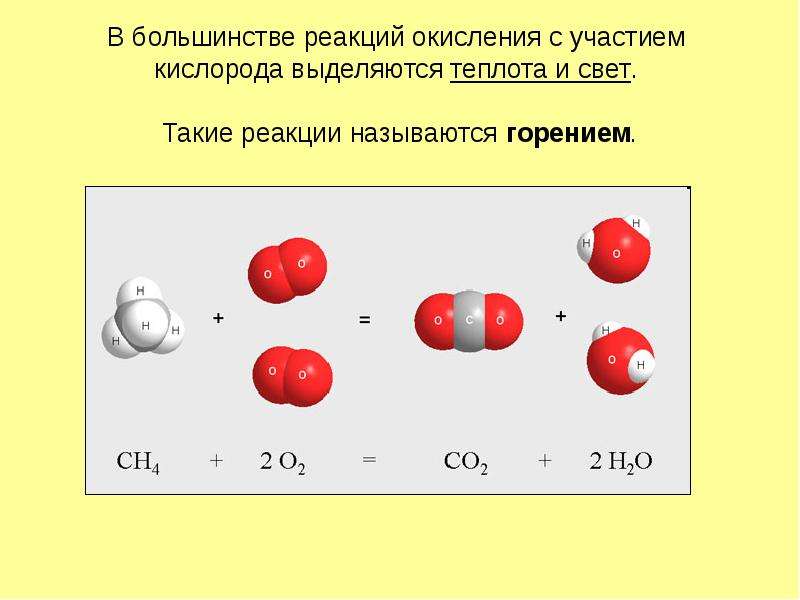
Содержание слайда: В большинстве реакций окисления с участием
кислорода выделяются теплота и свет.
Такие реакции называются горением.
№12 слайд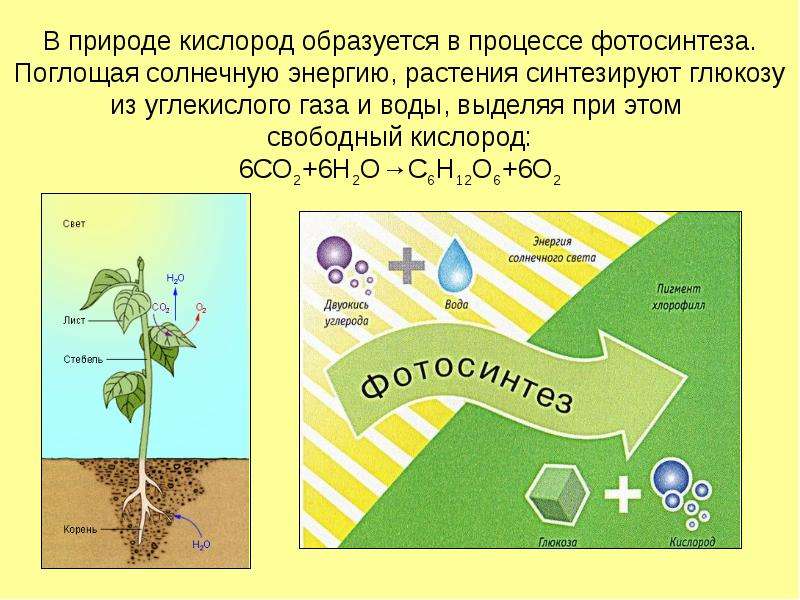
Содержание слайда: В природе кислород образуется в процессе фотосинтеза. Поглощая солнечную энергию, растения синтезируют глюкозу из углекислого газа и воды, выделяя при этом
свободный кислород:
6CO2+6H2O→C6H12O6+6O2
№13 слайд
Содержание слайда: Озон получают при действии электрического разряда на кислород в специальном приборе – озонаторе.
В природе озон образуется при грозовых разрядах.
№14 слайд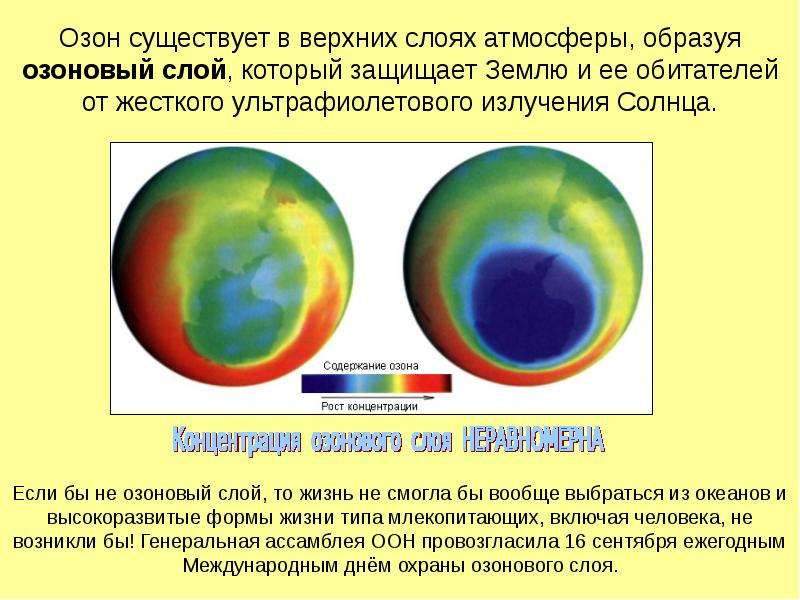
Содержание слайда: Озон существует в верхних слоях атмосферы, образуя озоновый слой, который защищает Землю и ее обитателей от жесткого ультрафиолетового излучения Солнца.
№15 слайд
Содержание слайда: Применение кислорода
Для дыхания:
Медицинский кислород хранится в металлических газовых баллонах высокого давления. Для подачи кислорода и кислородно-воздушных смесей применяются кислородные ингаляторы различных моделей и модификаций.
- Кислород применяют и для обогащения кислородом водной среды в рыбоводстве.
№16 слайд
Содержание слайда: Применение кислорода
- В качестве окислителя для ракетного топлива применяется жидкий кислород, пероксид водорода, азотная кислота и другие богатые кислородом соединения. Смесь жидкого кислорода и жидкого озона — один из самых мощных окислителей ракетного топлива.
- В химической промышленности кислород используют как реактив-окислитель в многочисленных синтезах.
- Кислород в баллонах голубого цвета широко используется для газопламенной резки и сварки металлов.
№17 слайд
Содержание слайда: Применение озона О3
- при получении многих веществ в лабораторной и промышленной практике;
- для отбеливания бумаги;
- для очистки воды и воздуха от микроорганизмов (озонирование);
- для дезинфекции помещений и одежды.
№18 слайд
№19 слайд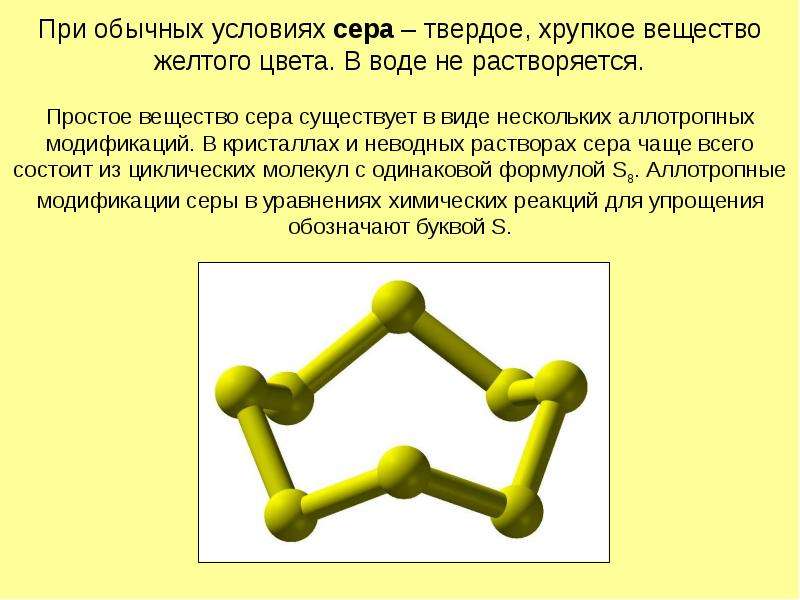
Содержание слайда: При обычных условиях сера – твердое, хрупкое вещество желтого цвета. В воде не растворяется.
Простое вещество сера существует в виде нескольких аллотропных модификаций. В кристаллах и неводных растворах сера чаще всего состоит из циклических молекул с одинаковой формулой S8. Аллотропные модификации серы в уравнениях химических реакций для упрощения обозначают буквой S.
№20 слайд
Содержание слайда: Химические свойства серы
Окислительные свойства серы проявляются при ее взаимодействии с металлами, кроме золота и платины, например:
Fe+S=FeS
Сера взаимодействует с неметаллами, например горит в кислороде:
S+O2=SO2
При взаимодействии серы с водородом при высокой температуре образуется сероводород:
S+H2↔H2S
№21 слайд
Содержание слайда: Применение серы
Серу применяют для производства серной кислоты, вулканизации каучука, как фунгицид в сельском хозяйстве и как сера коллоидная — лекарственный препарат.
№22 слайд
№23 слайд
Содержание слайда: Домашнее задание:
Параграф §45.
№24 слайд
Содержание слайда: Список используемых источников
http://ru.wikipedia.org/wiki/Кислород
http://ru.wikipedia.org/wiki/Сера
http://ru.wikipedia.org/wiki/Сульфид_железа(II)
http://ru.wikipedia.org/wiki/Озоновый_слой
http://shkola.lv/index.php?mode=cht&chtid=367
http://www.innovateus.net/science/what-oxygen
http://www.daviddarling.info/encyclopedia/O/oxygen.html
http://chemistry-chemists.com/N4/212-247.htm
http://www.ebio.ru/org07.html
http://www.prostozavod.com.ua/ekotexnologii/ozon-kak-on-vliyaet-na-vsex-nas.html
http://www.ua.all.biz/sera-komovaya-kuplyu-sera-tehnicheskaya-v-big-g1925507
http://www.liveinternet.ru/tags/%F1%E5%F0%E0/page3.html
http://www.vetlek.ru/shop/?gid=1472&pg=3

































