Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
36 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
3.03 MB
Просмотров:
138
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Характеристика элементов VII группы главной подгруппы
Хлор
Выполнила Ширяева София
ХБ-5
№2 слайд
№3 слайд
№4 слайд
№5 слайд
№6 слайд
Содержание слайда: Нахождение в природе
№7 слайд
№8 слайд
№9 слайд
№10 слайд
№11 слайд
Содержание слайда: Характеристика химического элемента
Хлор – элемент VII А группы. Порядковый номер 17
Относительная атомная масса: 35,4527 а. е. м. (г/моль)
Количество протонов, нейтронов, электронов: 17,18,17
Строение атома:
№12 слайд
Содержание слайда: Электронная формула:
Типичные степени окисления: -1, 0, +1, +3, +4, +5, +7
Энергия ионизации: 1254,9(13,01) кДж/моль (эВ)
Сродство к электрону: 349 (кДж/моль)
Электроотрицательность по Полингу: 3,20
№13 слайд
Содержание слайда: Характеристика простого вещества
Тип связи: ковалентная неполярная
Молекула двухатомная
Изотопы: 35Cl (75,78 %) и 37Cl(24,22 %)
Тип кристаллической решетки: молекулярная
№14 слайд
Содержание слайда: Термодинамические параметры
№15 слайд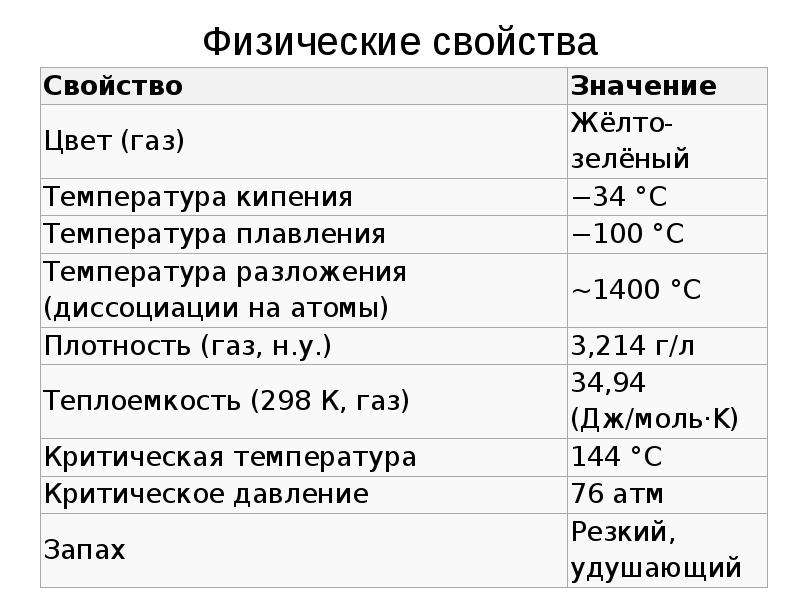
Содержание слайда: Физические свойства
№16 слайд
Содержание слайда: Химические свойства
1. Реакция дисмутации («хлорная вода»)
1 стадия: Cl2 + H2O = HCl + HOCl
2 стадия: HOCl = HCl + [О] – атомарный кислород
№17 слайд
Содержание слайда: 3. Взаимодействие со сложными веществами
а) с водой: см. выше реакция дисмутации
б) с кислородсодержащими кислотами: не реагирует!
в) с растворами щелочей:
на холоду: Cl2 + 2NaOH = NaCl + NaClO + H2O
при нагревании: 3Cl2+ 6 KOH = 5KCl + KClO3 + 3H2O
д) со многими органическими веществами:
Cl2 + CH4 = CH3Cl + HCl
C6H6 + Cl2 = C6H5Cl + HCl
№18 слайд
Содержание слайда: Важнейшие соединения хлора
№19 слайд
Содержание слайда: Свойства соляной кислоты:
Свойства соляной кислоты:
Очень устойчива к нагреванию
В воде кислота
Слабый окислитель по протону
Под действием сильных окислителей анион окисляется
№20 слайд
№21 слайд
Содержание слайда: Смесь 3v HCl : 1v HNO3 называется «царской водкой».
Смесь 3v HCl : 1v HNO3 называется «царской водкой».
Она способна растворять даже золото и платину.
4 H3O+ + 3 Cl− + NO3− = NOCl + Cl2 + 6 H2O
Расстворение идет благодаря высокой концентрации хлорид-ионов :
3 Pt + 4 HNO3 + 18 HCl → 3 H2[PtCl6] + 4 NO↑ + 8 H2O
Для хлороводорода также характерны реакции присоединения к кратным связям (электрофильное присоединение):
R-CH=CH2 + HCl → R-CHCl-CH3
R-C≡CH + 2 HCl → R-CCl2-CH3
№22 слайд
№23 слайд
Содержание слайда: Оксид хлора (I), оксид дихлора, ангидрид хлорноватистой кислоты (Cl2O)
Оксид хлора (I), оксид дихлора, ангидрид хлорноватистой кислоты (Cl2O)
В нормальных условиях представляет собой буровато-жёлтый газ с характерным запахом, напоминающим запах хлора. При температурах ниже 2 °C — жидкость золотисто-красного цвета. Ядовит: поражает дыхательные пути. При больших концентрациях взрывоопасен. Самопроизвольно медленно разлагается:
Кислотный и солеобразующий. Хорошо растворим в воде с образованием слабой хлорноватистой кислоты:
Быстро реагирует со щелочами:
Cl2O + 2NaOH(разб.) = 2NaClO + H2O
№24 слайд
№25 слайд
Содержание слайда: Проявляет окислительно-восстановительные свойства.
Проявляет окислительно-восстановительные свойства.
2ClO2 + 5H2SO4 (разб.) + 10FeSO4 = 5Fe2(SO4)3 + 2HCl + 4H2O
ClO2 + O3 = ClO3 + O2
ClO2 + 2NaOHхол. = NaClO2 + NaClO3 + H2O
ClO2 реагирует со многими с органическими соединениями и выступает окислителем средней силы.
№26 слайд
№27 слайд
№28 слайд
№29 слайд
Содержание слайда: Получение
№30 слайд
Содержание слайда: Получение
№31 слайд
Содержание слайда: Самые большие запасы хлора содержатся в составе солей вод морей и океанов
№32 слайд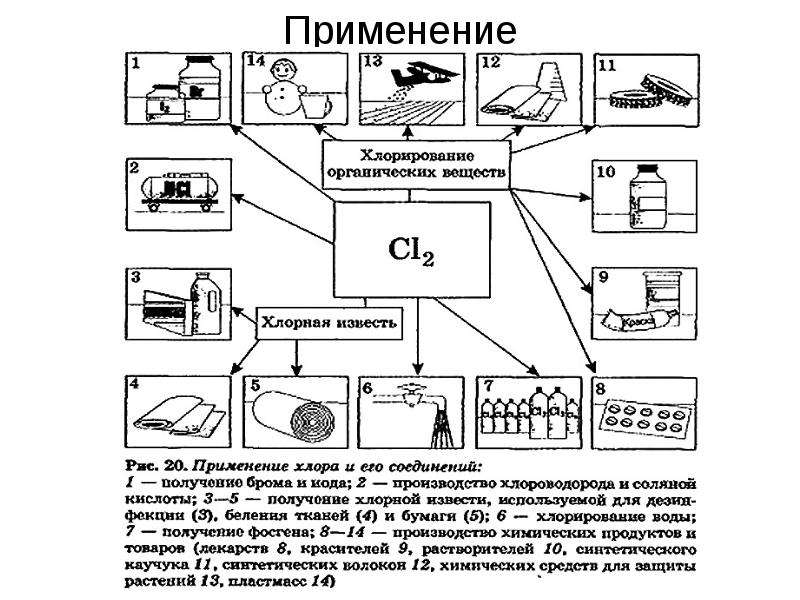
Содержание слайда: Применение
№33 слайд
Содержание слайда: Физиологическое действие
№34 слайд
№35 слайд
№36 слайд













































