Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
21 слайд
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
580.50 kB
Просмотров:
159
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Элементы IV группы главной подгруппы.
Углерод.
План:
1. Нахождение в природе.
2. Электронное строение и положение в ПСХЭ.
3. Методы получения: лабораторные и промышленные.
4. Аллотропные видоизменения углерода.
5. Химические свойства. Карбиды.
6. Применение. Токсичность.
7. Интересное об углероде.
№2 слайд
Содержание слайда: Нахождение в природе.
Среди множества химических элементов, без которых невозможно существование жизни на Земле, углерод является главным. Более 99% углерода в атмосфере содержится в виде углекислого газа. Около 97% углерода в океанах существует в растворённой форме ( ), а в литосфере - в виде минералов.
Элементарный углерод присутствует в атмосфере в малых количествах в виде графита и алмаза, а в почве - в форме древесного угля.
№3 слайд
Содержание слайда: Положение в ПСХЭ.
Общая характеристика элементов подгруппы углерода.
№4 слайд
Содержание слайда: Электронное строение
№5 слайд
Содержание слайда: Методы получения: лабораторные и промышленные.
Углерод
Неполное сжигание метана:
СН4 + О2 = С + 2Н2О
Оксид углерода (II)
В промышленности:
Оксид углерода (II) получают в особых печах, называемых газогенераторами, в результате двух последовательно протекающих реакций. В нижней части газогенератора, где кислорода достаточно, происходит полное сгорание угля и образуется оксид углерода (IV):
C + O2 = CO2 + 402 кДж.
№6 слайд
Содержание слайда: По мере продвижения оксида углерода (IV) снизу вверх последний соприкасается с раскалённым углём:
По мере продвижения оксида углерода (IV) снизу вверх последний соприкасается с раскалённым углём:
CO2 + C = CO – 175 кДж.
Получающийся газ состоит из свободного азота и оксида углерода (II). Такая смесь называется генераторным газом. В газогенераторах иногда через раскалённый уголь продувают водяной пар:
C + H2O = CO + H2 – Q, «CO + H2» - водяной газ.
В лаборатории:
Действуя на муравьиную кислоту концентрированной серной кислотой, которая связывает воду:
HCOOH H2O + CO.
№7 слайд
Содержание слайда: Оксид углерода (IV)
Оксид углерода (IV)
В промышленности:
Побочный продукт при производстве извести:
CaCO3 CaO + CO2.
В лаборатории:
При взаимодействии кислот с мелом или мрамором:
CaCO3 + 2HCl CaCl2 + CO2+ H2O.
Карбиды
Карбиды получают при помощи прокаливания металлов или их оксидов с углём.
№8 слайд
Содержание слайда: Угольная кислота
Угольная кислота
Получают растворением оксида углерода (IV) в воде. Так как угольная кислота очень не прочное соединение, то эта реакция обратима:
CO2 + H2O H2CO3.
Кремний
В промышленности:
При нагревании смеси песка и угля:
2C + SiO2 Si + 2CO.
В лаборатории:
При взаимодействии смеси чистого песка с порошком магния:
2Mg + SiO2 2MgO + Si.
№9 слайд
Содержание слайда: Кремниевая кислота
Кремниевая кислота
Получают при действии кислот на растворы её солей. При этом она выпадает в виде студенистого осадка:
Na2SiO3 + HCl 2NaCl + H2SiO3
2H+ + SiO32- H2SiO3
№10 слайд
Содержание слайда: Аллотропные видоизменения углерода.
Углерод существует в трех аллотропных модификациях: алмаз, графит и карбин.
№11 слайд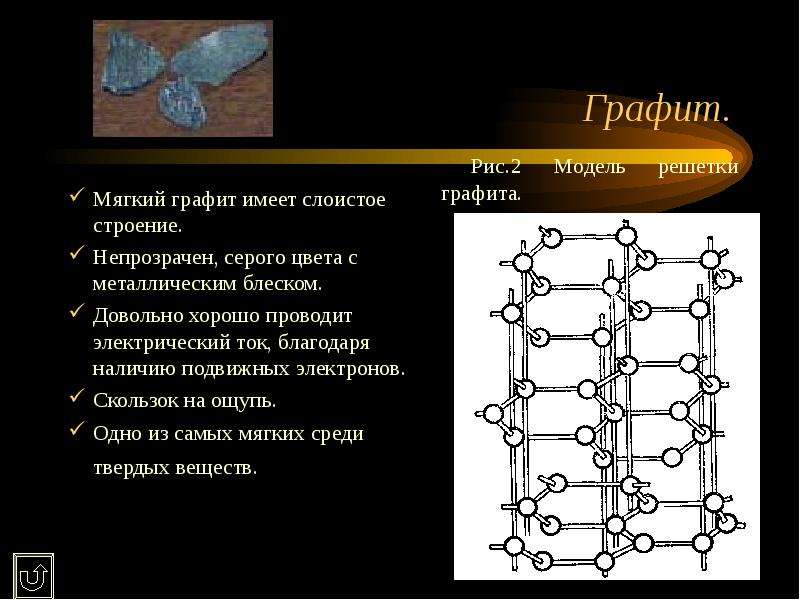
Содержание слайда: Графит.
Мягкий графит имеет слоистое строение.
Непрозрачен, серого цвета с металлическим блеском.
Довольно хорошо проводит электрический ток, благодаря наличию подвижных электронов.
Скользок на ощупь.
Одно из самых мягких среди твердых веществ.
№12 слайд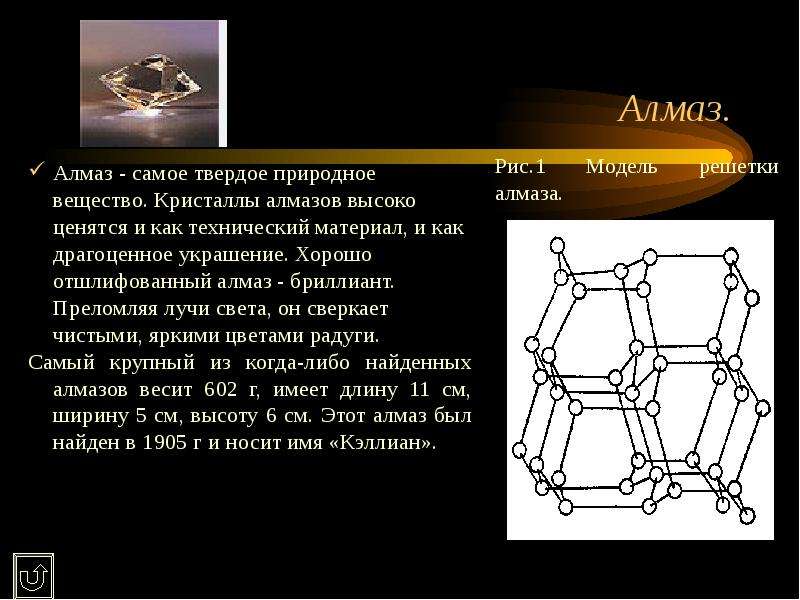
Содержание слайда: Алмаз.
Алмаз - самое твердое природное вещество. Кристаллы алмазов высоко ценятся и как технический материал, и как драгоценное украшение. Хорошо отшлифованный алмаз - бриллиант. Преломляя лучи света, он сверкает чистыми, яркими цветами радуги.
Самый крупный из когда-либо найденных алмазов весит 602 г, имеет длину 11 см, ширину 5 см, высоту 6 см. Этот алмаз был найден в 1905 г и носит имя «Кэллиан».
№13 слайд
Содержание слайда: Карбин и Зеркальный углерод.
Карбин представляет собой порошок глубокого черного цвета с вкраплением более крупных частиц.
Карбин - самая термодинамически устойчивая форма элементарного углерода.
Зеркальный углерод имеет слоистое строение.
Одна из важнейших особенностей зеркального углерода (кроме твердости, стойкости к высоким температурам и т. д.) - его биологическая совместимость с живыми тканями.
№14 слайд
Содержание слайда: Химические свойства.
Щелочи переводят кремний в соли кремниевой кислоты с выделением водорода :Si + 2КОН + H2O= К2Si03 + 2Н2
С водой углерод и кремний реагируют лишь при высоких температурах:
С + Н2О ¬ СО + Н2
Si + ЗН2О = Н2SiO3 + 2Н2
Углерод в отличие от кремния непосредственно взаимодействует с водородом: С + 2Н2 = СН4
№15 слайд
Содержание слайда: Карбиды.
Соединения углерода с металлами и другими элементами, которые по отношению к углероду являются электроположительными, называются карбидами.
При взаимодействии карбида алюминия с водой образуется метан
Al4C3 + 12H2O = 4Al (OH)3 + 3CH4
При взаимодействии с водой карбида кальция – ацетилен:
CaC2 + 2H2O = Ca (OH)2 + C2H2
№16 слайд
Содержание слайда: Применение.
Углерод определяется тем, что свыше 90 % всех первичных источников потребляемой в мире энергии приходится на органическое топливо.
Гидрокарбонат натрия продают в аптеках и продовольственных магазинах под названием питьевой соды.Питьевую соду применяют в кондитерском деле и хлебопечении.
№17 слайд
Содержание слайда: Оксид углерода (IV)
Получение сахара.
Тушение пожаров.
Производство фруктовых вод.
«Сухой лёд».
№18 слайд
Содержание слайда: Оксид кремния (IV)
Силикатных кирпичи.
Керамические изделия.
Стекло.
№19 слайд
Содержание слайда: Силикаты.
Клей.
№20 слайд
Содержание слайда: Интересный факт.
Подземный углерод мог не раз вызвать массовое вымирание на планете и постоянно грозит разразиться новой катастрофой в любой момент.
Одно из этих событий произошло 245 миллионов лет назад в конце Пермской эры, которая представляла собой самый трагический случай вымирания фауны в земной хронологии: ископаемые породы свидетельствуют о вымирании тогда около 96% всех морских обитателей.
Возможно подобный же случай привел к началу вымирания динозавров задолго до катастрофы с падением астероида 65 миллионов лет.
№21 слайд






























