Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
17 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
95.50 kB
Просмотров:
166
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Химические реакции
Выполнила
Болгова ЕД
преподаватель химии
ГБОУ ГАК с Московское
№2 слайд
Содержание слайда: Аннотация
Данная презентация может быть использована при изучении химии на 1 курсе по программе НПО по при изучении темы «Химические реакции».
В презентации рассматривается классификация химических реакций, протекающих с изменением состава вещества.
№3 слайд
Содержание слайда: Цели и задачи урока
Образовательная
обобщить и систематизировать знания обучающихся о классификации химических реакций
отработать навыки определения типа реакции и составления уравнений химических реакций разных типов
Развивающие
Развитие логического мышления обучающихся
Развивать у будущих производственников умение делать обобщение, выводы
Воспитательная
Продолжить формирование творческого начала обучающихся.
Воспитывать инициативу и самостоятельность в трудовой деятельности.
№4 слайд
Содержание слайда: Содержание
Аннотация
Цели и задачи урока
Типы химических реакций
По числу вступивших в реакцию веществ
По числу вступивших в реакцию веществ
№5 слайд
Содержание слайда: Типы химических реакций
По числу вступивших в реакцию веществ
По тепловому эффекту
По обратимости
По изменению степени окисления
По агрегатному состоянию веществ
По механизму
№6 слайд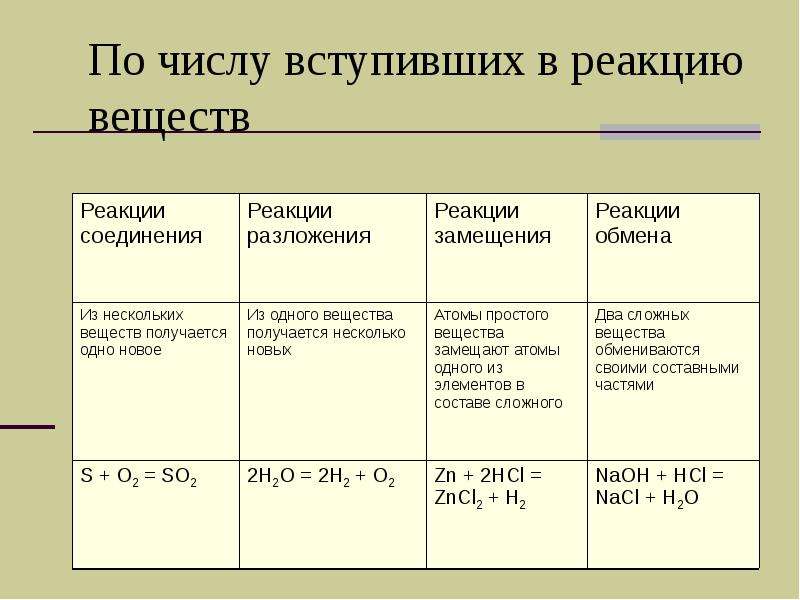
Содержание слайда: По числу вступивших в реакцию веществ
№7 слайд
Содержание слайда: Правило Бертолле
В растворах электролитов реакции идут до конца в случае, если в результате образуется осадок, газ или малодиссоциирующее вещество (например, вода)
№8 слайд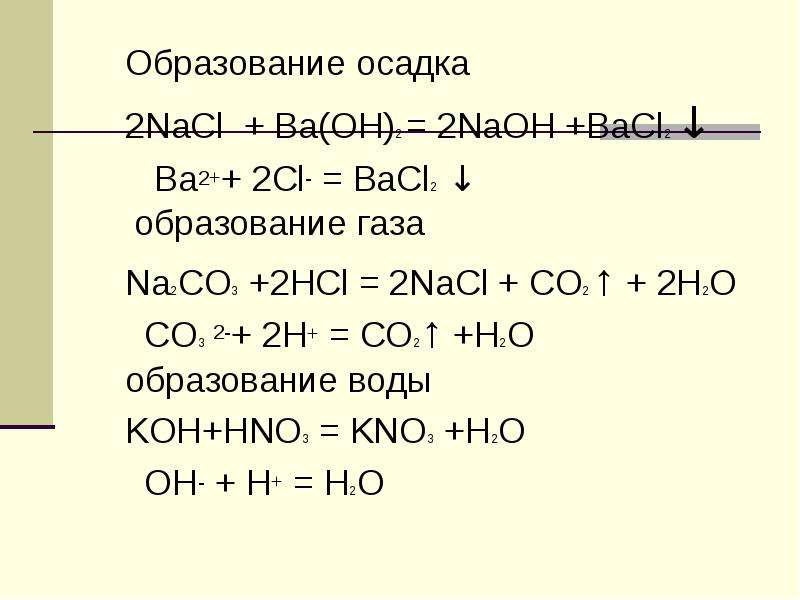
Содержание слайда: Образование осадка
Образование осадка
2NaCl + Ba(OH)2 = 2NaOH +BaCl2 ↓
Ba2++ 2Cl- = BaCl2 ↓
образование газа
Na2CO3 +2HCl = 2NaCl + CO2 ↑ + 2H2O
CO3 2-+ 2H+ = CO2↑ +H2O
образование воды
KOH+HNO3 = KNO3 +H2O
OH- + H+ = H2O
№9 слайд
Содержание слайда: По тепловому эффекту
Экзотермические -
идут с выделение теплоты
S + O2 = SO2 + Q
№10 слайд
Содержание слайда: По обратимости
Необратимые -
идут только в одном направлении
Условия: образование осадка или слабого электролита (Н2О), выделение газа, выделение большого количества теплоты
№11 слайд
Содержание слайда: По изменению степени окисления
Идут без изменения степени окисления элементов
CaCO3 = CaO + CO2
№12 слайд
Содержание слайда: По механизму
Ионные
NaOH + HCl = NaCl + H2O
Na+ + OH- + H+ +Cl- =
Na+ + Cl- + H2O
H+ + OH- = H2O
№13 слайд
Содержание слайда: По агрегатному состоянию веществ
Гомогенные -
между веществами нет поверхности раздела фаз
H2 + Cl2 = 2HCl
№14 слайд
Содержание слайда: Проверь себя
Перепиши схемы химических реакций в тетрадь, расставьте коэффициенты.
Mn(OH)2 MnO + H2O -Q
FeSO4 + BaCI2 BaSO4 + FeCI2
Ba(HCO3)2 BaCO3 + CO2 + H2O
Si + CI2 SiCI4
As2O5 + H2O H3AsO4
P + CI2 PCI3
K2SO4 + AgNO3 Ag2So4 + KNO3
Sn + HCI SnCI2 + H2 +Q
Определите тип химических реакций.
№15 слайд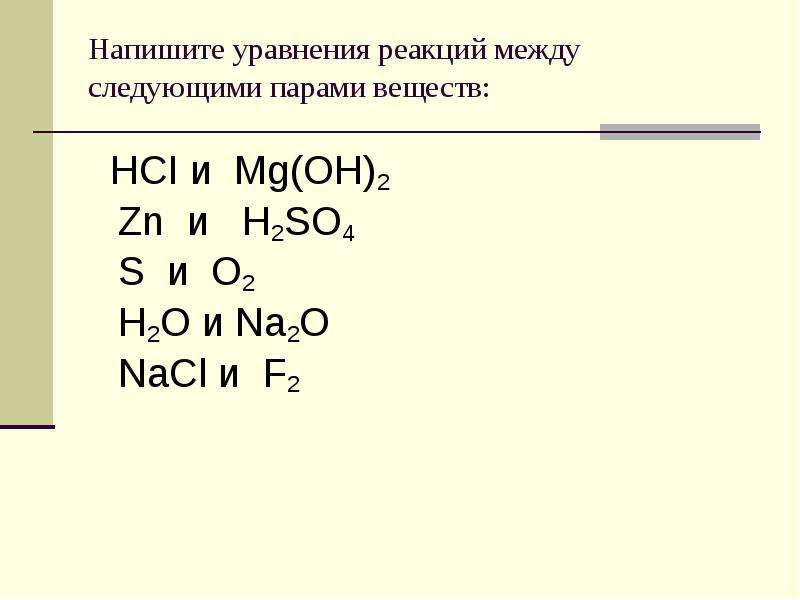
Содержание слайда: Напишите уравнения реакций между следующими парами веществ:
HCI и Mg(OH)2
Zn и H2SO4
S и O2
H2O и Na2O
NaCl и F2
№16 слайд
Содержание слайда: Вывод
Поставленные цели урока достигнуты
№17 слайд
Содержание слайда: Ресурсы
Литература,
Габриелян О. С. Химия 11кл, М:Дрофа, 2008.
Габриелян О. С. Рунов Н. Н. Химический эксперимент в школе 11кл
Журин А. А. Химические уравнения задания для самостоятельной работы
Интернет ресурсы
http://www.hemi.nsu.ru
http://chemistry.ru
http://www.chem.km.ru/


























