Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
62 слайда
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
11.52 MB
Просмотров:
60
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Разработала:
Диденко Кристина Васильевна
учитель химии
МБОУ Гришинская школа
№2 слайд
Содержание слайда: Девиз: «Знать – значит победить»
Цель работы Задачи
Изучить коррозию металлов, исследовать причины и условия её возникновения.
Актуальность
Практическое использование современных взглядов на коррозию металлов и сплавов и защиты металлических изделий от разрушения в быту и на производстве.
№3 слайд
№4 слайд
№5 слайд
№6 слайд
Содержание слайда: «Знать – значит победить»
А. Н. Несмеянов
Цели урока:
познакомиться с типами коррозии, со способами защиты металлов от коррозии;
объяснить реакции окисления-восстановления, протекающие на поверхности металла в процессе коррозии.
№7 слайд
Содержание слайда: Графический диктант
№8 слайд
Содержание слайда: Графический диктант
Металлом можно воспользоваться для получения серебра из его соли.
Может вытеснять цинк из его соли.
В реакциях с галогенами является окислителем.
При хранении на открытом воздухе быстро окисляется.
Раствор соли этого металла используют для борьбы с вредителями сада.
Легко режется ножом.
Проверяем.
№9 слайд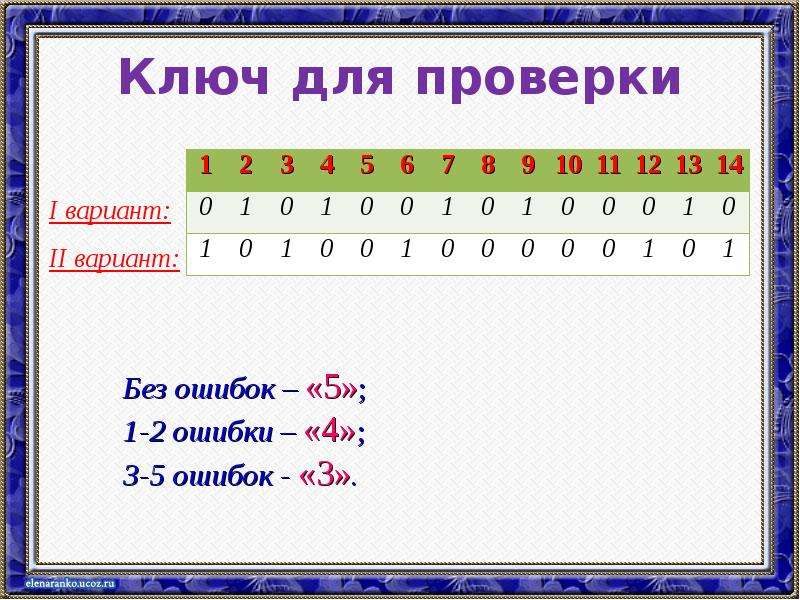
Содержание слайда: Ключ для проверки
I вариант:
II вариант:
Без ошибок – «5»;
1-2 ошибки – «4»;
3-5 ошибок - «3».
№10 слайд
Содержание слайда: Историческая страница
№11 слайд
Содержание слайда: Информационная
страница
КОРРОЗИЯ – это разрушение металлов и сплавов под действием внешней среды.
Коррозия – от латинского corrodere – разъедать.
№12 слайд
№13 слайд
Содержание слайда: Почему темнеет яблоко?
№14 слайд
Содержание слайда: Интересные факты
№15 слайд
Содержание слайда: Интересные факты
№16 слайд
Содержание слайда: Информационная
страница
КОРРОЗИЯ – это окислительно-восстановительный процесс, при котором атомы металла переходят в ионы. В роли окислителя, как правило, выступают О2 и Н+.
№17 слайд
№18 слайд
Содержание слайда: Химическая коррозия
№19 слайд
Содержание слайда: Электрохимическая коррозия
№20 слайд
№21 слайд
№22 слайд
№23 слайд
Содержание слайда: По характеру разрушений
№24 слайд
Содержание слайда: Сплошная коррозия
№25 слайд
Содержание слайда: Местная коррозия
№26 слайд
Содержание слайда: Причины возникновения местной коррозии
№27 слайд
Содержание слайда: Факторы,
влияющие
на скорость коррозии
№28 слайд
Содержание слайда: Цель:
исследовать влияние сред, контактов металлов на скорость коррозии
№29 слайд
№30 слайд
Содержание слайда: Метод исследования
№31 слайд
Содержание слайда: Что делали
1 стакан: Fe + H2O
2 стакан: Fe + р-р NaCl
3 стакан: Fe, Cu + р-р NaCl
4 стакан: Fe, Zn + р-р NaCl
5 стакан: Fe + р-р (NaCl + NaOH)
№32 слайд
Содержание слайда: Результат
эксперимента
№33 слайд
Содержание слайда: Что наблюдали
Стакан №1.
Железо слабо прокорродировало, в чистой воде коррозия идет медленнее, так как это слабый электролит.
№34 слайд
Содержание слайда: Стакан №2.
Стакан №2.
Скорость коррозии выше, чем в первом случае, следовательно, NaCl увеличивает скорость коррозии.
№35 слайд
№36 слайд
№37 слайд
№38 слайд
Содержание слайда: Вывод
Действительно, мы увидели, что скорость коррозии меняется в зависимости от контакта с другими химическими веществами. Коррозию железа усиливает контакт с менее активным металлом (Cu) и присутствие в воде растворимой соли; уменьшает контакт с более активным металлом и наличие в воде щелочи.
Из наблюдений можно сделать вывод, что алюминий для протекторной защиты использовать нельзя, так как железо все равно разрушается.
№39 слайд
№40 слайд
Содержание слайда: Консервная банка
№41 слайд
Содержание слайда: Оцинкованное ведро
№42 слайд
№43 слайд
Содержание слайда: Ингибиторы –
это вещества, способные в малых количествах замедлять протекание химических процессов или останавливать их.
№44 слайд
Содержание слайда: Практическая
страница
Способы защиты металлов от коррозии:
Шлифование поверхностей.
№45 слайд
Содержание слайда: Практическая
страница
Способы защиты металлов от коррозии:
Использование легированных сталей
№46 слайд
Содержание слайда: Практическая
страница
Способы защиты металлов от коррозии:
Нанесение защитных покрытий:
Неметаллических (лаки, эмали, смазка, масла)
№47 слайд
Содержание слайда: Практическая
страница
Способы защиты металлов от коррозии:
Нанесение защитных покрытий:
металлических (покрытие одного металла слоем другого)
Например никелирование, лужение, хромирование.
№48 слайд
Содержание слайда: Практическая
страница
Способы защиты металлов от коррозии:
Нанесение защитных покрытий:
Химических:
Воронение,
Оксидные пленки,
Полимерные пленки
И другие…
№49 слайд
Содержание слайда: Практическая
страница
Способы защиты металлов от коррозии:
Электрохимические методы
Протекторная защита – к металлической конструкции присоединяется кусок более активного металла, который служит анодом и разрушается.
№50 слайд
Содержание слайда: Практическая
страница
Способы защиты металлов от коррозии:
Электрохимические методы:
Катодная защита – конструкция присоединяется к внешнему источнику тока (так защищают трубы нефтепроводов и газопроводов)
№51 слайд
Содержание слайда: Практическая
страница
Способы защиты металлов от коррозии:
Обработка среды
(В котельных установках из воды удаляется кислород.)
№52 слайд
Содержание слайда: Нанотехнология.
Самовосстанавливающийся газопровод.
№53 слайд
Содержание слайда: Shewanella oneidensis — грамотрицательная, факультативно анаэробная бактерия
№54 слайд
Содержание слайда: «Стоп! Красный свет!»
Вопросы:
Что такое коррозия?
Какие виды коррозии вы знаете?
Когда и кем была создана теория коррозии металлов?
Когда и кем была сформулирована теория электрохимической коррозии?
Как можно замедлить коррозию?
№55 слайд
Содержание слайда: Задача
№56 слайд
Содержание слайда: Задача
№57 слайд
Содержание слайда: Задача
№58 слайд
Содержание слайда: Задача
№59 слайд
Содержание слайда: Задача
№60 слайд
№61 слайд
Содержание слайда: Рефлексия
№62 слайд
Содержание слайда: Домашнее задание
24
стр. 108-118.
вопросы 1, 4, 5 на стр. 118.
+ решить задачу №6 на стр. 118. (на отлично)







































































