Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
12 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
342.50 kB
Просмотров:
96
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Урок №5
8 класс
по учебнику О.С.Габриеляна
Учитель химии I категории
МОУ СОШ №6 Нягани
ХМАО-Югры Тюменской области
Ким Наталья Викторовна
№2 слайд
Содержание слайда: тема урока
Относительная атомная и молекулярная массы
№3 слайд
Содержание слайда: Химический диктант
№4 слайд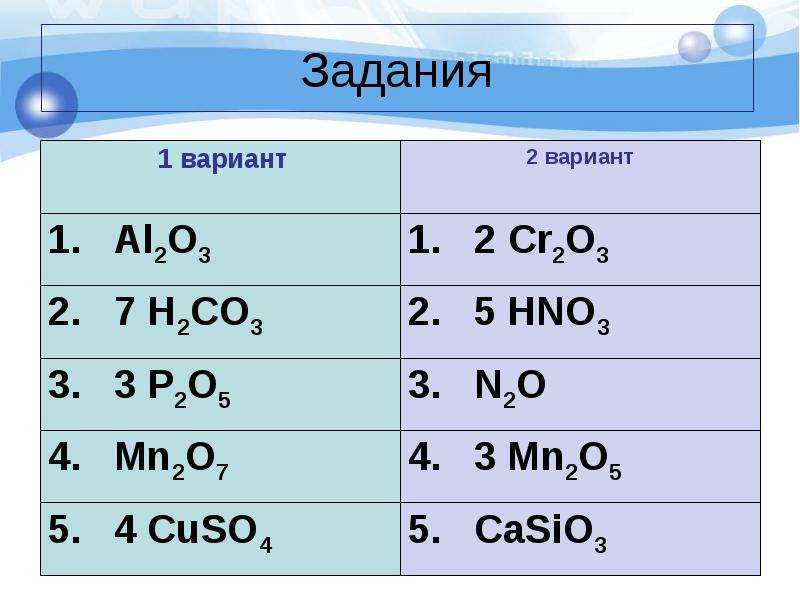
Содержание слайда: Задания
№5 слайд
Содержание слайда: Относительная атомная масса
Атомы элементов характеризуются определённой (только им присущей) массой.
Например, масса
атома Н равна 1,67 · 10−23 г, атома С − 1,995 · 10−23 г, атома О − 2,66 · 10−23 г.
№6 слайд
Содержание слайда: Относительная атомная масса
Пользоваться такими малыми значениями неудобно, поэтому введено понятие об относительной атомной массе Аr - отношении массы атома данного элемента к атомной единице массы (1,6605 · 10−24 г).
№7 слайд
Содержание слайда: Относительная молекулярная масса - Мr
Значения относительной молекулярной массы рассчитываются из значений относительной атомной массы с учётом числа атомов каждого элемента в формульной единице сложного вещества. Атомы и молекулы - частицы чрезвычайно малые, поэтому порции веществ, которые берутся для химических реакций, характеризуются физическими величинами, соответствующими большому числу частиц.
Мr = bAr (элемента 1)+ mAr(элемента 2)
№8 слайд
Содержание слайда: Относительная молекулярная масса - Мr
Установлено, что
12 г углерода (в виде графита или алмаза) содержат 6,02 · 1023 атомов С (Аr = 12),
28 г азота N2 содержат то же число молекул N2 (Mr = 28),
18 г H2O - то же число молекул H2O (Mr = 18) и т.д.
№9 слайд
Содержание слайда: Массовая доля элемента в сложном веществе
По известной химической формуле сложного вещества определяют массовые доли элементов, входящих в это вещество. Массовая доля элемента (wЭ) в общей массе сложного вещества - это отношение массы, приходящейся на этот элемент (то есть массы части), к массе всего вещества (то есть к массе целого):
wЭ = mЭ/mвещ
№10 слайд
Содержание слайда: Массовая доля элемента в сложном веществе
Массовая доля элемента - это доля от единицы или доля от 100%. В сложном веществе wЭ всегда меньше единицы (или меньше 100%).
Например, для воды H2O
wH = 0,11 (11%) и wO = 0,89 (89%).
Сумма массовых долей элементов, входящих в сложное вещество, равна 1 (100%).
№11 слайд
Содержание слайда: Домашнее задание
§ 5,
№ 6,7,8
№12 слайд
Содержание слайда: Использованы источники
1. Учебник «Химия-8», автор: О.С. Габриелян;
2. Анимационные картинки с сайтов:
http://www.chemistry.ssu.samara.ru/chem5/index5.htm;
http://chemistry.ru/index.php.





















