Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
30 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
1.63 MB
Просмотров:
91
Скачиваний:
1
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Общая и неорганическая химия. Лекция 21
Общая характеристика элементов VА-группы. Азот
№2 слайд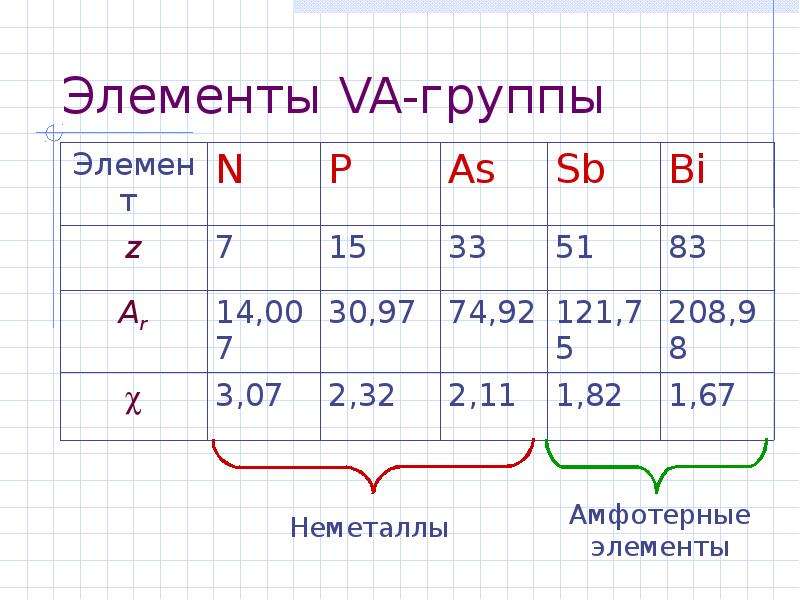
Содержание слайда: Элементы VA-группы
№3 слайд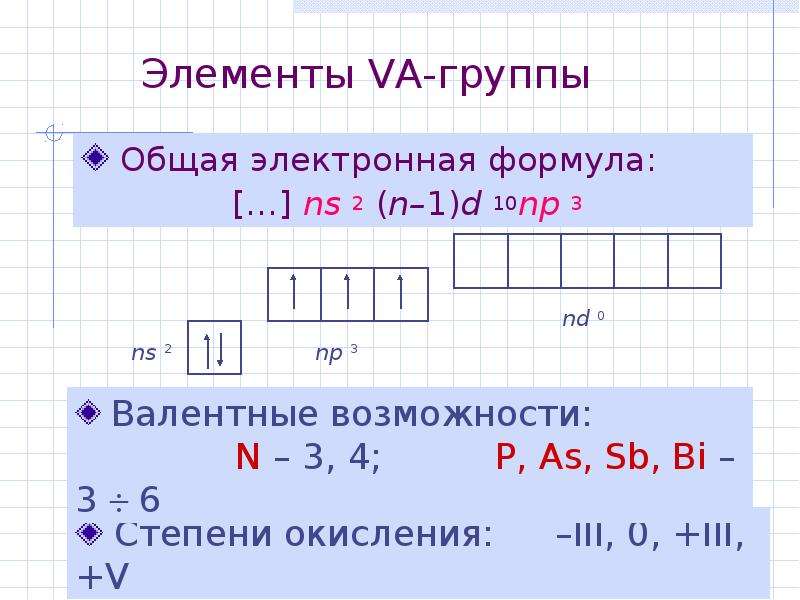
Содержание слайда: Элементы VА-группы
Общая электронная формула:
[…] ns 2 (n–1)d 10np 3
№4 слайд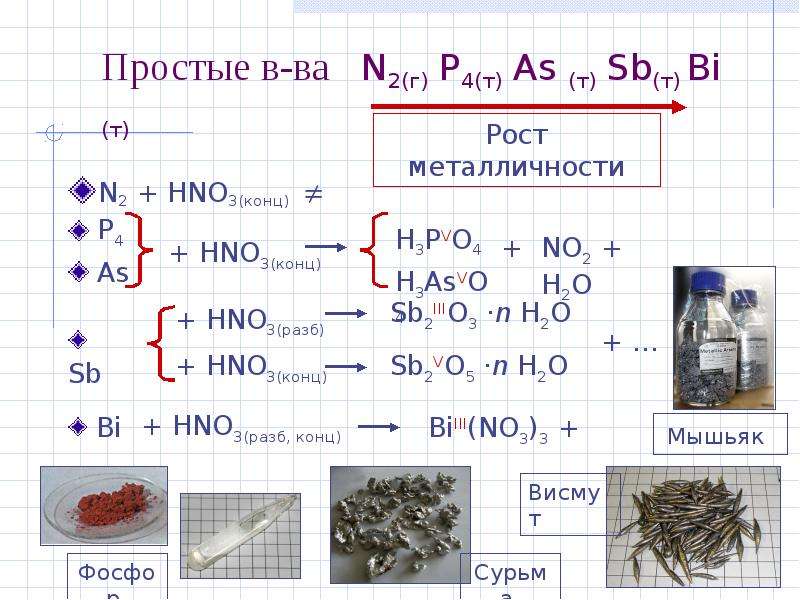
Содержание слайда: Простые в-ва N2(г) P4(т) As (т) Sb(т) Bi (т)
N2 + HNO3(конц)
№5 слайд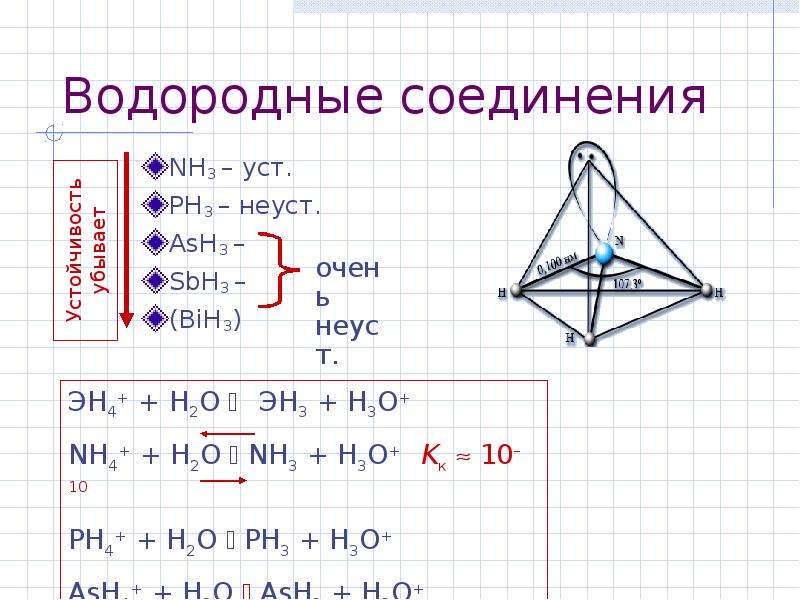
Содержание слайда: Водородные соединения
NH3 – уст.
PH3 – неуст.
AsH3 –
SbH3 –
(BiH3)
№6 слайд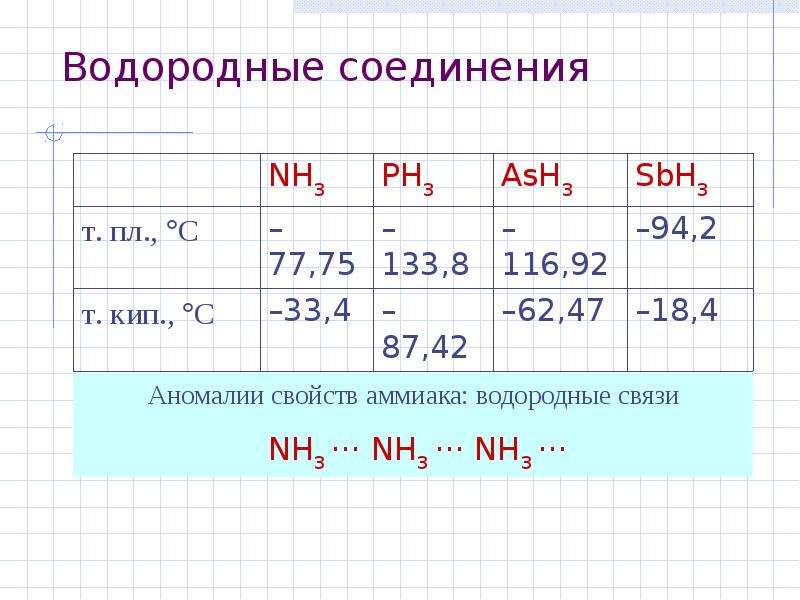
Содержание слайда: Водородные соединения
№7 слайд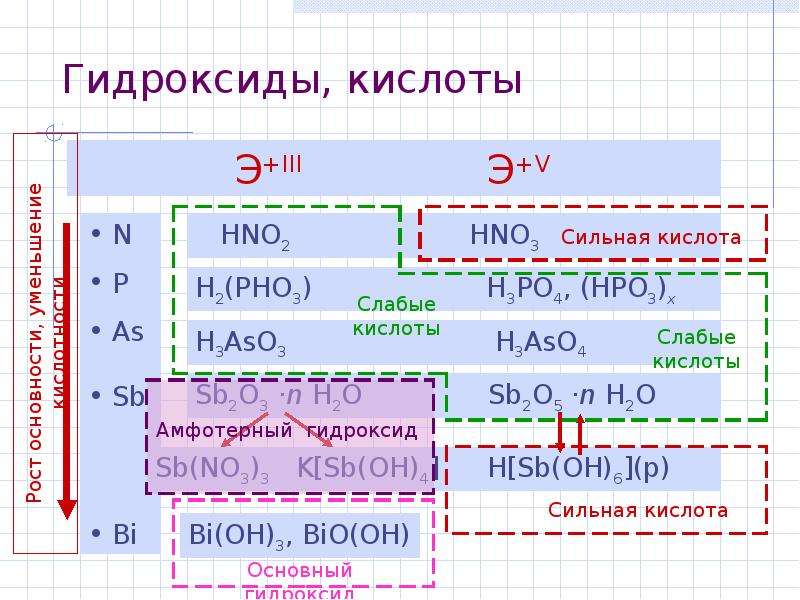
Содержание слайда: Гидроксиды, кислоты
№8 слайд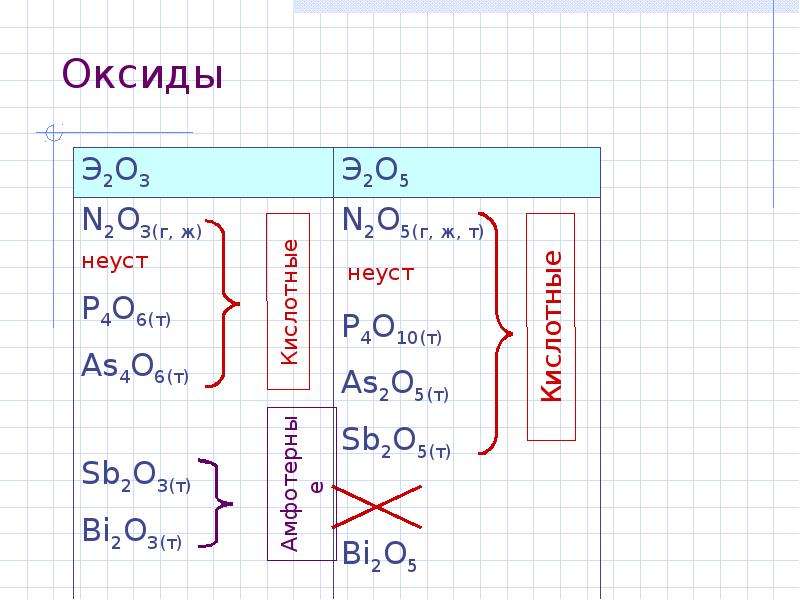
Содержание слайда: Оксиды
№9 слайд
Содержание слайда: Степени окисления
Ст.ок. +V: P, As, Sb
N(+V), Bi(+V) – сильные окислители
Ст.ок. +III: P, As, Sb, Bi
N(+III) – активный окислитель и восстановитель
Ст.ок. 0: N
№10 слайд
Содержание слайда: Распространение в природе
12. P – 0,09 масс.%
16. N – 0,03 масс.%
47. As – 5·10–4 масс.%
62. Sb – 5·10–5 масс.%
66. Bi – 1·10–5 масс.%
№11 слайд
Содержание слайда: Азот, фосфор
Нитратин (чилийская селитра) NaNO3
Нитрокалит (индийская селитра) KNO3
Нашатырь NH4Cl
№12 слайд
Содержание слайда: Мышьяк, сурьма, висмут
Реальгар As4S4
Аурипигмент As2S3
Арсенопирит FeAsS
Тетраэдрит Cul2As4S13
Антимонит (сурьмяный блеск) Sb2S3
Висмутин (висмутовый блеск) Bi2S3
№13 слайд
Содержание слайда: История открытия элементов
Азот: 1772 г., Д. Резерфорд, Г.Кавендиш, 1769-1771 гг., К.Шееле, А.Л. Лавуазье
Фосфор: 1669 г., Хённиг Бранд
Мышьяк: XIII в., Альберт Великий, XVI в., Парацельс, 1735 г., Г. Брандт
Сурьма: 3000 лет до н.э.; XVI в., Парацельс, Василий Валентин, 1735 г., Г. Брандт
Висмут: XV-XVI вв., Агрикола, Василий Валентин, 1739 г., И.Потт
№14 слайд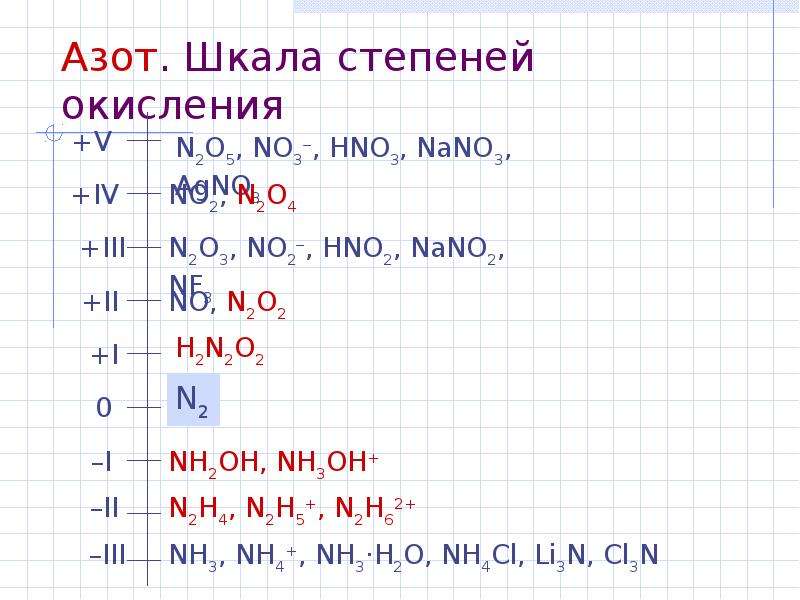
Содержание слайда: Азот. Шкала степеней окисления
№15 слайд
Содержание слайда: Свойства азота
N2 – бесцветный газ, без запаха и вкуса, т.пл. –210,0 С, т.кип. –195,8 С
малорастворим в воде и орг. р-рителях
энергия связи в молекуле N2 равна 945 кДж/моль, длина связи 110 пм.
№16 слайд
Содержание слайда: Получение и применение азота
В промышленности:
фракционная дистилляция сжиженного воздуха (жидкий кислород остается в жидкой фазе).
В лаборатории:
термич. разл. NH4NO2 (расплав, конц. водн. р-р):
NH4NO2 = N2 + 2H2O; NH4+ + NO2 = N2 + 2H2O
окисление аммиака (без катализатора):
4NH3 + 3O2 = 2N2 + 6H2O
Применение
Синтез аммиака (… азотная к-та, нитраты и т.д.)
Создание инертной атмосферы (металлургия и др.)
№17 слайд
Содержание слайда: Водородные соединения азота
№18 слайд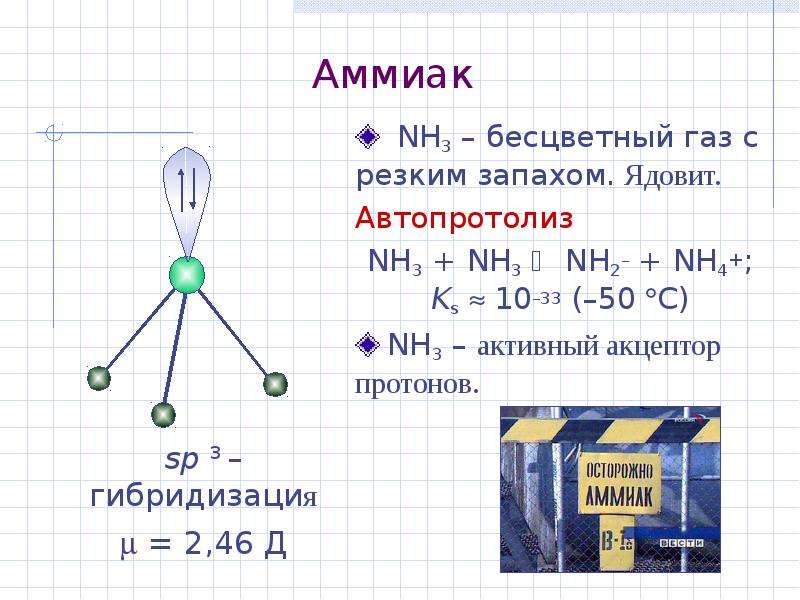
Содержание слайда: Аммиак
NH3 – бесцветный газ с резким запахом. Ядовит.
Автопротолиз
NH3 + NH3 NH2– + NH4+; Ks 10–33 (–50 С)
NH3 – активный акцептор протонов.
№19 слайд
Содержание слайда: Аммиак в водном растворе
Высокая растворимость в воде (в 1 л воды 700 л NH3)
Гидратация и протолиз:
NH3 + H2O = NH3·H2O
NH3 · H2O + H2O NH4+ + OH + H2O; pH 7
Kо = 1,75 · 10–5
№20 слайд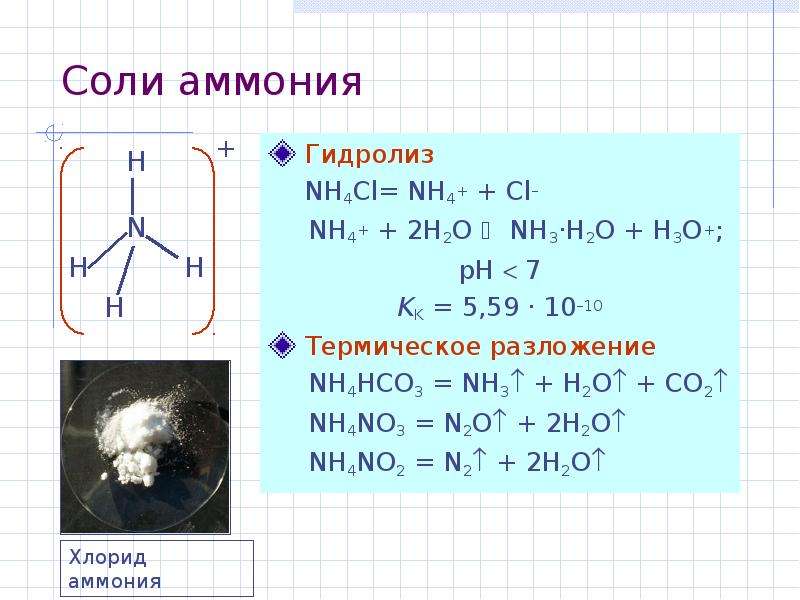
Содержание слайда: Соли аммония
Гидролиз
NH4Cl= NH4+ + Cl–
NH4+ + 2H2O NH3·H2O + H3O+;
pH 7
KK = 5,59 · 10–10
Термическое разложение
NH4HCO3 = NH3 + H2O + CO2
NH4NO3 = N2O + 2H2O
NH4NO2 = N2 + 2H2O
№21 слайд
Содержание слайда: Окислительно-восстановительные свойства
Горение
4 NH3 + 3O2 = 2N2 + 6H2O (без кат.)
4 NH3 + 5O2 = 4NO + 6H2O (кат. Pt, Cr2O3)
В водном растворе
pH 7: 2 NH3·H2O + 6OH 6e = N2 + 8H2O; = –0,74В
pH 7: 2NH4+ 6e = N2 + 8H+; = +0,27В
8 NH3·H2O 6e = N2 + 8H2O + 6NH4+; = +0,23В
Примеры:
8 NH3·H2O + 3Br2 = N2 + 8H2O + 6 NH4Br
2 NH3·H2O + 2KMnO4 = N2 + 2MnO2 + 4H2O + 2KOH
№22 слайд
Содержание слайда: Получение аммиака
В промышленности
N2 + 3H2 2NH3 + Q
(300-500 С, 300 атм, катализатор: Fe, Pt)
В лаборатории (при нагревании)
NH4Cl + NaOH =
= NaCl + H2O + NH3
NH3·H2O = H2O + NH3
№23 слайд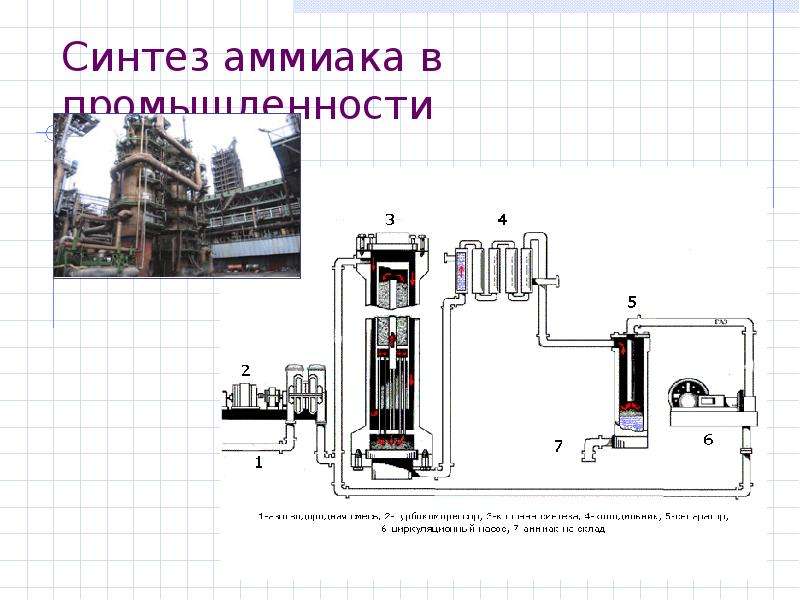
Содержание слайда: Синтез аммиака в промышленности
№24 слайд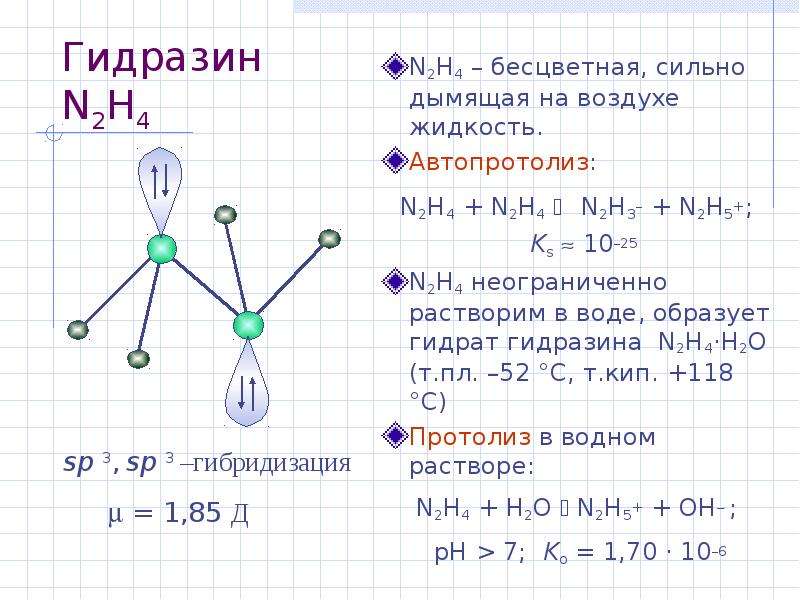
Содержание слайда: Гидразин N2H4
N2H4 – бесцветная, сильно дымящая на воздухе жидкость.
Автопротолиз:
N2H4 + N2H4 N2H3– + N2H5+;
Ks 10–25
N2H4 неограниченно растворим в воде, образует гидрат гидразина N2H4·H2O (т.пл. –52 °С, т.кип. +118 °С)
Протолиз в водном растворе:
N2H4 + H2O N2H5+ + OH ;
pH > 7; Kо = 1,70 · 10–6
№25 слайд
Содержание слайда: Протоноакцепторные свойства
N2H4 – акцептор протонов (две неподеленные пары электронов):
N2H4 + H3O+ = N2H5+ + H2O
катион гидразиния(1+)
N2H4 + 2H3O+ = N2H62+ + 2H2O
катион гидразиния(2+)
Соли: [N2H5]Cl, [N2H5]2SO4, [N2H6]SO4 (получ. в изб.к-ты)
№26 слайд
Содержание слайда: Окислительно-восстановительные свойства гидразина
Гидразин как восстановитель
рН 7: N2H4·H2O + 4OH 4e = N2 + 5H2O; = –1,12В
рН 7: N2H5+ 4e = N2 + 5H+; = –0,23 В
Гидразин как окислитель
рН 7: N2H4·H2O + 3H2O + 2e = 2 NH3·H2O + 2OH; = +0,03 В
рН 7: N2H5+ + 3H+ + 2e = 2NH4+; = +1,27 В
Восстановительные свойства гидразина ярче выражены в щелочной среде, а окислительные – в кислотной.
Пример: N2H4 + 2I2 = N2 + 4 HI (pH 7)
Получение: 2NH3 + NaClO = N2H4 + NaCl + H2O
№27 слайд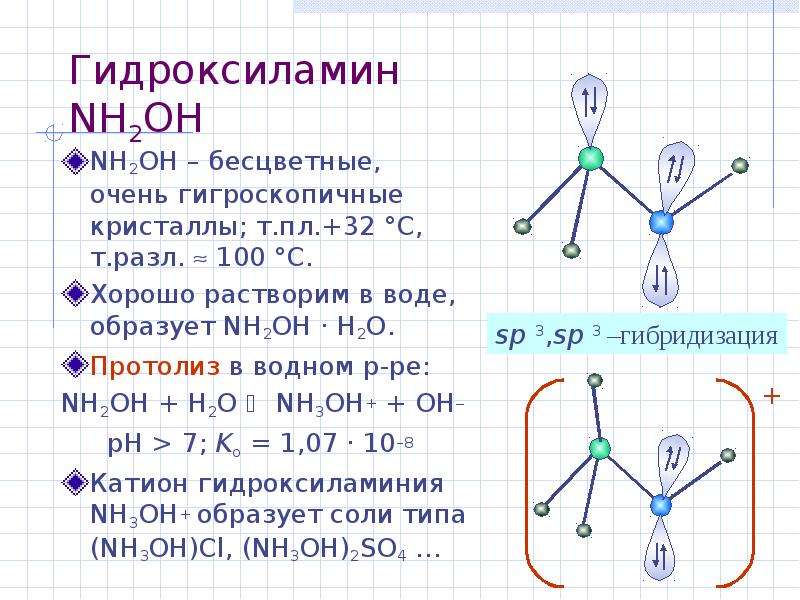
Содержание слайда: Гидроксиламин NH2OH
NH2OH – бесцветные, очень гигроскопичные кристаллы; т.пл.+32 °С, т.разл. 100 °С.
Хорошо растворим в воде, образует NH2OH · H2O.
Протолиз в водном р-ре:
NH2OH + H2O NH3OH+ + OH
pH > 7; Kо = 1,07 · 10–8
Катион гидроксиламиния NH3OH+ образует соли типа (NH3OH)Cl, (NH3OH)2SO4 …
№28 слайд
Содержание слайда: Окислительно-восстановительные свойства гидроксиламина
Гидроксиламин как восстановитель
рН 7: 2(NH2OH·H2O) + 2OH 2e = N2 + 6H2O;
= –3,04 В
рН 7: 2NH3OH+ 2e = N2 + 4H+ + 2H2O; = –1,87 В
Гидроксиламин как окислитель
рН 7: (NH2OH·H2O) + H2O +2e = NH3·H2O + 2OH; = +0,52 В
рН 7: NH3OH+ + 2H+ + 2e = NH4+ + H2O; = +1,35 В
Получение: пропускание смеси NO и H2 через суспензию катализатора (Pt) в разб. HCl
№29 слайд
Содержание слайда: Азидоводород HN3
HN3 – бесцветная летучая жидкость, неограниченно растворимая в воде (при содержании в растворе свыше 3% масс. – взрывоопасен).
Протолиз в водн. р-ре:
HN3 + H2O N3 + H3O+
рН 7; KK = 1,90 · 10–5
Азид-анион N3 имеет линейную форму.
Соли MN3 подвергаются гидролизу (рН 7).
Соли MN3 (M = Ag, Cu…) взрывоопасны (разл. на металл и N2).
№30 слайд
Содержание слайда: Окислительно-восстановительные свойства
Восстановительные свойства азидоводорода в растворе обусловлены легкостью превращения его в молекулярный азот:
2HN3 2e = 3N2 + 2H+; = –3,10 В
Азидоводород – окислитель по отношению к веществам с сильными восстановительными свойствами:
HN3 + 3HI = N2 + NH4I + I2







































