Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
20 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
2.92 MB
Просмотров:
47
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Азот и его соединения
Символ - N
Атомный вес - 14.0067
Плотность - 0.808 (при -195.8°C)
Температура плавления - -209.86 °C
Температура кипения - -195.82 °C
Открыт - Д. Резерфордом в 1772 г.
№2 слайд
Содержание слайда: Жидкий азот
Жидкий азот —не взрывоопасен и не ядовит.
№3 слайд
Содержание слайда: Применение жидкого азота
;
для охлаждения различного оборудования и техники;
для охлаждения компонентов компьютера при экстремальном разгоне
№4 слайд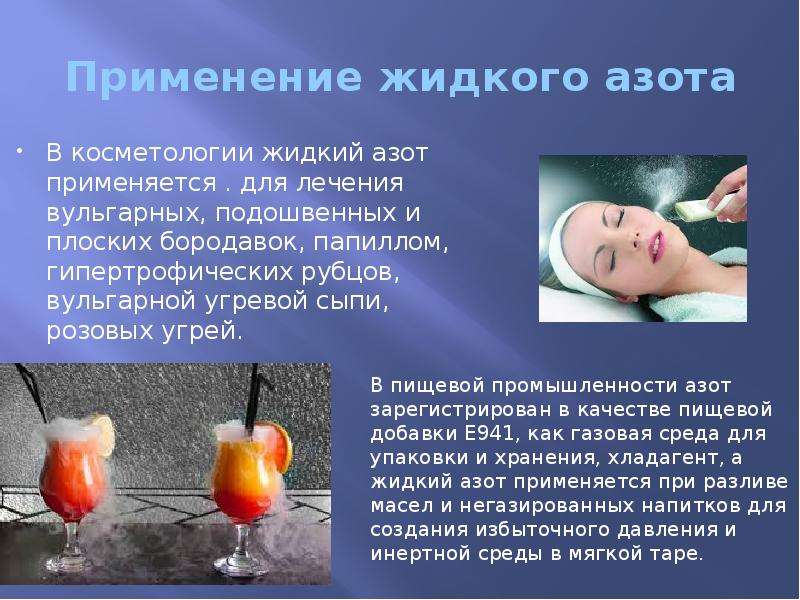
Содержание слайда: Применение жидкого азота
В косметологии жидкий азот применяется . для лечения вульгарных, подошвенных и плоских бородавок, папиллом, гипертрофических рубцов, вульгарной угревой сыпи, розовых угрей.
№5 слайд
Содержание слайда: Поведение веществ в жидком азоте
Вещества в жидком азоте становятся хрупкими
№6 слайд
Содержание слайда: Ожоги жидким азотом
Следует охладить поражённые участки тела водой или холодными предметами, ввести обезболивающие препараты, наложить на раны повязки из стерильных перевязочных средств или подручных материалов.
№7 слайд
Содержание слайда: Кессонная болезнь
Кессонная болезнь возникает при быстром снижении давления (например, при всплытии с глубины, выхода из кессона или барокамеры, или подъеме на высоту). При этом газ азот, ранее растворенный в крови или тканях, образует газовые пузырьки в кровеносных сосудах. Характерные симптомы включают боль или неврологические нарушения. Тяжелые случаи могут быть фатальными.
№8 слайд
Содержание слайда: Химические свойства азота
В химическом отношении азот довольно инертный газ из-за прочной ковалентной связи, атомарный же азот химически очень активен. Из металлов свободный азот реагирует в обычных условиях только с литием, образуя нитрид:
6Li + N2 = 2Li3N
С повышением температуры активность молекулярного азота увеличивается. При взаимодействии азота с водородом при нагревании, повышенном давлении и присутствии катализатора образуется аммиак:
N2 + 3H2 = 2NH3
С кислородом азот соединяется только в электрической дуге с образованием оксида азота (II):
N2 + O2 = 2NO
№9 слайд
Содержание слайда: Оксиды азота
№10 слайд
Содержание слайда: Азотная кислота
Температура кипения азотной кислоты +83 °С, температура замерзания –41 °С, т.е. при обычных условиях это жидкость. Резкий запах и то, что при хранении она желтеет, объясняется тем, что концентрированная кислота малоустойчива и под действием света или при нагревании частично разлагается.
4HNO3 = 2H2O + 4NO2 + O2.
№11 слайд
Содержание слайда: Взаимодействие с металлами
Концентрированная азотная кислота Me + HNO3(конц.) → соль + вода + NO2
С концентрированной азотной кислотой не взаимодействуют благородные металлы (Au, Ru, Os, Rh, Ir, Pt), а ряд металлов (Al, Ti, Cr, Fe, Co, Ni) при низкой температуре пассивируются концентрированной азотной кислотой. Реакция возможна при повышении температуры
Ag + 2HNO3(конц.) → AgNO3 + H2O + NO2↑.
№12 слайд
Содержание слайда: Взаимодействие с металлами
Разбавленная азотная кислота
Продукт восстановления азотной кислоты в разбавленном растворе зависит от активности металла, участвующего в реакции:
Активный металл
8Al + 30HNO3(разб.) → 8Al(NO3)3 + 9H2O + 3NH4NO3
Металл средней активности
10Cr + 36HNO3(разб.) → 10Cr(NO3)3 + 18H2O + 3N2
Металл малоактивный
3Ag + 4HNO3(разб.) → 3AgNO3 + 2H2O + NO
№13 слайд
Содержание слайда: Получение азотной кислоты
NaNO3 + H2SO4 = NaHSO4 + HNO3
№14 слайд
Содержание слайда: Применение азотной кислоты
Производство азотных и комплексных удобрений.
Производство взрывчатых веществ.
Производство красителей.
Производство лекарств.
Производство пленок, нитролаков, нитроэмалей.
Производство искусственных волокон.
Как компонент нитрующей смеси, для траления металлов в металлургии.
№15 слайд
Содержание слайда: Аммиак
.
№16 слайд
Содержание слайда: Аммиак - опасен
В медицине 10% водный раствор аммиака известен как нашатырный спирт. Резкий запах аммиака раздражает специфические рецепторы слизистой оболочки носа и способствует возбуждению дыхательного и сосудодвигательного центров, поэтому при обморочных состояниях или алкогольном отравлении пострадавшему дают вдыхать пары нашатырного
№17 слайд
Содержание слайда: Получение аммиака
лаборатории используют действие сильных щелочей на соли аммония:
NH4Cl + NaOH = NH3↑ + NaCl + H2O
(NH4)2SO4 + Ca(OH)2 = 2NH3↑ + CaSO4 + 2H2O
№18 слайд
Содержание слайда: Химические свойства аммиака
NH3 – сильный восстановитель.
1. Горение аммиака (при нагревании)
4NH3 + 3O2 → 2N2 + 6H20
2. Каталитическое окисление амииака (катализатор Pt – Rh, температура)
4NH3 + 5O2 → 4NO + 6H2O
№19 слайд
Содержание слайда: Взаимодействие аммиака с водой и кислотами
И водный раствор аммиака, и соли аммония содержат особый ион — катион аммония NH4, играющий роль катиона металла. Он получается в результате того, что атом азота имеет свободную (неподеленную) электронную пару, за счет которой и формируется еще одна ковалентная связь с катионом водорода, переходящего к аммиаку от молекул кислот или воды:
Такой механизм образования ковалентной связи, которая возникает не в результате обобществления непарных электронов, а благодаря свободной электронной паре, имеющейся у одного из атомов, называется донорно-акцепторным.
№20 слайд
Содержание слайда: Соли аммония
вступают в обменную реакцию с кислотами и солями:
(NH4)2SO4 + Ba(NO3)2 → BaSO4 ↓ + 2NH4NO3 (NH4)2CO3 + 2HCl → 2NH4Cl + Н2O + CO2 ↑ взаимодействуют с растворами щелочей с образованием аммиака – качественная реакция на ион аммония:
NH4Cl + NaOH → NaCl + NH3 ↑ + Н2O
разлагаются при нагревании NH4Cl → NH3↑ + HCl