Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
15 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
1.94 MB
Просмотров:
59
Скачиваний:
1
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: «Магний»
Выполнил:
Искаков Чингиз
№2 слайд
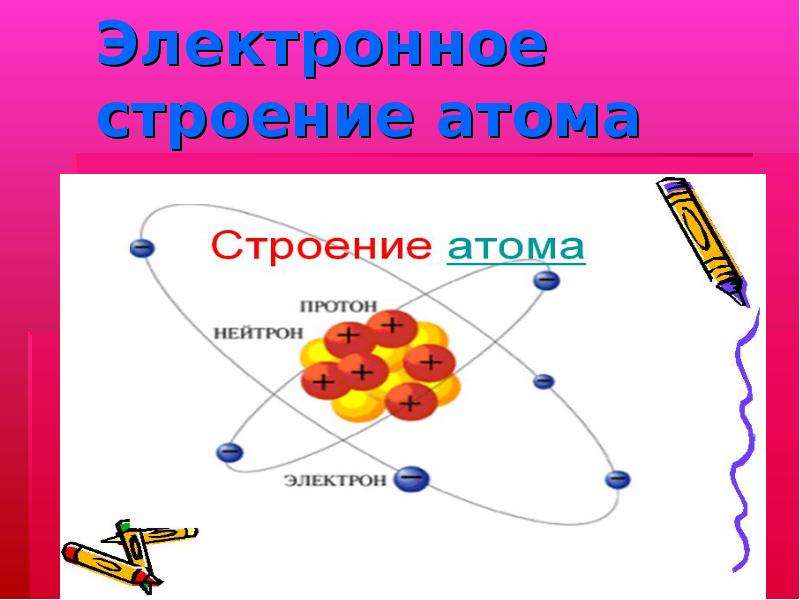
Содержание слайда: Электронное строение атома Mg
№3 слайд
Содержание слайда: Строение простого вещества
№4 слайд
Содержание слайда: Физические свойства Mg
№5 слайд
Содержание слайда: Химические свойства Mg
№6 слайд
Содержание слайда: Горение Mg в кислороде
2Mg + O2 = 2MgO
№7 слайд
Содержание слайда: Горение Mg в воде
Что будет, если тушить магний водой?
На заводе по переработке вторичного сырья в Уолтон Хиллс, штат Огайо возник пожар. В здании было большое количество металлов, среди них титан, сталь и магний. Пожарные, опасаясь, что огонь перекинется на соседнюю бензозаправку решили залить горящее здание водой. Результат не заставил себя ждать - произошел сильный взрыв, во все стороны разлетелись куски раскаленного добела магния. Ослепительный огонь поднялся на высоту 50 м. Однако пожарных это ни чему не научило - они продолжили заливать здание, что вызвало новые взрывы магния. Пожарные вынуждены были отступать под дождем горящего магния. От жара огня начали плавиться стены здания. Единственный способ погасить пожар магния - засыпать металл большим количеством песка, что было в данном случае технически невозможно, но это не повод заливать горящий магний водой. Некомпетентные действия пожарных значительно усугубили масштаб аварии.
Mg + 2H2O = Mg(OH)2 + H2
№8 слайд
Содержание слайда: Горение Mg в хлоре
Mg + Cl2 = MgCl2
№9 слайд
Содержание слайда: Вспышка смеси Mg + AgNO3 от капли воды
№10 слайд
Содержание слайда: «Горение магния на воздухе»
2Mg + O2 = 2MgO
№11 слайд
Содержание слайда: Магнийтермия
Магнийтермия – получение металлов восстановлением оксидов металлов магнием, которое сопровождается выделением значительного количества теплоты.
4Mg+ Fe3O4 = 4MgO + 3Fe
3Mg + Al2O3 = 3MgO + 2Al
№12 слайд
Содержание слайда: Нахождение Mg в земной коре
№13 слайд
Содержание слайда: Получение Mg
№14 слайд
Содержание слайда: Применение Mg и его сплавов
№15 слайд
Содержание слайда: Выводы
Магний – химический элемент II группы ПСХЭ Д.И. Менделеева, в химическом отношении – весьма активный металл, соединения магния имеют основной характер. Магний – характерный элемент мантии Земли, минералы магния многочисленны. Более половины из них образовались в биосфере – на дне морей, озер, в почвах. В промышленности наибольшее количество магния получают электролизом расплава хлорида магния. Широко применяются сплавы магния в промышленности. Магний – постоянная часть растительных и животных организмов. Из препаратов магния в медицинской практике применяют: сульфат магния (как успокаивающее, противосудорожное, спазмолитическое, слабительное и желчегонное средство), магнезию жженую (магния оксид) и карбонат магния (легкое слабительное).