Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
10 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
237.50 kB
Просмотров:
53
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Составление электронных формул и электронно-графических схем строения атома
Разработал:
Лебедев
Сергей Николаевич
учитель химии высшей категории
ГОУ школа-интернат V-VI вида. г. Кострома.
Дополнено:
Можаев Г.М. kontren.narod.ru
№2 слайд
Содержание слайда: Составление электронных формул и электронно-графических схем строения атома
научимся составлять электронные и электронно-графические схемы строения атома
№3 слайд
Содержание слайда: 1. Запиши знак химического элемента.
Перед ним внизу укажи его порядковый номер.
Порядковый номер химического элемента показывает, сколько электронов в атоме.
У атома хрома 24 электрона.
№4 слайд
Содержание слайда: 2. По образцу составь электронную формулу.
Порядок заполнения энергетических уровней в атоме.
1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4р6 …
№5 слайд
Содержание слайда: Определи: По порядку ли идут энергетические уровни.
Если уровни идут по порядку, то так их и оставь.
Если уровни идут не по порядку, то перепиши их, расставив по мере возрастания.
Нет. 4s и 3d подуровни идут не по порядку.
Надо переписать и расставить их по мере возрастания.
№6 слайд
Содержание слайда: «Провал электрона»
Если d- подуровень близок к полному заполнению:
(d9 – не хватает одного электрона до d10),
или к заполнению наполовину:
(d4 – не хватает одного электрона до d5)
на него часто «проваливается» электрон
с s – подуровня.
Исправляем
№7 слайд
Содержание слайда: Правила для составления электронно-графической схемы
Каждый подуровень имеет определенное число орбиталей
На каждой орбитали могут находиться не более двух электронов
Если на орбитали два электрона, то у них должен быть разный спин.
№8 слайд
Содержание слайда: 3. Составь электронно-графическую схему
№9 слайд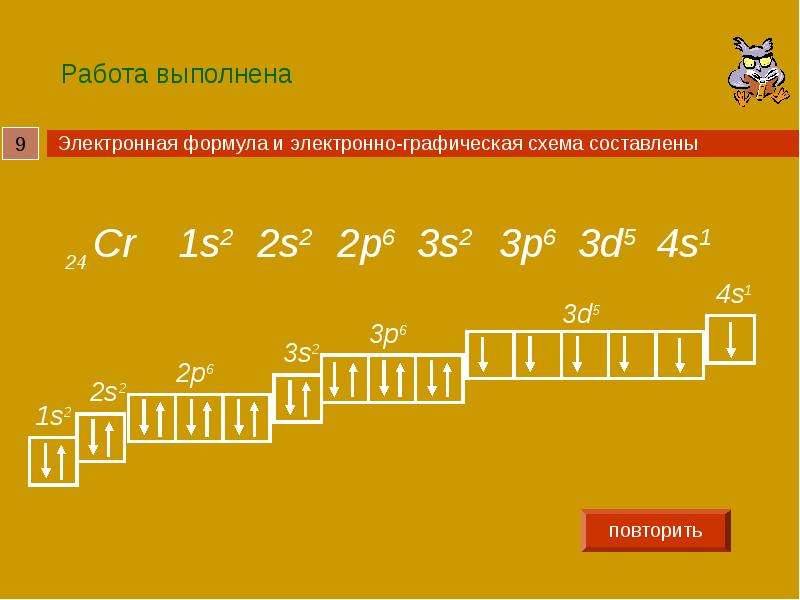
Содержание слайда: Работа выполнена
№10 слайд
Содержание слайда: Дополнительная информация
Последовательность заполнения подуровней:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 6s2 4f14 5d10 6p6 7s2 5f14 6d10 7p6 …
Орбитали можно показывать не только клеточками, но и линиями.
В атомах элементов V-VII периодов могут встретиться и другие случаи «провала» электронов, не подчиняющиеся простым правилам. Составленные формулы надо проверять по справочным данным
При возбуждении атома его внешние электроны могут распариваться и переходить на ближайшие свободные подуровни.