Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
23 слайда
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
221.88 kB
Просмотров:
85
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Лекция №4
Тема: «Алкины»
План:
1. Общая характеристика,гомологический ряд,номенклатура ,изомерия.
2. Методы синтеза алкенов.
3. Физические свойства
4. Химические свойства:
а) реакции присоединения;
б) реакции замещения;
в)реакции окисления;
в) реакции полимеризации;
5.Отдельные представители алкинов.
№2 слайд
Содержание слайда: 1. Общая характеристика,гомологический ряд,номенклатура ,изомерия.
№3 слайд
№4 слайд
Содержание слайда: Гомологический ряд
№5 слайд
Содержание слайда: Номенклатура
Систематическая (международная) номенклатура:
а) выбираем длинную цепочку с тройной связью;
б) нумеруем цепочку с той стороны, где ближе тройная связь;
в) называем радикалы;
г) называем цепочку, окончание – ан меняем на –ин;
д) в конце цифрой указываем место тройной связи.
1 2 3 4 5
СН3- С ≡ С – СН - СН3
СН3
4 –метилпентин - 2
№6 слайд
Содержание слайда: 2. Рациональная номенклатура:
а) выбираем 2 центральных атома, соединённых тройной связью;
б) отсекаем все связи, отходящие от тройной связи;
в) называем радикалы от младшего к старшему;
г) к названию радикалов добавляем слово «ацетилен».
СН3- С ≡ С – СН - СН3
СН3
метилизопропилацетилен
№7 слайд
Содержание слайда: Изомерия
Алкинам свойственна изомерия углеродного
скелета (начиная с C5H8), изомерия положения тройной связи (начиная с C4H6) и межклассовая изомерия с алкадиенами.
Изомерия положения тройной связи :
1 2 3 4
СН ≡С - СН2 - СН3 бутин - 1
1 2 3 4
СН3 - С ≡ С - СН3 бутин - 2
№8 слайд
Содержание слайда: 2. Методы синтеза алкенов.
1.Разложением водой карбида кальция СаС2,который получают спеканием негашеной извести СаО с коксом:
СаО + 3C 2500°C CaC2 + CO
СаС2 + 2Н2O → НС ≡ СН + Са(ОН)2
№9 слайд
Содержание слайда: Н Сl 2NaOH спирт.р-р
Н Сl 2NaOH спирт.р-р
СН –СН + СН ≡ СН + 2NaСl + 2Н2О
Сl Н
1,2 - дихлорэтан
3. Дегидрирование алканов :
2СН4 С2Н2 + 3Н2
№10 слайд
Содержание слайда: 3. Физические свойства алканов
Ацетиленовые углеводороды, содержащие в молекуле от двух до четырех углеродных атомов (при обычных условиях), — газы,
начиная с C5H8 — жидкости,
а высшие алкины (с С16Н30 и выше) — твердые вещества.
№11 слайд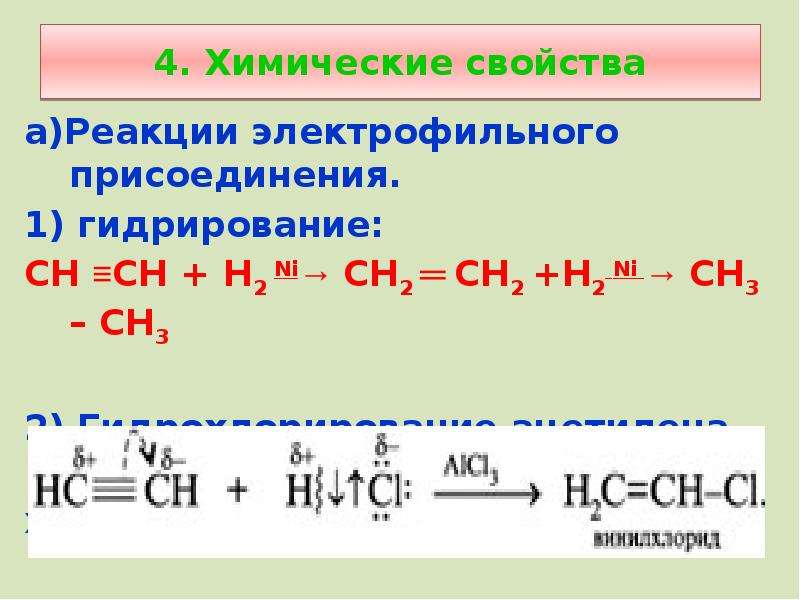
Содержание слайда: 4. Химические свойства
а)Реакции электрофильного присоединения.
1) гидрирование:
СН ≡СН + Н2 Ni→ СН2 ═ СН2 +Н2 Ni → СН3 – СН3
2) Гидрохлорирование ацетилена дает винил-
хлорид:
№12 слайд
№13 слайд
№14 слайд
№15 слайд
Содержание слайда: б). Реакции замещения
Особенностью алкинов, явл. их способность отще-
плять протон по действием сильных оснований,
т.е. проявлять слабые кислотные свойства.
Возможность отщепления протона обусловлена
сильной поляризацией σ- связи =С←Н. Причиной
поляризации явл. высокая электроотрицательность
атома С в состоянии sp –гибридизации. Алкины в
отличии от алкенов способны обр. соли - ацетилениды
+2[Ag(NН3)2]ОН
НС ≡ СН AgС=СAg↓ + 4NН3 ↑+ 2Н2О
желто-серый, ацетиленид серебра
№16 слайд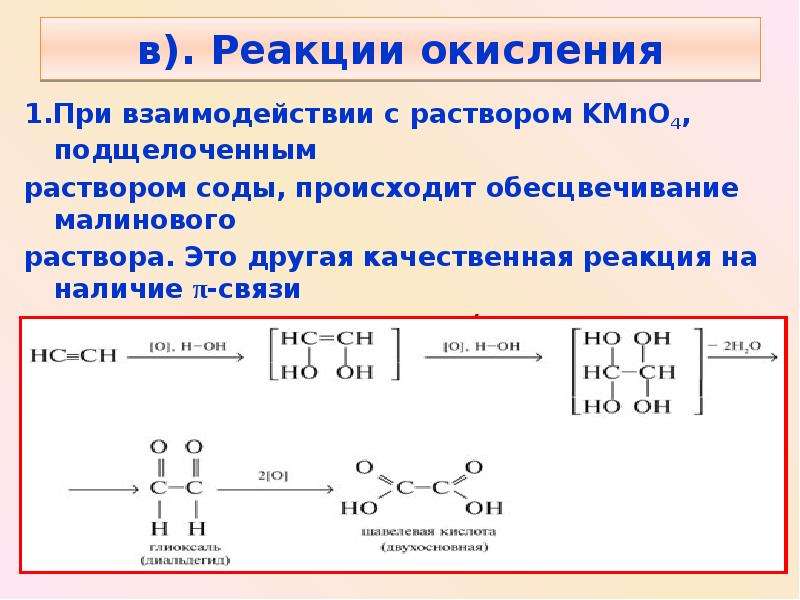
Содержание слайда: в). Реакции окисления
1.При взаимодействии с раствором KMnО4, подщелоченным
раствором соды, происходит обесцвечивание малинового
раствора. Это другая качественная реакция на наличие π-связи
в органическом соединении (реакция Е.Е.Вагнера).
В кислой среде происходит окисление ацетилена до щавелевой
кислоты:
№17 слайд
Содержание слайда: 2. Окисление алкинов в более жёстких условиях:
1)СН ≡ СН + 2KMnО4 + 3Н2SО4 2СО2 + Н2О +
К2SО4 +2MnSО4
[о]
2)СН3-С ≡ С - СН3 2СН3-СООН + К2SО4+Н2О +
бутин-2
MnSО4
№18 слайд
Содержание слайда: г). Реакции полимеризации
Как и алкены, алкины вступают в реакцию
полимеризации. Полимеризация этина и его гомо-
логов в зависимости от применяемого катализато-
ра проходит по-разному.
Димеризация:
№19 слайд
№20 слайд
№21 слайд
Содержание слайда: 5. Отдельные представители алкинов
Наибольшее практическое значение имеют ацетилен
H–C ≡ C–H и винилацетилен CH2= CH–C ≡ CH.
Ацетилен (С2Н2) – бесцветный газ, без запаха, об-
ладает слабым наркотическим свойством, мало
растворим в воде ,хорошо в ацетоне. Смеси ацетиле-
на с воздухом взрывоопасны. При горении ацетиле-
на в кислороде выделяется большое количество теп-
ла и температура пламени достигает 30000С. На этом
основано применение ацетилена для резки и сварки
металлов. Ацетилен является исходным сырьем для
производства уксусной кислоты, синтетических
каучуков.
№22 слайд
№23 слайд
































