Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
20 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
1.50 MB
Просмотров:
151
Скачиваний:
2
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Химия элементов. Лекция 7
Общая характеристика элементов IIБ-группы. Цинк и кадмий. Ртуть
№2 слайд
Содержание слайда: d-элементы:
[…] ns12(n–2)f 14(n–1)d 010np0
Многообразие степеней окисления (от 0 до +VIII), склонность к ОВР.
Низшие ст. ок. – основные св-ва, высшие – кислотные.
Металличность: не образуются одноатомные анионы Эх–, характерны одноатомные катионы Эх+.
Простые вещества тяжелые, плотные, тугоплавкие металлы; в ЭХРН – в основном до водорода.
Комплексообразователи и катализаторы (есть незаселенные d-орбитали)
Отличия свойств элемента 4 периода, сходство свойств элем. 5 и 6 периода (причина – лантаноидное сжатие).
№3 слайд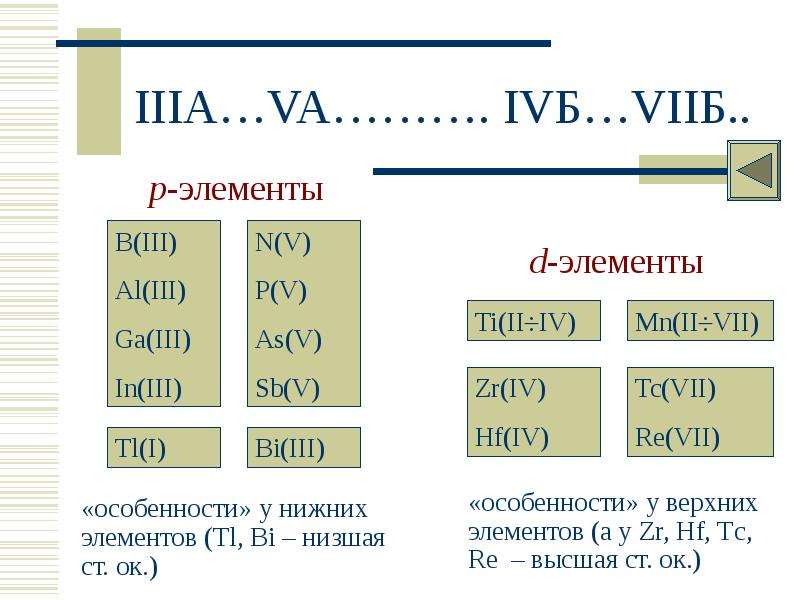
Содержание слайда: IIIA…VA………. IVБ…VIIБ..
№4 слайд
Содержание слайда: Элементы IIБ-группы
№5 слайд
Содержание слайда: Элементы IIБ-группы
Общая электронная формула: […] ns2 (n–1)d10
№6 слайд
Содержание слайда: Простые вещества
№7 слайд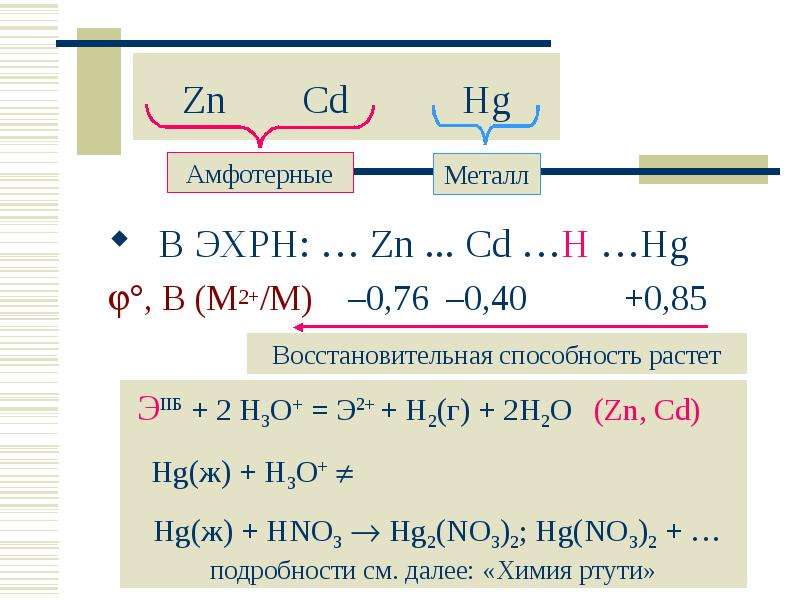
Содержание слайда: Zn Cd Hg
В ЭХРН: … Zn ... Cd …H …Hg
, В (M2+/M) –0,76 –0,40 +0,85
№8 слайд
Содержание слайда: Кислородные соединения
ZnO CdO HgO
№9 слайд
Содержание слайда: Комплексные соединения
ЭIIБ КЧ Тип гибр. Примеры
№10 слайд
Содержание слайда: Комплексные соединения
[ZnI4]2– [CdI4]2– [HgI4]2–
(обр.) 4 · 10–3 1 · 106 5,6 · 1029
№11 слайд
Содержание слайда: Распространение в природе и важнейшие минералы
В земной коре по массе
25. Zn 0,012 %
63. Hg 5·10–4 %
64. Cd 1·10–4 %
№12 слайд
Содержание слайда: Цинк и кадмий
№13 слайд
Содержание слайда: Цинк и кадмий
Zn + 2 H3O+ + 2H2O = [Zn+II(H2O)4]+ + H2
= – 0,76 В
Zn + 2 OH + 2H2O = [Zn+II(OH)4] + H2
= – 1,2 В
Cd + 2 OH (разб.)
№14 слайд
Содержание слайда: Восстановительные свойства
4Zn + KNO3 + 7KOH + 6H2O =
= 4K2[Zn(OH)4] + NH3
Zn + 4 OH – 2e– = [Zn(OH)4]2–
NO3– + 6 H2O + 8e– = NH3 + 9 OH
Zn + KNO3 + H2SO4 =
= ZnSO4 + KNO2 + H2O
Zn – 2e– = Zn2+
NO3– + 2H+ + 2e– = NO2– + H2O
№15 слайд
Содержание слайда: Комплексообразование
Zn(OH)2 + 4 NH3.H2O =
= [Zn(NH3)4](OH)2 + 4H2O (КЧ 4)
Cd(OH)2 + 6 NH3.H2O =
= [Cd(NH3)6](OH)2 + 6H2O (КЧ 6)
Только цинк:
Zn + 4 NH3.H2O =
= [Zn(NH3)4]+ + H2 + 2 OH + 2H2O
[Zn(NH3)4]+/ Zn = –1,03 В
№16 слайд
Содержание слайда: Особенности химии ртути
Hg(ж) – летуча, ядовита
CH3Hg+ – самый сильный яд
Hg образует амальгамы (например NaxHgy)
2NaHg + 2H2O = 2Hg + 2NaOH + H2
№17 слайд
Содержание слайда: Hg + HNO3
Hg + 4HNO3(конц., изб.) =
= Hg(NO3)2 + 2NO2 + 2H2O;
(Hg2+/Hg) = + 0,85 В
6Hg(изб.) + 8HNO3(разб.) =
= 3Hg2(NO3)2 + 2NO + 4H2O;
(Hg22+/Hgж) = + 0,79 В
Hg2+I(NO3)2 + 4HNO3(конц.) =
= 2Hg+II(NO3)2 + 2NO2 + 2H2O
(Hg2+/Hg22+) = + 0,92 В
№18 слайд
Содержание слайда: Hg22+ Hg0 + Hg2+
[(H2O)Hg–Hg(H2O)]2+
Hg2(NO3)2 =
= Hg22+ + 2NO3
Каломель Hg2Cl2
Hg2Cl2(т)
Hg22+ + 2Cl–;
ПР = 1,3·10–18
Все соединения – – ионные кристаллы
№19 слайд
Содержание слайда: Hg22+ и Hg2+
Hg22+ + 2OH =
= HgO + Hg + H2O
Hg22+ + 2e– = 2Hg
Hg22+ + 4OH – 2e– =
= 2HgO + 2H2O
Hg22+ + H2S =
= HgS + Hg + 2H+
Hg22+ + 2e– = 2Hg
Hg22+ + 2H2S – 2e– =
= 2HgS + 4H+
№20 слайд
Содержание слайда: Окислительно-восстановительные свойства
Hg(NO3)2 + 2HCl = HgCl2(р) + 2H2O
2HgCl2 + [SnCl3] + Cl = Hg2Cl2(т)+ [SnCl6]2
2HgCl2 + 2e– = Hg2Cl2(т) + 2Cl (белый осадок)
[SnCl3] + 3Cl – 2e– = [SnCl6]2
Hg2Cl2 + [SnCl3] + Cl = 2Hg + [SnCl6]2
Hg2Cl2(т) + 2e– = 2Hg(ж) + 2Cl (черный осадок)
[SnCl3] + 3Cl – 2e– = [SnCl6]2
(HgCl2/ Hg2Cl2 ) = +0,66 В
(Hg2Cl2 /Hgж) = +0,27 В





























