Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
27 слайдов
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
2.68 MB
Просмотров:
141
Скачиваний:
0
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Химия элементов. Лекция 11
Общая характеристика элементов VIБ-группы. Хром
№2 слайд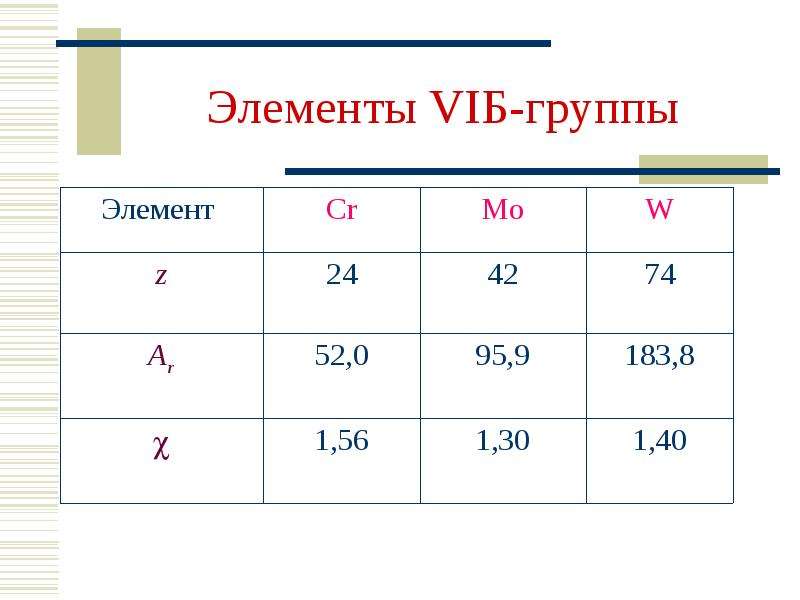
Содержание слайда: Элементы VIБ-группы
№3 слайд
Содержание слайда: Электронное строение
Cr: […] 4s1 3d 5 4p0
Mo: […] 5s1 4d 55p0
W: […] 6s 2 4f 145d 46p0
№4 слайд
Содержание слайда: Простые вещества
№5 слайд
Содержание слайда: Простые вещества
№6 слайд
Содержание слайда: Простые вещества
Кислоты-окислители (пассивация на холоду): ЭVIБ + HNO3(конц), H2SO4(конц)
Э (Mo,W) + 2HNO3 + 8HF =
= Н2[ЭVIF8] + 2NO + 4H2O
Э + 8HF – 6e– = [ЭF8]2– + 2H+
NO3 – + 4H+ + 3e– = NO + 2H2O
Э (Cr,Mo,W) + 3NaNO3 + 2NaOH =
= Na2ЭVIO4 + 3NaNO2 + H2O
Cr + NaOH (р)
№7 слайд
Содержание слайда: Металлы
№8 слайд
Содержание слайда: Кислородные соединения
Cr Mo, W
+ II: CrO – черн., т.разл. 700 C (до Cr2O3 и Cr); Cr(OH)2 – желт. (основный)
+III: Cr2O3 – зел. уст.; Cr(OH)3 – серо-гол.; CrO(OH) – зел. (амфотерн.)
+IV: CrO2 черн., т.разл. 450 C (до Cr2O3 и O2)
+VI: CrO3 – красн., т.разл. 220 C (до Cr2O3 и O2); H2CrO4 и H2Cr2O7 (желт. и оранж. р-р, до 75% масс.)
№9 слайд
Содержание слайда: Э+VI: CrO3 MoO3 WO3
т. пл., °С: 197 795 1473
№10 слайд
Содержание слайда: Комплексные соединения
Ст. ок. 0: [Э0(CO)6]
[Cr0(CO)6] – гексакарбонилхром: диамагнитный
№11 слайд
Содержание слайда: Комплексные соединения CrIII
[Cr(H2O)4Cl2]Cl · 2H2O
зеленый
№12 слайд
Содержание слайда: Изополисоединения (ст.ок. +VI)
2CrO42 + 2H3O+ Cr2O72 + 3H2O; KcI 1014
3Cr2O72 + 2H3O+ 2Cr3O102 + 3H2O
………….
Cr2O72 + 2OH– 2CrO42 + H2O; KcIII 1014
№13 слайд
Содержание слайда: Изополисоединения
№14 слайд
Содержание слайда: Пероксокомплексы
Cr2O72 + 4H2O2 + 2H3O+ + L =
= 2[CrVI(L)O(O22)2] + 7H2O
голубого цвета
(экстракция органическим р-рителем)
№15 слайд
Содержание слайда: Распространение в природе и важнейшие минералы
21. Cr 0,019% масс.
39. Mo 1·10–3%
27. W 7·10–3%
№16 слайд
Содержание слайда: Минералы
гюбнерит MnWO4
повеллит CaMoO4
молибдошеелит Ca(W,Mo)O4
ферберит FeWO4
№17 слайд
Содержание слайда: Получение
Cr2O3 + 2Al = 2Cr + Al2O3 (t°)
(Cr2IIIFeII)O4 + 4C = Fe + 2Cr + 4CO
феррохром
WO3 + 3H2 = W + 3H2O (t°)
MoO3 + 3H2 = Mo + 3H2O (t°)
№18 слайд
Содержание слайда: Химия хрома. Cr(II)
Cr(OH)2 – основный гидроксид, восстановитель
CrII(OH)2(т) + O2 Cr2IIIO3 · nH2O(т)
Cr(OH)2(т) + 2H3O+ + 2H2O = [CrII(H2O)6]2+
желтый (HClO4) голубой
CrII(OH)2(т) + 2HCl + 2H2O =
= [CrII(H2O)4Cl2](р)
№19 слайд
Содержание слайда: Аквакатион хрома(II)
Сильнейший восст-ль: (Cr3+/Cr2+) = –0,41 В
4[CrII(H2O)6]2+ + O2 + 4H3O+ =
= 4[CrIII(H2O)6]3+ + 6H2O
2[CrII(H2O)4Cl2] + [SnIICl3]– =
= 2[CrIII(H2O)4Cl2]+ + Sn0 + 3Cl–
Стабилизация степени окисления +II:
2[CrII(H2O)4Cl2] + 4CH3COO– =
= [Cr2II(H2O)2(CH3COO)4] + 4Cl– + 6H2O
красного цвета, устойч.
№20 слайд
Содержание слайда: Устойчивый кластерный комплекс хрома(II)
, -связи
диамагнитный комплекс тетраацетатодиаквадихром
№21 слайд
Содержание слайда: Оксид хрома(III) Cr2O3
Cr2O3 - пигмент (зелен.), амфотерн., уст. в ОВР
Получение:
(NH4)2Cr2O7 = Cr2O3 + N2 + 4H2O
Cr2O3 + H2O, H3O+, OH–
Сплавление:
Cr2O3 + 2NaOH = 2NaCrO2 + H2O
Cr2O3 + 3Na2S2O7 = Cr2(SO4)3 + 3Na2SO4
№22 слайд
Содержание слайда: [Cr(H2O)6]3+ + 3NH3·H2O Cr2O3·nH2O(т) + …
серо-зеленый гель
[Cr(H2O)6]3+ + H2O [Cr(H2O)5OH]2+ + H3O+;
KK = 1,12 · 10–4
2[Cr(H2O)5OH]2+ [(H2O)5Cr(OH)2Cr(H2O)5]4+
№23 слайд
Содержание слайда: Cr(VI)
H2CrO4 + H2O = HCrO4 + H3O+
(H2CrO4 – сильная к-та)
HCrO4– + H2O CrO42 + H3O+; pH > 6
KK = 3,2·10–7
2HCrO4– Cr2O72 + H2O; pH 26; Kc 1,6·102
Cr2O72 + 2 OH 2CrO42 + H2O; KcIII 1014
pH < 7 pH > 7
№24 слайд
Содержание слайда: Окислительно-восстановительные свойства
рН < 7:
Cr2O72 + 14H3O+ + 6e = 2[Cr(H2O)6]3+ + 9H2O;
= +1,33 В
рН > 7:
CrO42 + 4H2O + 3e = [Cr(OH)6]3 + 2 OH;
= – 0,16 В
Окислительные свойства сильнее выражены в кислотной среде
№25 слайд
Содержание слайда: Cr(VI) Cr(III) Cr(II)
K2Cr2O7(т) + 14 HCl(конц.) + H2O =
= 2[CrIII(H2O)4Cl2]Cl(р) + 3Cl2 + 2KCl
зеленый
Zn + 2HCl = ZnCl2 + H2
2[CrIII(H2O)4Cl2]Cl(р) + Zn =
= 2[CrII(H2O)4Cl2](р) + ZnCl2
голубого цвета
№26 слайд
Содержание слайда: Разложение дихромата аммония
(NH4)2Cr2O7 = Cr2O3 + N2 + 4H2O
№27 слайд
Содержание слайда: Cr(VI)
CrO3(т) + 2HCl(г) = CrCl2O2(ж) + H2O(г); +t°
диоксид-дихлорид хрома (бинарное соединение)
Получение:
K2Cr2O7 + NaCl + H2SO4(конц.) CrCl2O2 + …
Гидролиз: CrCl2O2 + 2H2O = H2CrO4 + 2HCl
недост. H2O: H2CrO4
изб. H2O, рН 26: 2HCrO4–, Cr2O72–
[CrO3(OH)]– + Cl– + H3O+ [CrO3Cl]– + 2H2O




































