Оцените презентацию от 1 до 5 баллов!
Тип файла:
ppt / pptx (powerpoint)
Всего слайдов:
21 слайд
Для класса:
1,2,3,4,5,6,7,8,9,10,11
Размер файла:
1.65 MB
Просмотров:
148
Скачиваний:
1
Автор:
неизвестен
Слайды и текст к этой презентации:
№1 слайд
Содержание слайда: Химия элементов. Лекция 6
Комплексные соединения: типы и классификация. Методы получения и разрушения. Решение задач.
№2 слайд
Содержание слайда: Типы комплексных соединений.
1. Аквакомплексы
В водных растворах:
[Be(H2O)4]2+
[Al(H2O)6]3+
[Cr(H2O)6]3+ …
Кристаллогидраты:
[Be(H2O)4]SO4
[Al(H2O)6]Cl3
[K(H2O)6][Cr(H2O)6](SO4)2
[Cu(H2O)4]SO4·H2O
[Ni(H2O)6]SO4·H2O
№3 слайд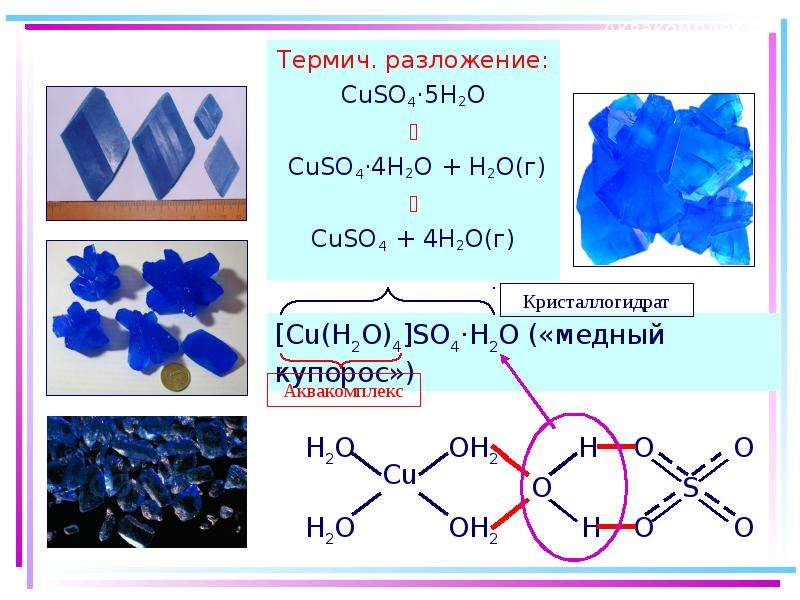
Содержание слайда: Аквакомплексы
Термич. разложение:
CuSO4·5H2O
CuSO4·4H2O + H2O(г)
CuSO4 + 4H2O(г)
№4 слайд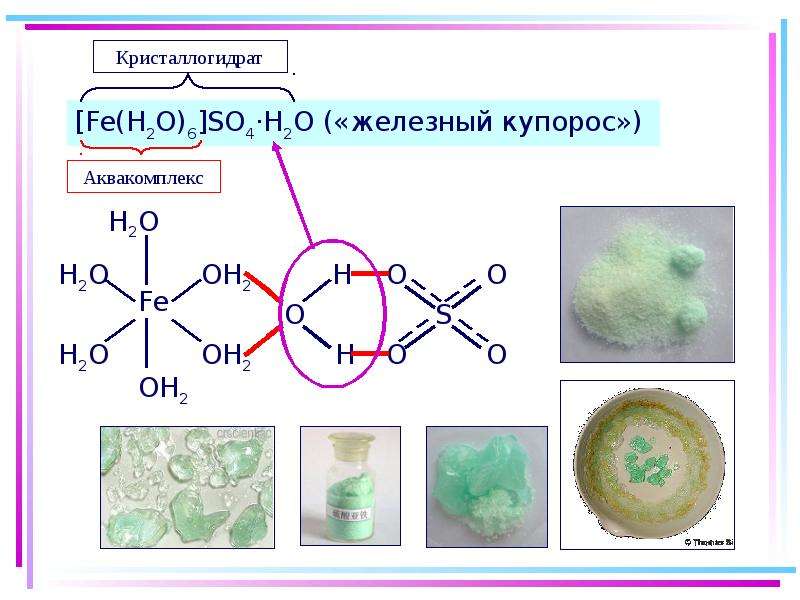
Содержание слайда: Аквакомплексы
№5 слайд
Содержание слайда: 2. Гидроксокомплексы
Получение:
Zn(OH)2 + 2OH–(изб.) = [Zn(OH)4]2–; pH >> 7
Разрушение:
[Zn(OH)4]2– (+H3O+)
+ CH3COOH; CO2; NH4+ (сл.к-ты, pH 7)
Zn(OH)2(т)
+ H3O+ (сильн.к-ты, pH < 7)
[Zn(H2O)4]2+
Образование гидроксокомплексов характерно для амфотерных элементов.
№6 слайд
Содержание слайда: 3. Аммины (аммиакаты)
Получение:
AgCl(т) + 2NH3·H2O(изб.) = [Ag(NH3)2]+ +Cl– + 2H2O
Разрушение:
[Ag(NH3)2]+ + H3O+ NH4+ + …
[Ag(NH3)2]+ + I– AgI(т) + …
[Ag(NH3)2]+ + t° NH3(г) + …
№7 слайд
Содержание слайда: 4. Ацидокомплексы
Получение:
HgI2(т) + 2I–(изб.) = [HgI4]2–
[Fe(H2O)6]3+ + 6NCS−=[Fe(NCS)6]3− + 6H2O
Разрушение:
[HgI4]2– + S2– = HgS(т) + 4I–
[Fe(NCS)6]3− + 4F− = [FeF4]− + 6NCS−
№8 слайд
Содержание слайда: 5. Гидридокомплексы
Получение:
4 NaH + B(OCH3)3 = Na[BH4] + 3CH3ONa (при 250 C)
4 LiH + AlCl3 = Li[AlH4] + 3LiCl
3 Li[BH4] + AlCl3 = Al[BH4]3 + 3LiCl
Разрушение:
Na[AlH4] + 4 H2O = NaOH + Al(OH)3 + 4 H2 (ОВР)
2 Na[BH4] + H2SO4 = Na2SO4 + B2H6 + 2 H2 (ОВР)
№9 слайд
Содержание слайда: 6. Анионгалогенаты M[ЭГmГn] (Э, Г и Г – галогены)
Получение:
KI + I2 = K[I(I)2]; CsCl + IBr = Cs[I(Br)(Cl)]
Разрушение:
K[I(I)2] + t° = KI + I2(г)
Cs[I(Br)(Cl)] + t° = CsCl + IBr(г)
№10 слайд
Содержание слайда: 8. Карбонилы
Получение:
Ni(т) + 4CO(г) = [Ni(CO)4](ж) (ниже 50 С)
тетракарбонилникель(0)
Разрушение:
[Ni(CO)4](ж) + t° = Ni(т) + 4 CO(г) (выше 200 С)
[Ni(CO)4] + H2SO4(разб.) = NiSO4 + 4 CO + H2
№11 слайд
Содержание слайда: Правило Сиджвика для определения состава комплексов
№12 слайд
Содержание слайда: Правило Сиджвика (примеры)
* 27Co0 [Ar]3d74s2 || 36Kr
* 18 – 9 = 9e –;
* х = 9/2 = 4,5 (?)
* радикал [·Co(CO)4]
* тетракарбонилкобальт
(неуст.)
* димер [Co2(CO)8] (уст.) октакарбонилдикобальт
№13 слайд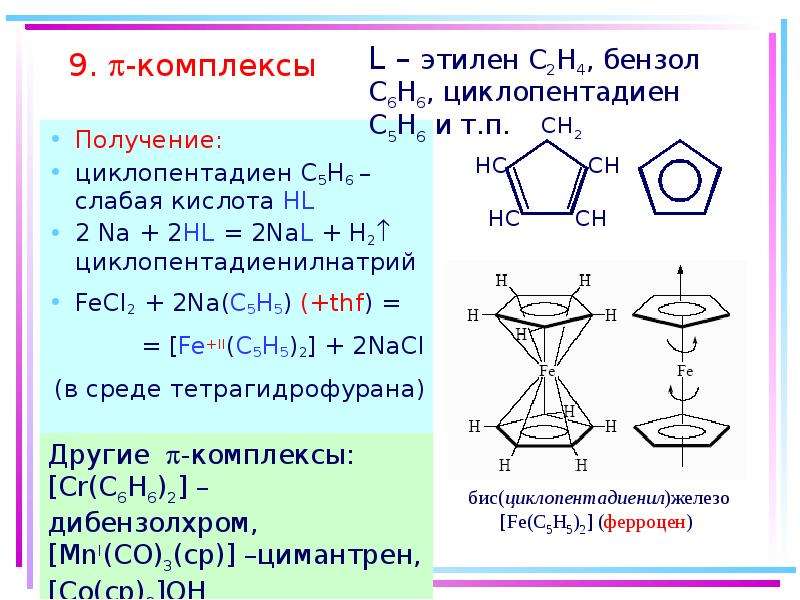
Содержание слайда: 9. -комплексы
Получение:
циклопентадиен С5H6 – слабая кислота HL
2 Na + 2HL = 2NaL + H2 циклопентадиенилнатрий
FeCl2 + 2Na(C5H5) (+thf) =
= [Fe+II(C5H5)2] + 2NaCl
(в среде тетрагидрофурана)
№14 слайд
Содержание слайда: 10. Хелаты
Внутр. сфера состоит из циклич. группировок, включающих M (комплексообразователь)
NH2CH2COOH-аминоуксусная кислота (глицин)
Cu(OH)2 + 2 NH2CH2COOH =
= [Cu(NH2CH2COO)2] + 2 H2O
NH2CH2COO (глицинат-ион) - бидентатный лиганд
№15 слайд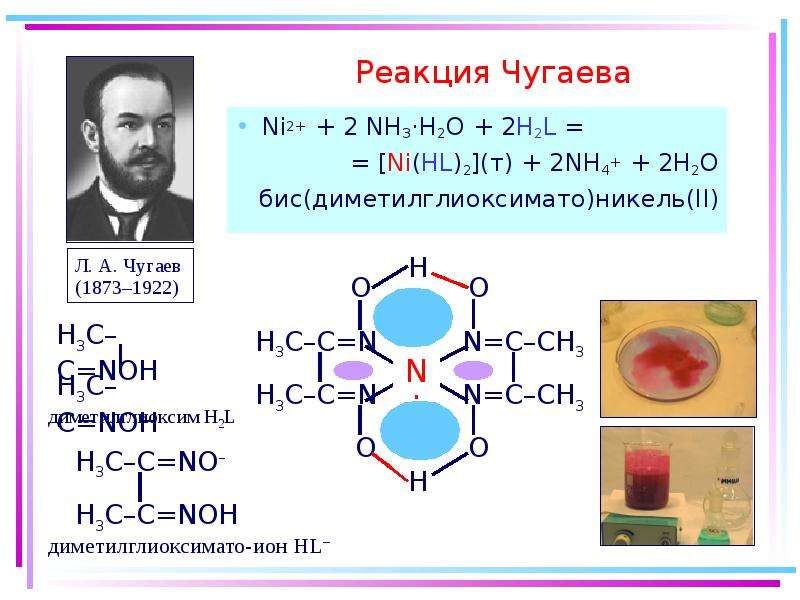
Содержание слайда: Реакция Чугаева
Ni2+ + 2 NH3·H2O + 2H2L =
= [Ni(HL)2](т) + 2NH4+ + 2H2O
бис(диметилглиоксимато)никель(II)
№16 слайд
Содержание слайда: Методы синтеза комплексных соединений
Реакция обмена лигандов
А) в водном растворе (обр, принцип Ле Шателье):
[Сu(H2O)4]2+ + 4NH3·H2O = [Cu(NH3)4]2+ + 8H2O
(обр. прод.) > (обр. исх.реаг.)
Б) в неводном растворителе:
[Al(H2O)6]3+ + NH3·H2O
[Al(H2O)6]3+(s) + 6NH3(ж) = [Al(NH3)6]3+(s) + 6H2O(s)
В) без растворителя:
[Ni(H2O)6]Cl2(т) + 6NH3(г) = [Ni(NH3)6]Cl2(т) +6H2O(г)
Г) внутримол. обмен лигандов в тв. фазе:
2[Co(H2O)6]Cl2(т) + t° = Co[CoCl4](т) + 12H2O
розовый синий
№17 слайд
Содержание слайда: Методы синтеза комплексных соединений
Д) ОВР + реакции обмена лигандов
+Ок.+ L
[СoII(H2O)6]2+ [СoIIIL6]3+
Ок.: H2O2, KNO2 … L – NH3, NO2– …
Примеры:
2CoIICl2 + 12NH3 + H2O2 = 2[CoIII(NH3)6](OH)Cl2
CoIICl2 + 7KNO2 + 2CH3COOH =
= K3[CoIII(NO2)6] + NO + 2KCl + 2CH3COOK + H2O
+ Вс
[NiII(CN)4]2– [Ni0(CN)4]4–
№18 слайд
Содержание слайда: Решение задач. 1. Растворение осадка при комплексообразовании
AgBr(т) Ag+ + Br – ; ПРAgBr = 7,7·10–13
Ag+ + 2 SO3S2– [Ag(SO3S)2]3– ; обр = 4·1013
AgBr(т) + 2 SO3S2– [Ag(SO3S)2]3– + Br –;
Kc = ?
№19 слайд
Содержание слайда: Решение задач. 2. Реакция обмена лигандов
[Co(NH3)6]3+ + 6 CN– [Co(CN)6]3– + 6 NH3 ;
Kc = ?
Co3+ + 6 NH3 [Co(NH3)6]3+ ; обр(1) = 1,6·1035
Co3+ + 6 CN– [Co(CN)6]3– ; обр(2) = 1,0·1064
№20 слайд
Содержание слайда: Решение задач. 3. Разрушение комплекса
[Cu(NH3)4]2+ + 4 H3O+ [Cu(H2O)4]2+ + 4 NH4+ ;
Kc = ?
Cu2+ + 4 NH3 [Cu(NH3)4]2+ ; обр = 7,9·1012
NH4+ + 2H2O NH3·H2O + H3O+ ; Kк = 5,75·10–10
№21 слайд
Содержание слайда: Решение задач. 4. Направление реакции
CuCN(т) + H2O + HCN [Cu(CN)2]– + H3O+
Kc = ?
Cu+ + 2CN– [Cu(CN)2]– ; обр = 1,0·1024
HCN + H2O CN– + H3O+ ; Kк = = 4,93·10–10
CuCN(т) Cu+ + CN– ; ПРCuCN = 3,2·10–20






























